Clear Sky Science · it
Esosomi derivati da MSC peritoneali sopprimono la sintesi di CCL24 tramite il trasporto di miR-320d contribuendo al miglioramento della fibrosi associata alla dialisi peritoneale
Perché è importante proteggere la membrana della dialisi
Per le persone con insufficienza renale, la dialisi peritoneale offre la possibilità di depurare il sangue a casa utilizzando la membrana addominale come filtro naturale. Tuttavia, nel corso degli anni questa delicata membrana può cicatrizzarsi e ispessirsi, costringendo infine i pazienti ad abbandonare il trattamento. Questo studio indaga le cause di tale cicatrizzazione e testa una strategia cellulare avanzata che impiega piccole vescicole biologiche per attenuare segnali immunitari dannosi e contribuire a mantenere la membrana in salute.
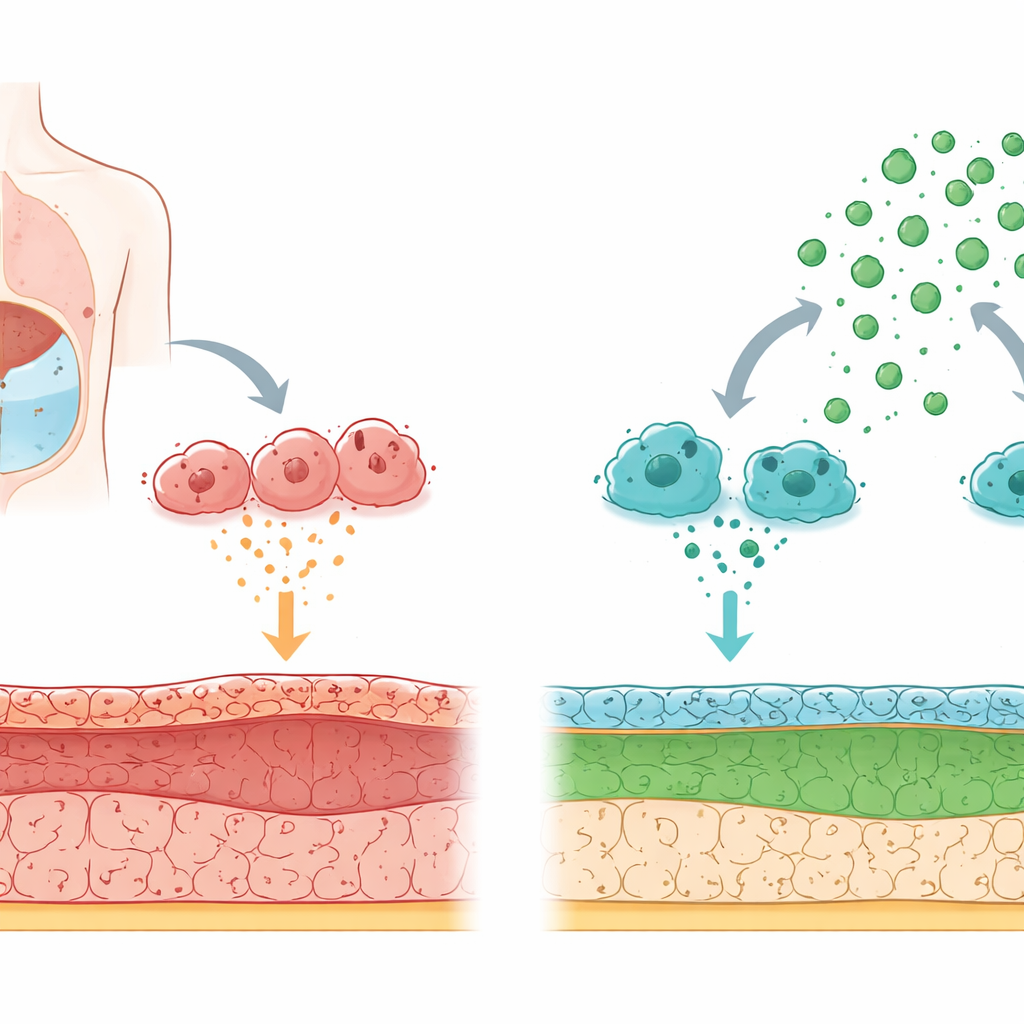
Come il filtro dell’organismo si danneggia nel tempo
La dialisi peritoneale funziona riempiendo l’addome con un liquido speciale affinché le scorie possano passare dal sangue attraverso la membrana peritoneale. L’esposizione prolungata a soluzioni di dialisi ad alto contenuto di glucosio e le infiammazioni ricorrenti danneggiano gradualmente questa guaina. Le cellule a contatto con il liquido possono cambiamento il loro carattere: invece di comportarsi come tessuto di rivestimento liscio e protettivo, iniziano ad assumere un profilo più simile a cellule produttrici di cicatrici che depositano fibre rigide. Questo spostamento, noto come transizione da cellule di rivestimento a cellule simili a fibroblasti, guida l’ispessimento e la perdita di funzione della membrana.
Messaggeri immunitari che spingono verso la formazione di cicatrici
I ricercatori si sono concentrati sui macrofagi, cellule immunitarie che pattugliano la cavità peritoneale. In un modello murino di danno indotto dalla dialisi hanno osservato livelli elevati di una proteina segnale chiamata CCL24 principalmente in questi macrofagi. Quando i macrofagi producevano più CCL24, le cellule del rivestimento vicine perdevano la loro struttura ordinata e cominciavano a sintetizzare proteine fibrose, tipiche della cicatrizzazione. Bloccare CCL24 nei macrofagi, o inibire il suo recettore di superficie (noto come CCR3) o l’interruttore chimico a valle (una via che coinvolge la proteina p38), impediva alle cellule di rivestimento di trasformarsi in cellule produttrici di cicatrici. Ciò colloca la CCL24 derivata dai macrofagi al centro del processo di fibrosi.
Pacchetti cellulari che calmano segnali dannosi
Il gruppo ha quindi rivolto l’attenzione a cellule stromali mesenchimali raccolte dal liquido di scarto dei pazienti in dialisi. Queste cellule rilasciano naturalmente esosomi—vescicole nanometriche che trasportano messaggi molecolari come piccoli RNA. Quando i macrofagi venivano esposti al fluido proveniente da queste cellule staminali, o a esosomi purificati, la loro produzione e il rilascio di CCL24 calavano nettamente. Di conseguenza l’influenza dannosa delle secrezioni dei macrofagi sul rivestimento peritoneale si riduceva e le cellule di rivestimento mantenevano di più le loro caratteristiche protettive. Rimuovere gli esosomi dal fluido delle cellule staminali annullava in gran parte questo beneficio, mostrando che queste piccole vescicole sono i principali messaggeri terapeutici.
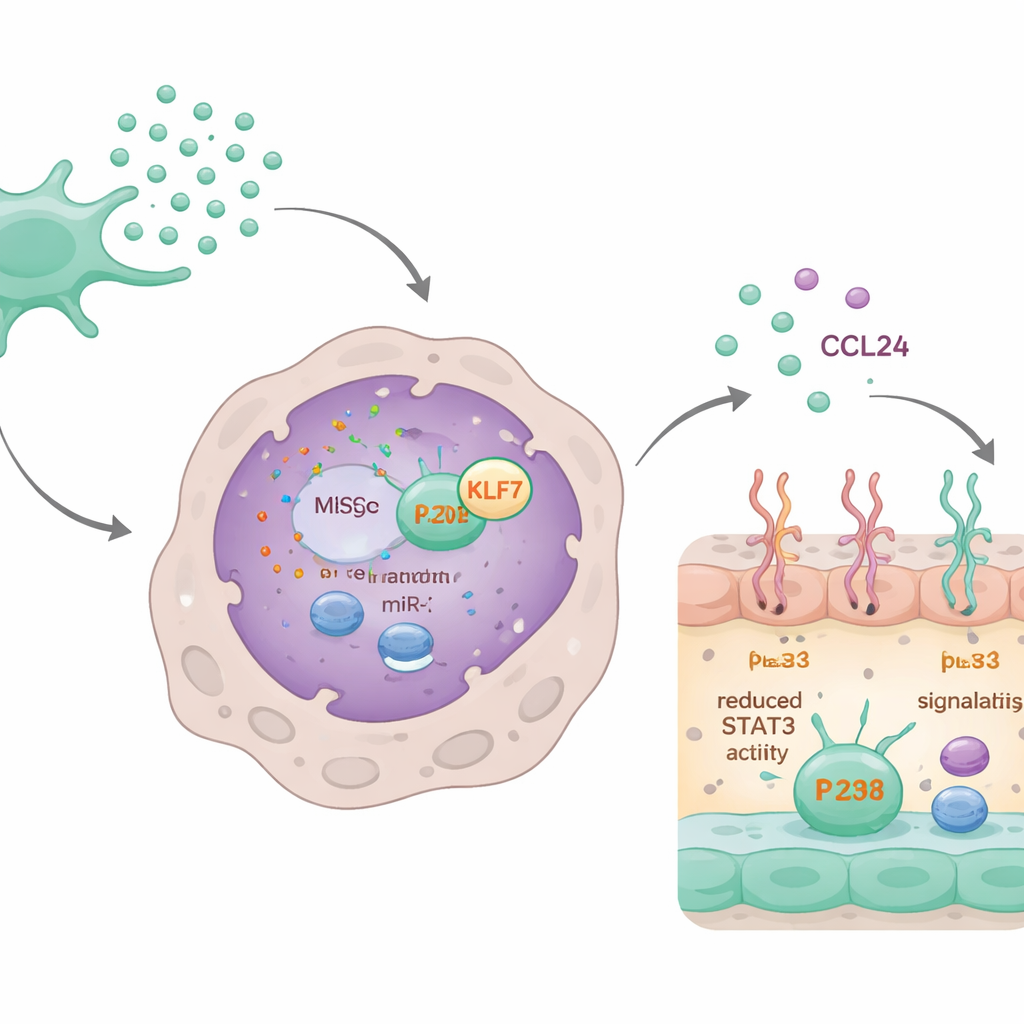
Il circuito del microRNA che spegne la fibrosi
Approfondendo, gli scienziati hanno scoperto che un microRNA specifico, miR-320d, contenuto negli esosomi era determinante. I macrofagi assorbivano agevolmente esosomi caricati con questo microRNA. Una volta all’interno, miR-320d si legava e riduceva i livelli di una proteina chiamata KLF7, che normalmente favorisce l’attivazione di un’altra proteina, STAT3. STAT3 attivata si lega al gene CCL24 e ne aumenta la produzione. Riducendo KLF7, miR-320d diminuiva l’attivazione di STAT3, il che a sua volta abbassava la sintesi e la secrezione di CCL24. Quando miR-320d veniva bloccato o KLF7 aumentato artificialmente, l’effetto calmante degli esosomi su CCL24 e sul comportamento dei macrofagi scompariva in larga misura.
Dalla coltura cellulare agli animali viventi
I ricercatori hanno ingegnerizzato le cellule staminali per rilasciare esosomi arricchiti con miR-320d supplementare e le hanno confrontate con esosomi non modificati. Gli esosomi potenziati venivano assorbiti con maggiore efficienza dai macrofagi e producevano riduzioni più marcate nei livelli di KLF7, nell’attività di STAT3 e nel rilascio di CCL24. In ratti sottoposti a un trattamento simile alla dialisi, iniezioni settimanali di esosomi standard o ricchi di miR-320d riducevano l’ispessimento e l’accumulo di collagene nella membrana peritoneale. Gli esosomi potenziati fornivano la protezione maggiore, preservando un aspetto più normale del tessuto e attenuando i passaggi chiave della segnalazione che portano dall’attivazione dei macrofagi alla trasformazione delle cellule di rivestimento e alla fibrosi.
Cosa può significare per le persone in dialisi
Questo lavoro delinea una catena di eventi in cui i macrofagi rilasciano CCL24, spingendo il rivestimento verso uno stato cicatrizzato e meno funzionale. Gli esosomi derivati dalle cellule staminali peritoneali, specialmente se caricati con miR-320d, interrompono questa catena silenziando l’interruttore di controllo KLF7–STAT3 che attiva CCL24. In termini pratici, lo studio suggerisce che gli esosomi derivati dalle cellule staminali del paziente potrebbero un giorno essere usati come terapia personalizzata e senza cellule per rallentare o prevenire il danno alla membrana peritoneale, aiutando le persone a rimanere in dialisi peritoneale più a lungo con meno complicanze.
Citazione: Zhao, X., Xi, M., Qi, H. et al. Peritoneal MSCs-derived exosomes suppress CCL24 synthesis through miR-320d delivery contributing to the improvement of peritoneal dialysis-associated fibrosis. Sci Rep 16, 11998 (2026). https://doi.org/10.1038/s41598-026-42489-w
Parole chiave: dialisi peritoneale, fibrosi peritoneale, macrofagi, esosomi, terapia con microRNA