Clear Sky Science · pl
Egzosomy pochodzące z mezenchymalnych komórek macierzystych otrzewnej hamują syntezę CCL24 poprzez dostarczenie miR-320d, przyczyniając się do poprawy włóknienia związanego z dializą otrzewnową
Dlaczego ochrona wyściółki dializacyjnej ma znaczenie
Dla osób z niewydolnością nerek dializa otrzewnowa daje wolność oczyszczania krwi w domu, wykorzystując naturalną wyściółkę jamy brzusznej jako filtr. Jednak wraz z upływem lat ta delikatna błona może ulegać bliznowaceniu i stwardnieniu, co ostatecznie zmusza pacjentów do zaprzestania leczenia. W badaniu analizowano mechanizmy powstawania tych zmian oraz testowano nowatorską strategię komórkową, wykorzystującą drobne biologiczne „paczki” do tłumienia szkodliwych sygnałów układu odpornościowego i utrzymania zdrowia błony.
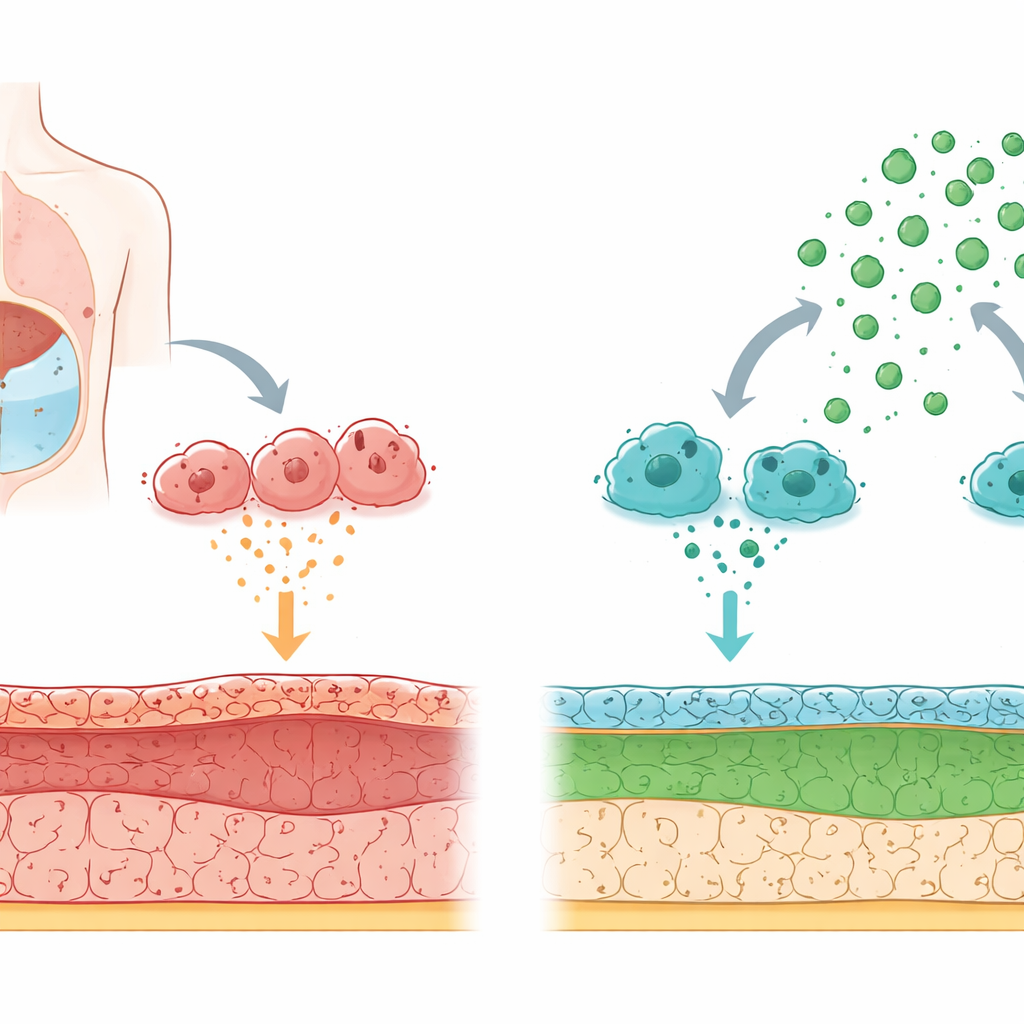
Jak filtr organizmu ulega uszkodzeniu z czasem
Dializa otrzewnowa polega na wypełnieniu jamy brzusznej specjalnym płynem, aby zbędne produkty przemiany materii przeszły z krwi przez błonę otrzewnową. Długotrwała ekspozycja na płyny dializacyjne o wysokiej zawartości glukozy oraz powtarzające się stany zapalne stopniowo uszkadzają tę wyściółkę. Komórki mające kontakt z płynem mogą zmieniać charakter: zamiast pełnić rolę gładkich, ochronnych „płytek”, zaczynają zachowywać się jak komórki tworzące blizny, odkładające sztywne włókna. Ta przemiana, określana jako przekształcenie komórek wyściółki w komórki o cechach fibroblastycznych, napędza pogrubienie i utratę funkcji błony.
Immunologiczne sygnały skłaniające komórki do bliznowacenia
Naukowcy skupili się na makrofagach — komórkach odpornościowych patrolujących jamę otrzewnową. W modelu szczurzym uszkodzeń wywołanych dializą wykryli wysokie poziomy białka sygnalizacyjnego CCL24, głównie w tych makrofagach. Gdy makrofagi wytwarzały więcej CCL24, pobliskie komórki wyściółki traciły porządek strukturalny i zaczynały produkować białka włókniste, co jest znakiem bliznowacenia. Zablokowanie CCL24 w makrofagach, albo zablokowanie jego receptora powierzchniowego (CCR3) czy też hamowanie jego dalszego szlaku sygnałowego (obejmującego białko p38) zapobiegało przemianie komórek wyściółki w komórki fibroblastyczne. To stawia CCL24 pochodzące z makrofagów w centrum procesu bliznowacenia.
„Paczki” z komórek macierzystych, które uciszają szkodliwe sygnały
Zespół zwrócił się następnie do mezenchymalnych komórek macierzystych pozyskanych z płynu odpadowego pacjentów poddawanych dializie. Komórki te naturalnie uwalniają egzosomy — pęcherzyki o rozmiarach nanometrów niosące molekularne komunikaty, takie jak małe RNA. Gdy makrofagi eksponowano na płyn pochodzący od tych komórek lub na oczyszczone egzosomy, ich produkcja i uwalnianie CCL24 gwałtownie spadały. W rezultacie szkodliwy wpływ wydzielin makrofagów na wyściółkę otrzewnej zmniejszał się, a komórki wyściółki zachowywały więcej cech ochronnych. Usunięcie egzosomów z płynu komórkowego w dużej mierze niwelowało tę korzyść, co wskazuje, że to właśnie te drobne „paczki” są głównymi nośnikami terapeutycznego efektu.
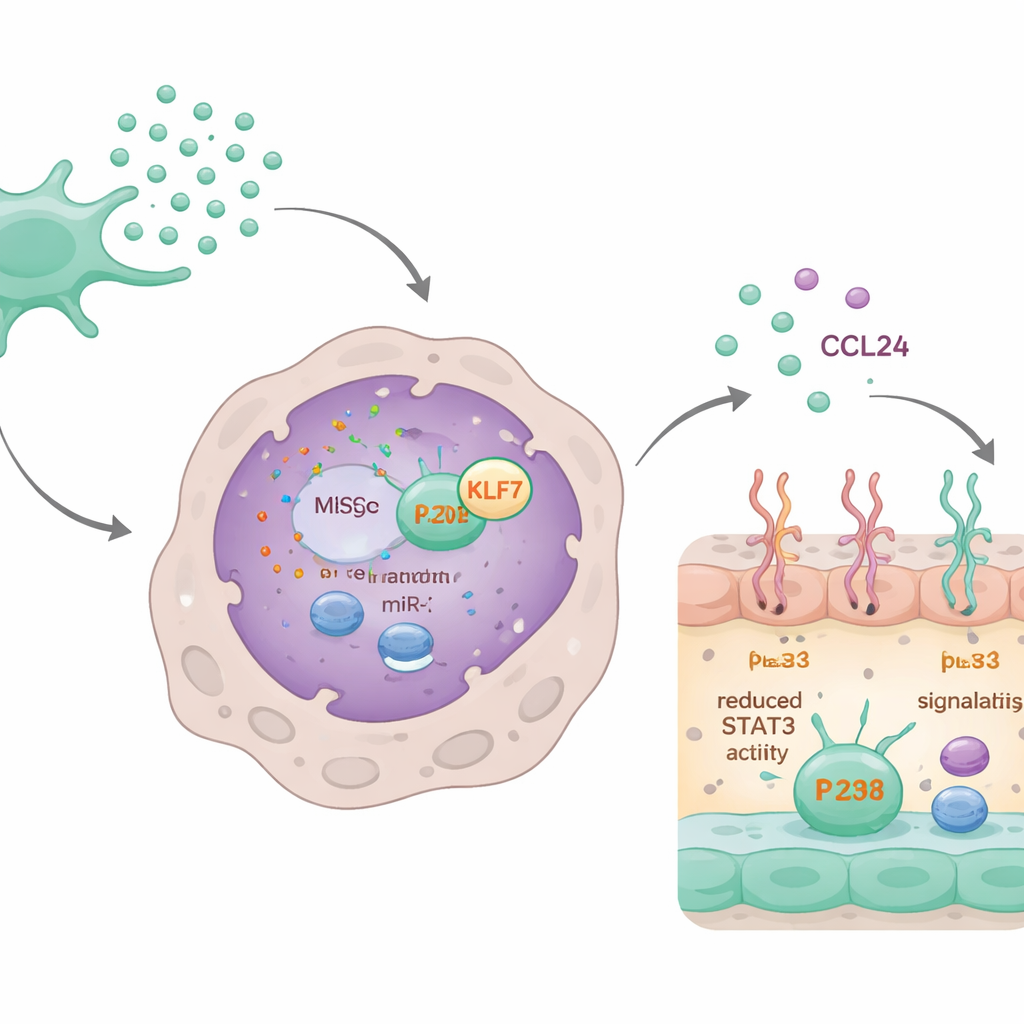
Obwód mikroRNA, który wyłącza bliznowacenie
Wnikliwsze badania wykazały, że kluczową rolę odgrywa specyficzny mikroRNA, miR-320d, przenoszony w egzosomach. Makrofagi chętnie pobierały egzosomy zawierające ten mikroRNA. Po wejściu do komórki miR-320d wiązał się z białkiem KLF7 i obniżał jego poziom — KLF7 normalnie pomaga aktywować kolejne białko, STAT3. Aktywowany STAT3 wiąże się z genem CCL24 i zwiększa jego ekspresję. Poprzez obniżenie KLF7, miR-320d redukował aktywację STAT3, co z kolei zmniejszało syntezę i wydzielanie CCL24. Gdy miR-320d był blokowany albo gdy sztucznie zwiększano poziom KLF7, uspokajający wpływ egzosomów na CCL24 i zachowanie makrofagów w dużej mierze zanikał.
Z hodowli komórek do zwierząt żywych
Naukowcy zaprojektowali komórki macierzyste tak, by wydzielały egzosomy wzbogacone o dodatkowe miR-320d i porównali je z niezmodyfikowanymi egzosomami. Wzmocnione egzosomy były szybciej pobierane przez makrofagi i wywoływały silniejsze spadki poziomów KLF7, aktywności STAT3 oraz uwalniania CCL24. U szczurów poddawanych zabiegowi przypominającemu dializę, cotygodniowe iniekcje zarówno standardowych, jak i bogatych w miR-320d egzosomów zmniejszały pogrubienie i nagromadzenie kolagenu w błonie otrzewnej. Egzosomy z dodatkiem miR-320d zapewniały największą ochronę, zachowując bardziej prawidłowy wygląd tkanki i tłumiąc kluczowe kroki sygnałowe prowadzące od aktywacji makrofagów do przekształcenia komórek wyściółki i bliznowacenia.
Co to może znaczyć dla pacjentów dializowanych
Badanie układa łańcuch zdarzeń, w którym makrofagi uwalniają CCL24, skłaniając wyściółkę dializacyjną do stanu bliznowacenia i utraty funkcji. Egzosomy z komórek macierzystych otrzewnej, zwłaszcza gdy są nasycone miR-320d, przerywają ten łańcuch, wyciszając przełącznik kontrolny KLF7–STAT3, który włącza produkcję CCL24. W praktycznym ujęciu oznacza to, że egzosomy pochodzące od samych pacjentów mogłyby w przyszłości posłużyć jako spersonalizowana, bezkomórkowa terapia spowalniająca lub zapobiegająca uszkodzeniom błony otrzewnej, pozwalając pacjentom dłużej pozostawać na dializie otrzewnowej przy mniejszej liczbie powikłań.
Cytowanie: Zhao, X., Xi, M., Qi, H. et al. Peritoneal MSCs-derived exosomes suppress CCL24 synthesis through miR-320d delivery contributing to the improvement of peritoneal dialysis-associated fibrosis. Sci Rep 16, 11998 (2026). https://doi.org/10.1038/s41598-026-42489-w
Słowa kluczowe: dializa otrzewnowa, włóknienie otrzewnej, makrofagi, egzosomy, terapia mikroRNA