Clear Sky Science · sv
Exosomer från peritoneala MSC hämmar CCL24‑syntes genom leverans av miR-320d och bidrar till förbättring av peritoneal dialysassocierad fibros
Varför det är viktigt att skydda dialysmembranet
För personer vars njurar har slutat fungera erbjuder peritoneal dialys friheten att rena blodet hemma genom att använda bukhinna som ett naturligt filter. Men över år kan denna känsliga hinna skadas och förtjockas, vilket till slut tvingar patienter att avbryta behandlingen. Denna studie undersöker varför ärrbildningen uppstår och prövar en modern cellbaserad strategi som använder små biologiska paket för att dämpa skadliga immunsignaler och hjälpa till att bevara hinnans hälsa.
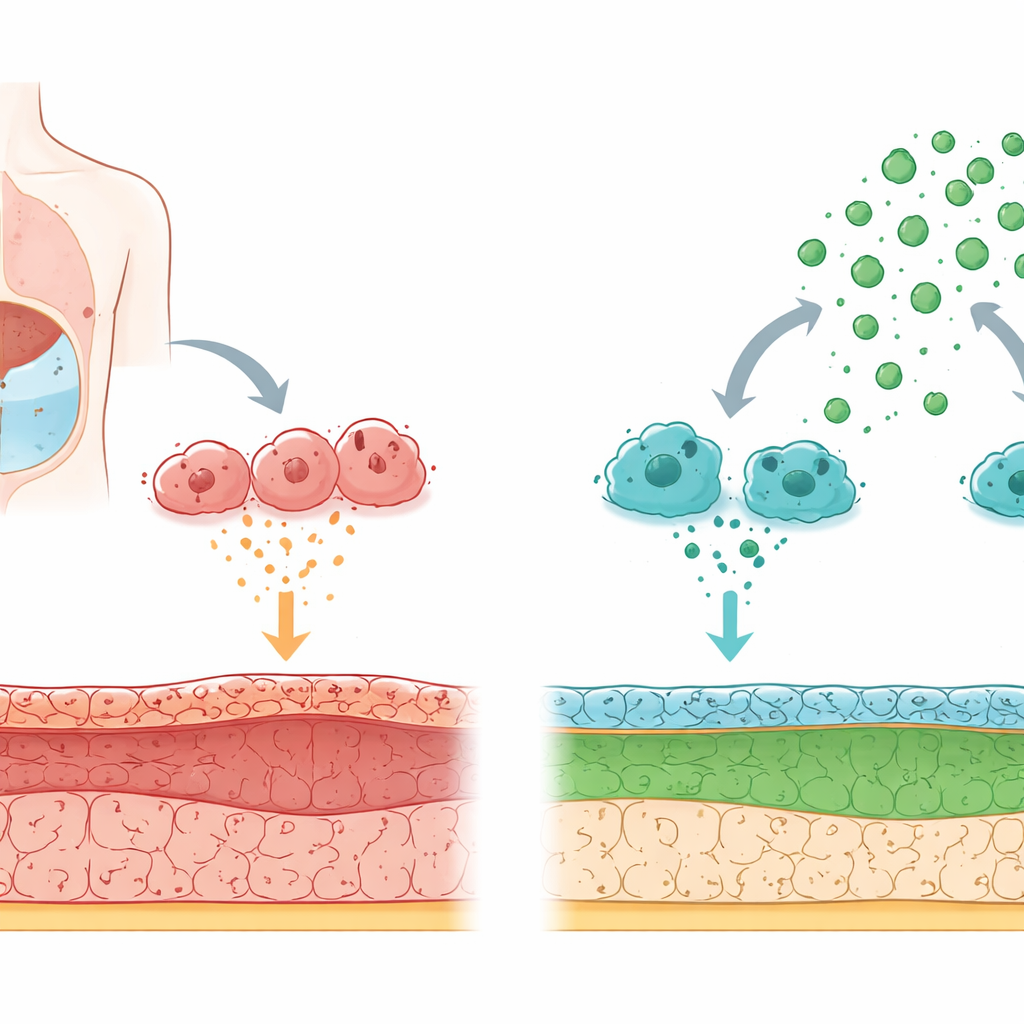
Hur kroppens filter skadas över tid
Peritoneal dialys fungerar genom att fylla buken med en särskild vätska så att avfallsprodukter kan passera från blodet över peritonealmembranet. Långvarig exponering för högglukos dialysvätska och upprepad inflammation skadar gradvis denna hinna. Cellerna som vetter mot vätskan kan förändra karaktär: i stället för att bete sig som släta, skyddande plattor börjar de agera mer som ärrbildande celler som avsätter styva fibrer. Denna omvandling, kallad övergång från hinnceller till ärrlika celler, driver förtjockning och funktionsförlust i membranet.
Immunsignaler som driver celler mot ärrbildning
Forskarlaget fokuserade på makrofager, immunceller som patrullerar peritonealrummet. I en råttmodell för dialysinducerad skada fann de höga nivåer av ett signalprotein kallat CCL24 främst i dessa makrofager. När makrofager producerade mer CCL24 förlorade intilliggande hinnceller sin ordnade struktur och började producera fibrösa proteiner, ett kännetecken för ärrbildning. Att blockera CCL24 i makrofager, eller att blockera dess ytreceptor (känd som CCR3) eller dess nedströms kemiska omkopplare (en väg som involverar proteinet p38), förhindrade att hinncellerna omvandlades till ärrbildande celler. Detta placerade makrofagderiverat CCL24 i centrum för ärrprocessen.
Stamcellspaket som tystar skadliga signaler
Gruppen vände sig sedan till mesenkymala stamceller insamlade från dialyspatienters dräneringsvätska. Dessa celler frisätter naturligt exosomer—nanometerstora vesiklar som bär molekylära budskap såsom små RNA-molekyler. När makrofager exponerades för vätska från dessa stamceller, eller för renade exosomer, sjönk deras produktion och utsöndring av CCL24 kraftigt. Som ett resultat minskade den skadliga påverkan från makrofagsekret på peritonealhinnan, och hinncellerna behöll fler av sina skyddande egenskaper. Att ta bort exosomer från stamcellsvätskan upphävde i stort sett denna fördel, vilket visar att dessa små paket är de huvudsakliga terapeutiska budbärarna.
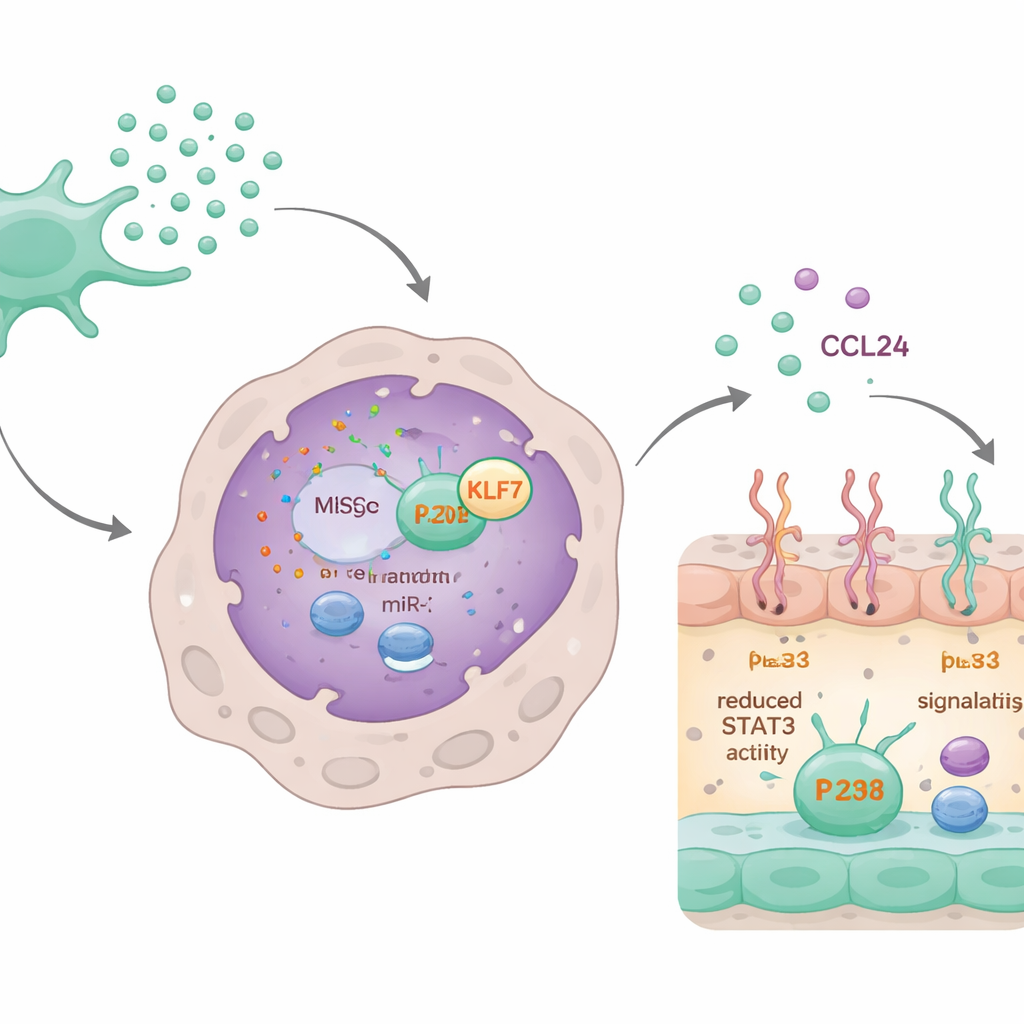
microRNA‑kretsen som släcker ärrbildningen
Vid djupare analys upptäckte forskarna att ett specifikt microRNA, miR‑320d, som transporterades inuti exosomerna var avgörande. Makrofager tog lätt upp exosomer innehållande detta microRNA. Väl inne i cellen band miR‑320d till och sänkte nivåerna av ett protein kallat KLF7, som normalt hjälper till att aktivera ett annat protein, STAT3. Aktiverat STAT3 binder till CCL24‑genen och ökar dess uttryck. Genom att minska KLF7 reducerade miR‑320d STAT3‑aktiveringen, vilket i sin tur sänkte CCL24‑syntes och sekretion. När miR‑320d blockerades eller KLF7 artificiellt ökades, försvann exosomernas lugnande effekt på CCL24 och makrofagernas beteende i stor utsträckning.
Från cellodling till levande djur
Forskarna konstruerade stamceller för att frisätta exosomer berikade med extra miR‑320d och jämförde dem med omodifierade exosomer. De förstärkta exosomerna togs upp mer effektivt av makrofager och gav kraftigare minskningar av KLF7‑nivåer, STAT3‑aktivitet och CCL24‑utsöndring. I råttor som genomgick dialysliknande behandling minskade veckovisa injektioner av antingen standard‑ eller miR‑320d‑rika exosomer förtjockning och kollagenansamling i peritonealmembranet. De förstärkta exosomerna gav bäst skydd, bevarade ett mer normalt vävnadsutseende och dämpade de centrala signalstegen som leder från makrofagaktivering till hinncellsomvandling och ärrbildning.
Vad detta kan betyda för personer som genomgår dialys
Arbetet beskriver en händelsekedja där makrofager frisätter CCL24, vilket driver dialyshinnan mot ett ärrat, mindre funktionellt tillstånd. Exosomer från peritoneala stamceller, särskilt när de är packade med miR‑320d, bryter denna kedja genom att stänga av KLF7–STAT3‑reglaget som slår på CCL24. I praktiska termer tyder studien på att en patients egna stamcellsderiverade exosomer en dag skulle kunna användas som en personlig, cellfri terapi för att bromsa eller förhindra skador på peritonealmembranet, så att patienter kan stanna kvar på peritoneal dialys längre med färre komplikationer.
Citering: Zhao, X., Xi, M., Qi, H. et al. Peritoneal MSCs-derived exosomes suppress CCL24 synthesis through miR-320d delivery contributing to the improvement of peritoneal dialysis-associated fibrosis. Sci Rep 16, 11998 (2026). https://doi.org/10.1038/s41598-026-42489-w
Nyckelord: peritoneal dialys, peritoneal fibros, makrofager, exosomer, microRNA‑terapi