Clear Sky Science · es
Exosomas derivados de MSCs peritoneales suprimen la síntesis de CCL24 mediante la entrega de miR-320d contribuyendo a la mejora de la fibrosis asociada a la diálisis peritoneal
Por qué importa proteger el revestimiento de la diálisis
Para las personas con fallo renal, la diálisis peritoneal ofrece la posibilidad de depurar la sangre en casa usando el revestimiento abdominal como filtro natural. Pero con los años, esta membrana delicada puede cicatrizar y engrosarse, llegando a obligar a los pacientes a abandonar el tratamiento. Este estudio analiza por qué se produce esa cicatrización y ensaya una estrategia celular de vanguardia que utiliza diminutos paquetes biológicos para calmar señales inmunitarias dañinas y ayudar a mantener la membrana sana.
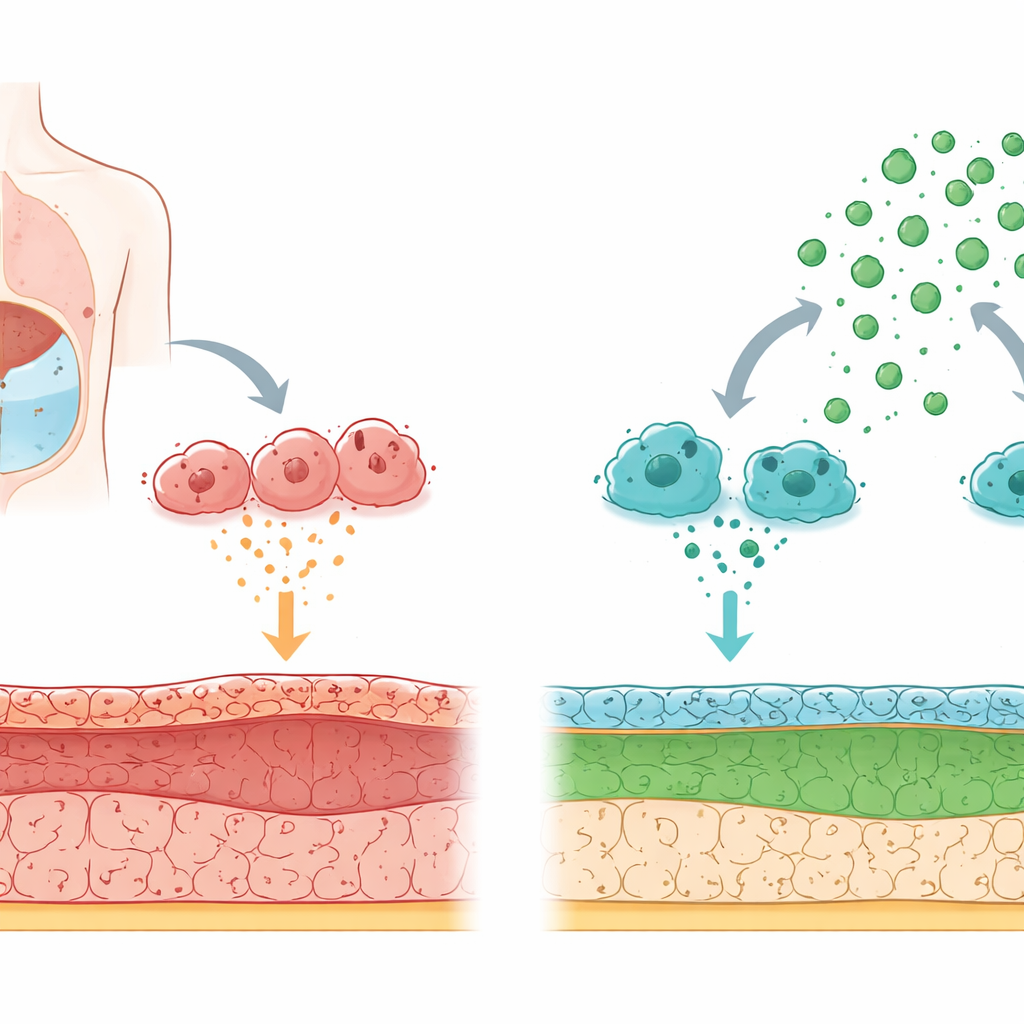
Cómo se daña el filtro del cuerpo con el tiempo
La diálisis peritoneal funciona llenando el abdomen con un líquido especial para que los desechos pasen de la sangre a través de la membrana peritoneal. La exposición prolongada a líquidos de diálisis con alto contenido de glucosa y la inflamación repetida lesionan poco a poco este revestimiento. Las células que miran hacia el líquido pueden cambiar de carácter: en lugar de comportarse como azulejos lisos y protectores, comienzan a actuar más como células formadoras de cicatriz que depositan fibras rígidas. Este cambio, llamado transición de células del revestimiento a células con aspecto cicatricial, impulsa el engrosamiento y la pérdida de funcionalidad de la membrana.
Mensajeros inmunitarios que empujan a las células hacia la cicatrización
Los investigadores se centraron en los macrófagos, células inmunitarias que patrullan la cavidad peritoneal. En un modelo de rata con lesión inducida por diálisis, encontraron niveles elevados de una proteína señal denominada CCL24 principalmente en estos macrófagos. Cuando los macrófagos producían más CCL24, las células vecinas del revestimiento perdían su estructura ordenada y empezaban a producir proteínas fibrilares, un sello de la cicatrización. Bloquear CCL24 en los macrófagos, o bloquear su receptor de superficie (conocido como CCR3) o su interruptor químico aguas abajo (una vía que involucra la proteína p38), evitó que las células del revestimiento se convirtieran en células formadoras de cicatriz. Esto situó a CCL24 derivado de macrófagos en el centro del proceso de cicatrización.
Paquetes de células madre que apagan señales dañinas
El equipo se dirigió entonces a células madre mesenquimales obtenidas del líquido de desecho de pacientes en diálisis. Estas células liberan de forma natural exosomas—vesículas de tamaño nanométrico que transportan mensajes moleculares como pequeños ARN. Cuando los macrófagos se expusieron al fluido de estas células madre, o a exosomas purificados, su producción y liberación de CCL24 cayó drásticamente. Como resultado, la influencia dañina de las secreciones de los macrófagos sobre el revestimiento peritoneal disminuyó y las células del revestimiento conservaron más de sus características protectoras. La eliminación de los exosomas del fluido de las células madre borró en gran medida este beneficio, mostrando que estos diminutos paquetes son los principales mensajeros terapéuticos.
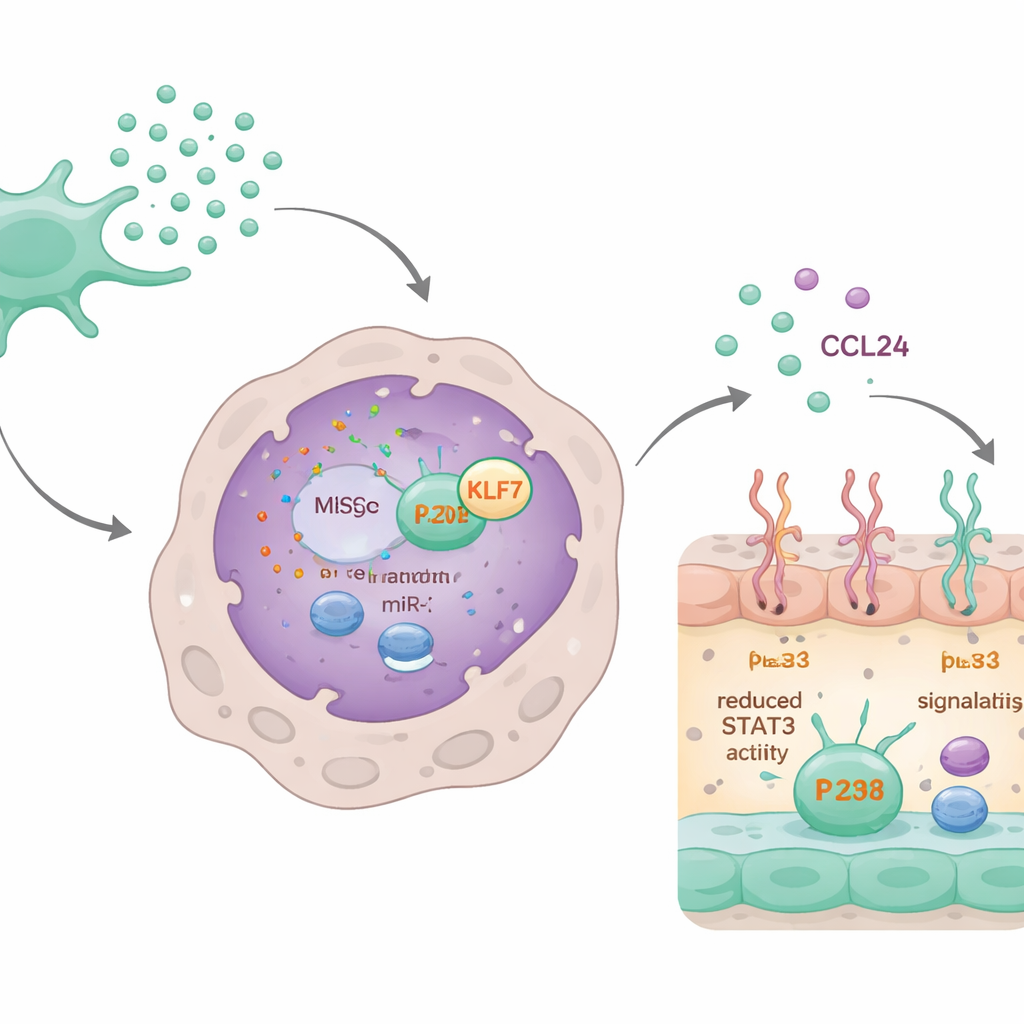
El circuito de microARN que apaga la cicatrización
Profundizando, los científicos descubrieron que un microARN específico, miR-320d, transportado dentro de los exosomas era clave. Los macrófagos incorporaron con facilidad exosomas cargados con este microARN. Una vez dentro, miR-320d se unió y redujo los niveles de una proteína llamada KLF7, que normalmente ayuda a activar otra proteína, STAT3. STAT3 activada se une al gen de CCL24 y aumenta su producción. Al reducir KLF7, miR-320d disminuyó la activación de STAT3, lo que a su vez redujo la síntesis y secreción de CCL24. Cuando se bloqueó miR-320d o se aumentó artificialmente KLF7, el efecto calmante de los exosomas sobre CCL24 y el comportamiento de los macrófagos desapareció en gran medida.
De cultivos celulares a animales vivos
Los investigadores modificaron células madre para que liberaran exosomas enriquecidos con miR-320d adicional y las compararon con exosomas no modificados. Los exosomas aumentados fueron incorporados con mayor eficiencia por los macrófagos y provocaron descensos más sólidos en los niveles de KLF7, la actividad de STAT3 y la liberación de CCL24. En ratas sometidas a un tratamiento similar a la diálisis, inyecciones semanales de exosomas estándar o ricos en miR-320d redujeron el engrosamiento y la acumulación de colágeno en la membrana peritoneal. Los exosomas potenciados ofrecieron la mayor protección, preservando una apariencia tisular más normal y atenuando los pasos de señalización clave que llevan desde la activación de los macrófagos hasta la transformación de las células del revestimiento y la cicatrización.
Qué podría significar esto para las personas en diálisis
Este trabajo describe una cadena de eventos en la que los macrófagos liberan CCL24, empujando el revestimiento de la diálisis hacia un estado cicatrizado y menos funcional. Los exosomas de células madre peritoneales, especialmente cuando están cargados con miR-320d, rompen esta cadena al silenciar el interruptor de control KLF7–STAT3 que activa CCL24. En términos prácticos, el estudio sugiere que los exosomas derivados de las propias células madre del paciente podrían emplearse en el futuro como una terapia personalizada y sin células para frenar o prevenir el daño de la membrana peritoneal, ayudando a que las personas permanezcan más tiempo en diálisis peritoneal con menos complicaciones.
Cita: Zhao, X., Xi, M., Qi, H. et al. Peritoneal MSCs-derived exosomes suppress CCL24 synthesis through miR-320d delivery contributing to the improvement of peritoneal dialysis-associated fibrosis. Sci Rep 16, 11998 (2026). https://doi.org/10.1038/s41598-026-42489-w
Palabras clave: diálisis peritoneal, fibrosis peritoneal, macrófagos, exosomas, terapia con microARN