Clear Sky Science · nl
Exosomen van peritoneale MSC’s onderdrukken de synthese van CCL24 via levering van miR-320d en dragen bij aan verbetering van peritoneale dialyse-geassocieerde fibrose
Waarom het beschermen van het dialysevlies belangrijk is
Voor mensen bij wie de nieren niet meer werken, biedt peritoneale dialyse de vrijheid om hun bloed thuis te zuiveren met het eigen buikvlies als natuurlijke filter. Maar na jaren kan dit kwetsbare membraan littekenvorming en verdikking ontwikkelen, waardoor patiënten uiteindelijk moeten stoppen met de behandeling. Deze studie onderzoekt waarom dat litteken ontstaat en test een geavanceerde celgebaseerde strategie die gebruikmaakt van kleine biologische pakketjes om schadelijke immuunsignalen te dempen en het membraan gezond te houden.
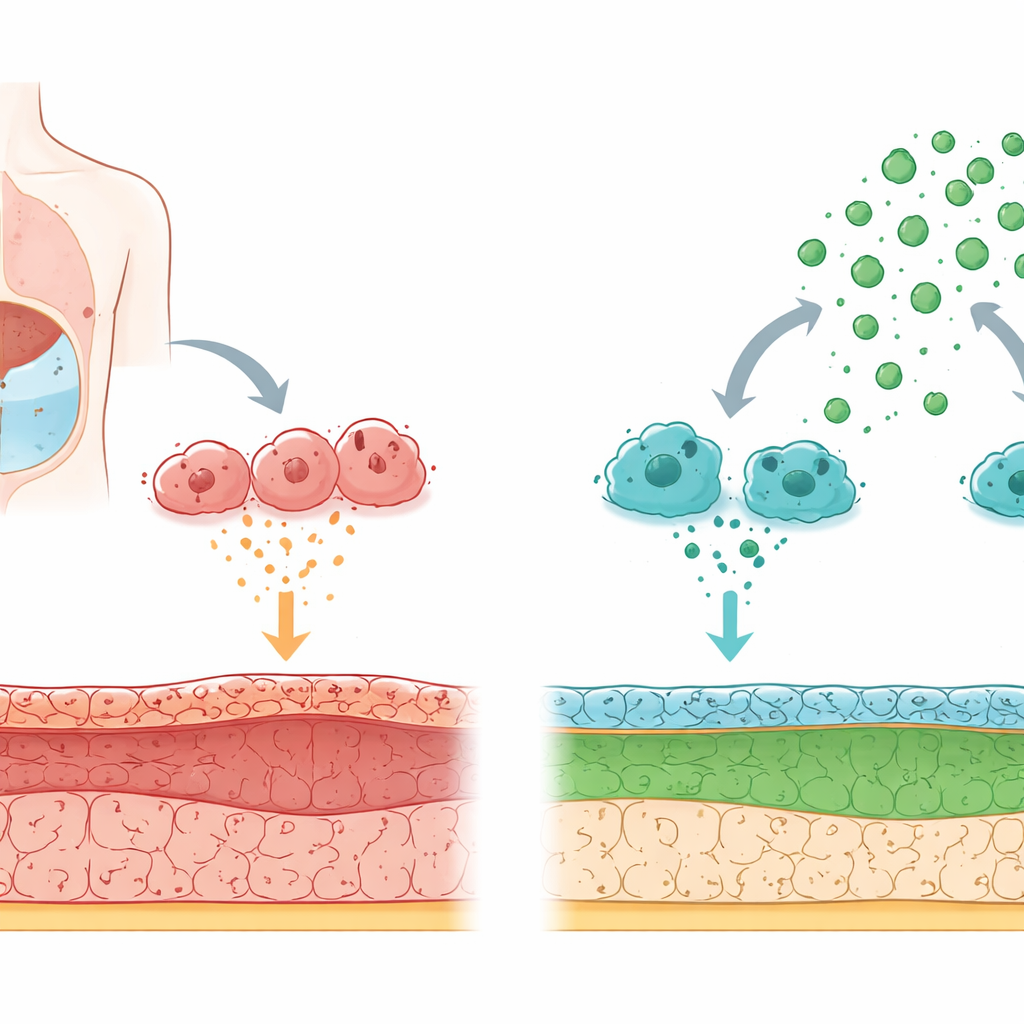
Hoe het lichaamseigen filter na verloop van tijd beschadigt
Peritoneale dialyse werkt door de buik te vullen met een speciale vloeistof zodat afvalstoffen vanuit het bloed over het peritoneale membraan kunnen passeren. Langdurige blootstelling aan hoog-glucose dialysevloeistof en herhaalde ontsteking beschadigen deze bekleding geleidelijk. De cellen die in contact staan met de vloeistof kunnen van karakter veranderen: in plaats van te functioneren als gladde, beschermende tegels, gaan ze zich meer gedragen als littekenvormende cellen die stijve vezels afzetten. Deze verschuiving, een overgang van bekledingscellen naar littekenachtige cellen, veroorzaakt verdikking en functieverlies van het membraan.
Immune boodschappers die cellen naar littekenvorming duwen
De onderzoekers richtten zich op macrofagen, immuuncellen die in de peritoneale holte patrouilleren. In een ratiemodel van dialyse-geïnduceerde schade vonden ze hoge niveaus van een signaalmolecuul genaamd CCL24 voornamelijk in deze macrofagen. Wanneer macrofagen meer CCL24 produceerden, verloren nabijgelegen bekledingscellen hun ordelijke structuur en begonnen ze vezelige eiwitten te maken—een kenmerk van littekenvorming. Het blokkeren van CCL24 in macrofagen, of het blokkeren van de receptor op het oppervlak (bekend als CCR3) of de downstream schakelaar (een route waarin het eiwit p38 betrokken is), voorkwam dat de bekledingscellen veranderden in littekenvormende cellen. Dit plaatste macrofaag-afgeleide CCL24 centraal in het littekenproces.
Stamcelpakketjes die schadelijke signalen dempen
Het team wendde zich vervolgens tot mesenchymale stamcellen die waren verzameld uit het afvalvocht van dialysepatiënten. Deze cellen geven van nature exosomen af—nanometer-grote vesikels die moleculaire boodschappen dragen, zoals kleine RNA’s. Wanneer macrofagen werden blootgesteld aan vocht van deze stamcellen, of aan gezuiverde exosomen, daalde hun productie en afgifte van CCL24 scherp. Hierdoor verminderde de schadelijke invloed van macrofaag-secreties op het peritoneale vlies, en behielden de bekledingscellen meer van hun beschermende eigenschappen. Het verwijderen van exosomen uit het stamcelvocht deed dit voordeel grotendeels verdwijnen, wat aantoont dat deze kleine pakketjes de belangrijkste therapeutische boodschappers zijn.
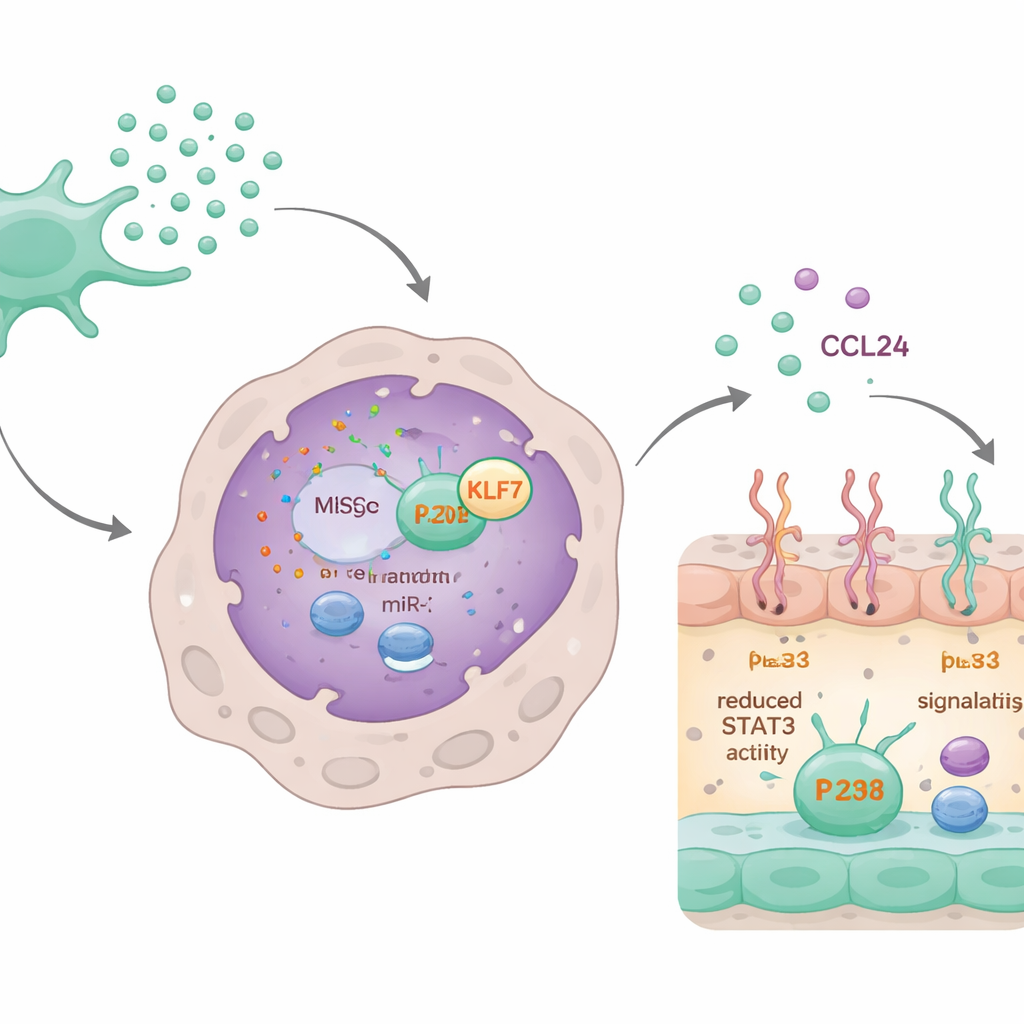
Het microRNA-circuit dat littekenvorming uitschakelt
Dieper gravend ontdekten de wetenschappers dat een specifiek microRNA, miR-320d, ingebed in de exosomen doorslaggevend was. Macrofagen namen exosomen die dit microRNA bevatten gemakkelijk op. Eenmaal binnen bond miR-320d zich aan en verlaagde het de niveaus van een eiwit genaamd KLF7, dat normaal gesproken helpt bij het activeren van een ander eiwit, STAT3. Geactiveerd STAT3 bindt aan het CCL24-gen en verhoogt de productie ervan. Door KLF7 terug te dringen, verminderde miR-320d de activatie van STAT3, wat op zijn beurt de synthese en secretie van CCL24 verlaagde. Wanneer miR-320d werd geblokkeerd of KLF7 kunstmatig werd verhoogd, verdween het kalmerende effect van de exosomen op CCL24 en het gedrag van macrofagen grotendeels.
Van cellulaire kweek naar levende dieren
De onderzoekers ontwierpen stamcellen die exosomen afgeven verrijkt met extra miR-320d en vergeleken deze met ongewijzigde exosomen. De versterkte exosomen werden efficiënter door macrofagen opgenomen en zorgden voor sterkere dalingen in KLF7-niveaus, STAT3-activiteit en CCL24-afgifte. Bij ratten die een dialyse-achtige behandeling ondergingen, verminderden wekelijkse injecties van zowel standaard- als miR-320d-rijke exosomen de verdikking en collageenophoping in het peritoneale membraan. De verbeterde exosomen boden de grootste bescherming, waarbij het weefsel er normaler bleef uitzien en de cruciale signaalstappen die leiden van macrofaagactivatie naar bekledingsceltransformatie en littekenvorming werden gedempt.
Wat dit kan betekenen voor mensen op dialyse
Dit werk schetst een keten van gebeurtenissen waarin macrofagen CCL24 afgeven, waardoor het dialysevlies afglijdt naar een verhard, minder functioneel stadium. Exosomen van peritoneale stamcellen, vooral wanneer ze boordevol miR-320d zitten, doorbreken deze keten door de KLF7–STAT3-schakelaar stil te leggen die CCL24 activeert. In praktische zin suggereert de studie dat de exosomen van iemands eigen stamcellen op den duur als een gepersonaliseerde, celvrije therapie gebruikt zouden kunnen worden om schade aan het peritoneale membraan te vertragen of te voorkomen, zodat mensen langer op peritoneale dialyse kunnen blijven met minder complicaties.
Bronvermelding: Zhao, X., Xi, M., Qi, H. et al. Peritoneal MSCs-derived exosomes suppress CCL24 synthesis through miR-320d delivery contributing to the improvement of peritoneal dialysis-associated fibrosis. Sci Rep 16, 11998 (2026). https://doi.org/10.1038/s41598-026-42489-w
Trefwoorden: peritoneale dialyse, peritoneale fibrose, macrofagen, exosomen, microRNA-therapie