Clear Sky Science · ru
Эксосомы, полученные от мезенхимальных МСК брюшины, подавляют синтез CCL24 посредством доставки miR-320d, способствуя улучшению фиброза, связанного с перитонеальным диализом
Почему важно защищать оболочку для диализа
Для людей с почечной недостаточностью перитонеальный диализ даёт возможность очищать кровь дома, используя собственную брюшную оболочку как естественный фильтр. Но с течением лет эта тонкая мембрана может рубцеваться и утолщаться, в конце концов вынуждая пациентов прекратить лечение. В этом исследовании изучают причины такого рубцевания и испытывают современную клеточную стратегию, использующую крошечные биологические посылки для подавления вредных иммунных сигналов и сохранения здоровья мембраны.
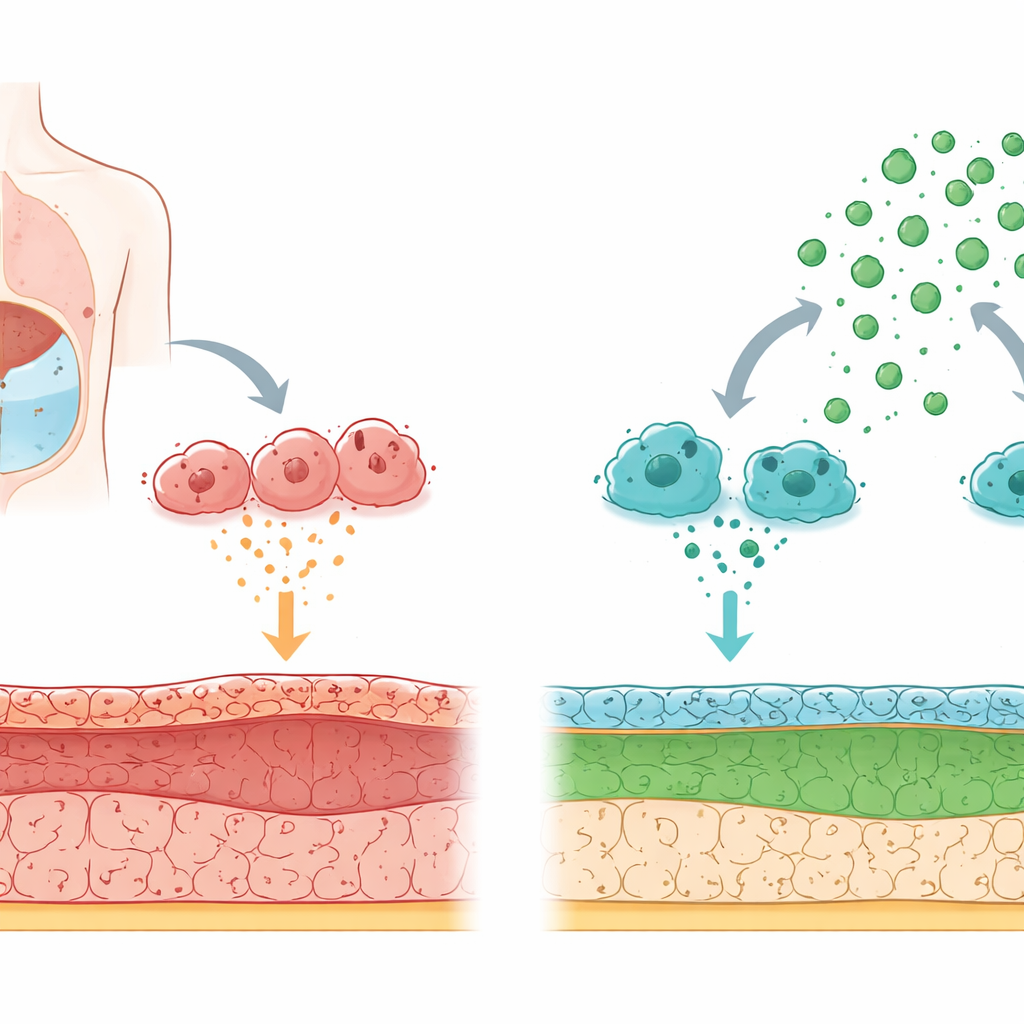
Как со временем повреждается фильтр организма
Перитонеальный диализ осуществляется путём заполнения брюшной полости специальной жидкостью, чтобы отходы могли переходить из крови через перитонеальную мембрану. Длительное воздействие высокоглюкозного диализного раствора и повторяющееся воспаление постепенно повреждают эту оболочку. Клетки, обращённые к жидкости, меняют характер: вместо того чтобы вести себя как гладкие, защитные «плитки», они начинают проявлять свойства клеток, формирующих рубец, и откладывать жёсткие волокна. Это преобразование, называемое переходом от клеток выстилки к рубцоподобным клеткам, приводит к утолщению и потере функции мембраны.
Иммунные посланники, склоняющие клетки к рубцеванию
Исследователи сосредоточились на макрофагах — иммунных клетках, патрулирующих перитонеальную полость. В модельном эксперименте на крысах с повреждением, вызванным диализом, они обнаружили повышенные уровни сигнального белка CCL24 преимущественно в этих макрофагах. Когда макрофаги вырабатывали больше CCL24, соседние клетки выстилки теряли упорядоченную структуру и начинали производить волокнистые белки, что является признаком рубцевания. Блокирование CCL24 в макрофагах или блокировка его рецептора на поверхности (известного как CCR3) либо блокирование нижестоящего сигнального пути (включающего белок p38) препятствовало превращению клеток выстилки в рубцующиеся клетки. Это поместило CCL24, происходящий от макрофагов, в центр процесса рубцевания.
Клеточные посылки, утихающие вредные сигналы
Далее команда обратилась к мезенхимальным стволовым клеткам, выделенным из отработанного диализного раствора пациентов. Эти клетки естественным образом выделяют эксосомы — везикулы нанометрового размера, несущие молекулярные сообщения, такие как малые РНК. Когда макрофаги подвергались воздействию среды от этих стволовых клеток или очищённых эксосом, их производство и выделение CCL24 резко снижалось. В результате вредное влияние секрета макрофагов на перитонеальную выстилку уменьшалось, и клетки выстилки сохраняли больше защитных свойств. Удаление эксосом из среды стволовых клеток в значительной степени лишало этот эффект, что показало: именно эти крошечные посылки являются основными терапевтическими носителями.
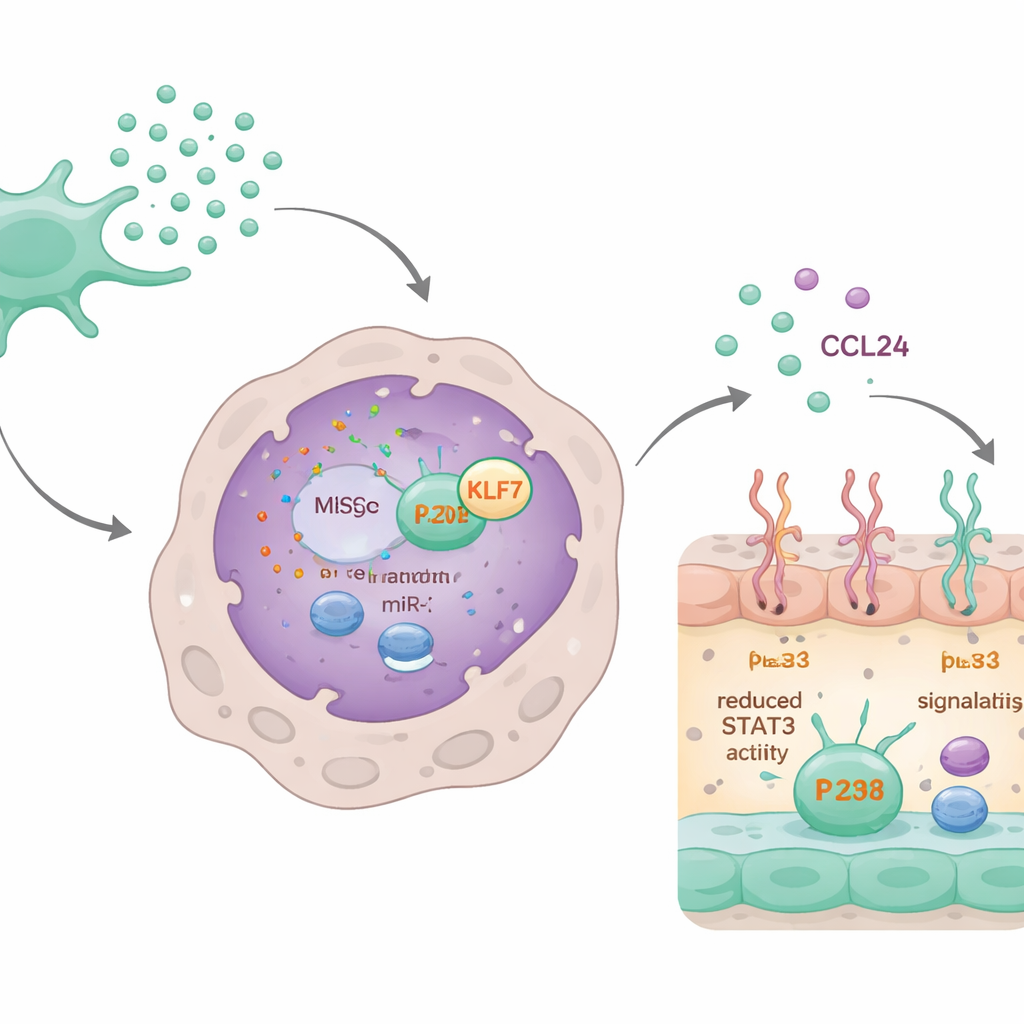
Цепочка микроРНК, которая выключает рубцевание
Углубившись в механизм, учёные обнаружили, что ключевую роль играет конкретная микроРНК — miR-320d, содержащаяся в эксосомах. Макрофаги эффективно поглощали эксосомы, загруженные этой микроРНК. Попав внутрь, miR-320d связывалась с мишенью и снижала уровни белка KLF7, который обычно способствует активации белка STAT3. Активированный STAT3 связывается с геном CCL24 и усиливает его экспрессию. Снижая KLF7, miR-320d уменьшала активацию STAT3, что в свою очередь снижало синтез и секрецию CCL24. При блокировании miR-320d или при искусственном повышении KLF7 успокаивающий эффект экосом на CCL24 и поведение макрофагов в основном исчезал.
От клеточных культур к живым животным
Исследователи модифицировали стволовые клетки так, чтобы они выделяли эксосомы, обогащённые дополнительной miR-320d, и сравнили их с немодифицированными эксосомами. Обогащённые эксосомы поглощались макрофагами более эффективно и вызывали более сильное снижение уровней KLF7, активности STAT3 и выделения CCL24. У крыс, получавших лечение, имитирующее диализ, еженедельные инъекции как стандартных, так и обогащённых miR-320d эксосом уменьшали утолщение и накопление коллагена в перитонеальной мембране. Наибольшую защиту обеспечивали усиленные эксосомы: они сохраняли более нормальный вид ткани и подавляли ключевые сигнальные шаги, ведущие от активации макрофагов к трансформации клеток выстилки и рубцеванию.
Что это может значить для пациентов на диализе
Эта работа описывает цепочку событий, при которой макрофаги выделяют CCL24, проталкивающий выстилку диализной полости к рубцовому, менее функциональному состоянию. Эксосомы от перитонеальных стволовых клеток, особенно загруженные miR-320d, разрывают эту цепь, усиливая молчание контрольного переключателя KLF7–STAT3, который включает CCL24. Говоря простыми словами, исследование указывает на то, что эксосомы, полученные из стволовых клеток самого пациента, в будущем могут быть использованы как персонализированная, безклеточная терапия для замедления или предотвращения повреждения перитонеальной мембраны, помогая людям дольше оставаться на перитонеальном диализе с меньшим числом осложнений.
Цитирование: Zhao, X., Xi, M., Qi, H. et al. Peritoneal MSCs-derived exosomes suppress CCL24 synthesis through miR-320d delivery contributing to the improvement of peritoneal dialysis-associated fibrosis. Sci Rep 16, 11998 (2026). https://doi.org/10.1038/s41598-026-42489-w
Ключевые слова: перитонеальный диализ, перитонеальный фиброз, макрофаги, эксосомы, терапия микроРНК