Clear Sky Science · de
Exosomen aus Peritoneal-MSCs unterdrücken die CCL24-Synthese durch miR-320d-Übertragung und tragen zur Verbesserung der peritonealdialyse‑assoziierten Fibrose bei
Warum es wichtig ist, die Dialyserinnenhaut zu schützen
Für Menschen mit Nierenversagen ermöglicht die Peritonealdialyse die Blutwäsche zu Hause, indem die körpereigene Bauchschleimhaut als natürlicher Filter genutzt wird. Doch im Lauf der Jahre kann diese empfindliche Membran narbig werden und sich verdicken, sodass Patienten die Behandlung schließlich abbrechen müssen. Diese Studie untersucht, warum diese Vernarbung auftritt und prüft eine fortschrittliche zellbasierte Strategie, die winzige biologische Pakete nutzt, um schädliche Immunbotschaften zu dämpfen und die Membran zu erhalten.
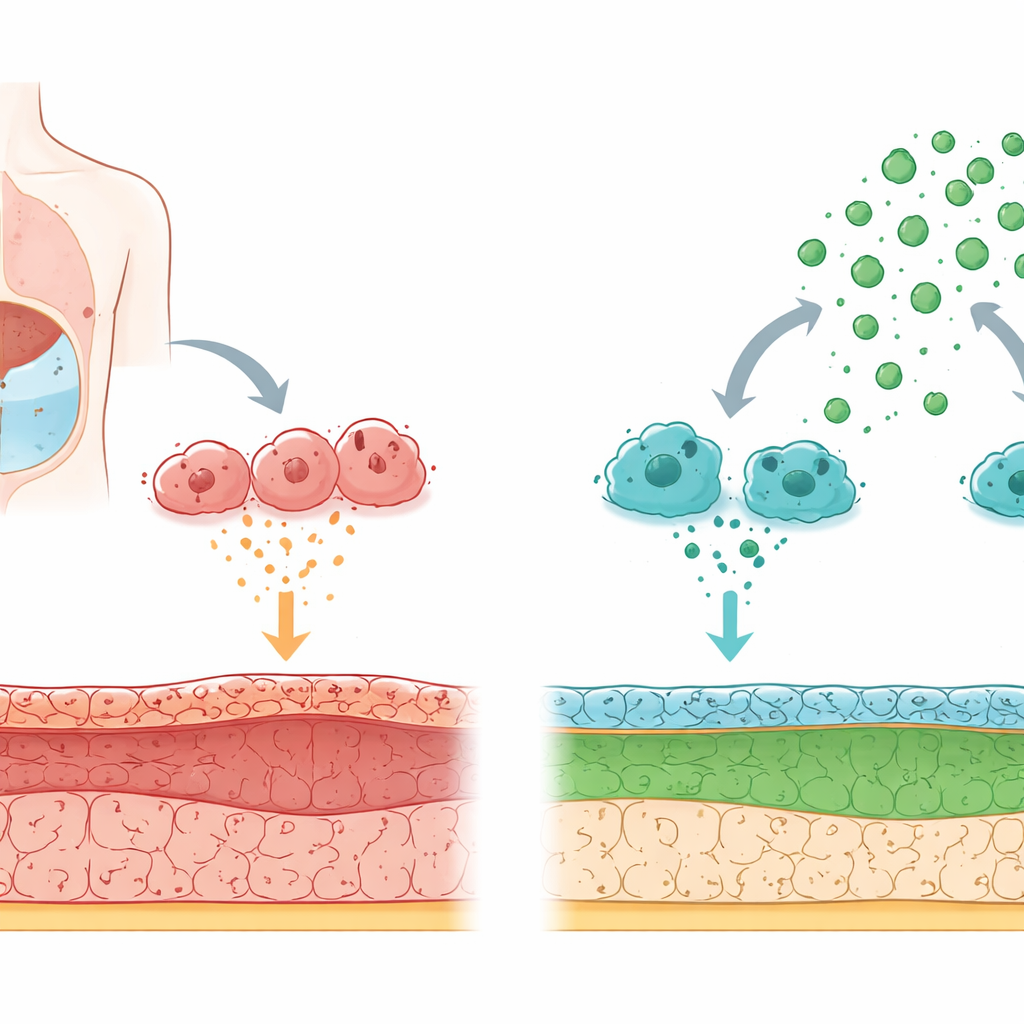
Wie der körpereigene Filter im Laufe der Zeit beschädigt wird
Die Peritonealdialyse funktioniert, indem der Bauch mit einer speziellen Flüssigkeit gefüllt wird, sodass Abfallstoffe aus dem Blut über die Peritonealmembran passieren können. Langfristige Exposition gegenüber hochglukosehaltiger Dialyseflüssigkeit und wiederholte Entzündungen schädigen diese Auskleidung langsam. Die Zellen, die der Flüssigkeit zugewandt sind, können ihren Charakter ändern: Anstatt wie glatte, schützende Flächen zu wirken, beginnen sie sich wie narbenbildende Zellen zu verhalten und legen steife Fasern ab. Dieser Wandel, eine Umwandlung von Auskleidungszellen zu narbenähnlichen Zellen, treibt die Verdickung und den Funktionsverlust der Membran voran.
Immunbotenstoffe, die Zellen zur Vernarbung treiben
Die Forschenden konzentrierten sich auf Makrophagen, Immunzellen, die die Peritonealhöhle überwachen. In einem Rattenmodell für dialysebedingte Schäden fanden sie hohe Konzentrationen eines Signalmoleküls namens CCL24 vor allem in diesen Makrophagen. Wenn Makrophagen mehr CCL24 produzierten, verloren benachbarte Auskleidungszellen ihre geordnete Struktur und begannen, faserige Proteine zu produzieren — ein Kennzeichen der Vernarbung. Das Blockieren von CCL24 in Makrophagen, oder das Blockieren seines Oberflächenempfängers (bekannt als CCR3) oder seines downstream liegenden Schaltkreises (ein Pfad, an dem das Protein p38 beteiligt ist), verhinderte die Umwandlung der Auskleidungszellen in narbenbildende Zellen. Damit rückte das von Makrophagen stammende CCL24 ins Zentrum des Vernarbungsprozesses.
Stammzellpakete, die schädliche Signale dämpfen
Das Team wandte sich dann mesenchymalen Stammzellen zu, die aus dem Abfallflüssigkeitsvolumen von Dialysepatienten gewonnen wurden. Diese Zellen geben natürlicherweise Exosomen ab — vesikelartige Partikel von Nanometergröße, die molekulare Botschaften wie kleine RNAs transportieren. Wurden Makrophagen mit der Flüssigkeit dieser Stammzellen oder mit gereinigten Exosomen exponiert, sank ihre Produktion und Freisetzung von CCL24 stark. Infolgedessen verringerte sich der schädliche Einfluss der Makrophagensekrete auf die Peritonealauskleidung, und die Auskleidungszellen behielten mehr ihrer schützenden Eigenschaften. Das Entfernen der Exosomen aus der Stammzellflüssigkeit hob diesen Nutzen weitgehend auf und zeigte, dass diese winzigen Pakete die wichtigsten therapeutischen Botenstoffe sind.
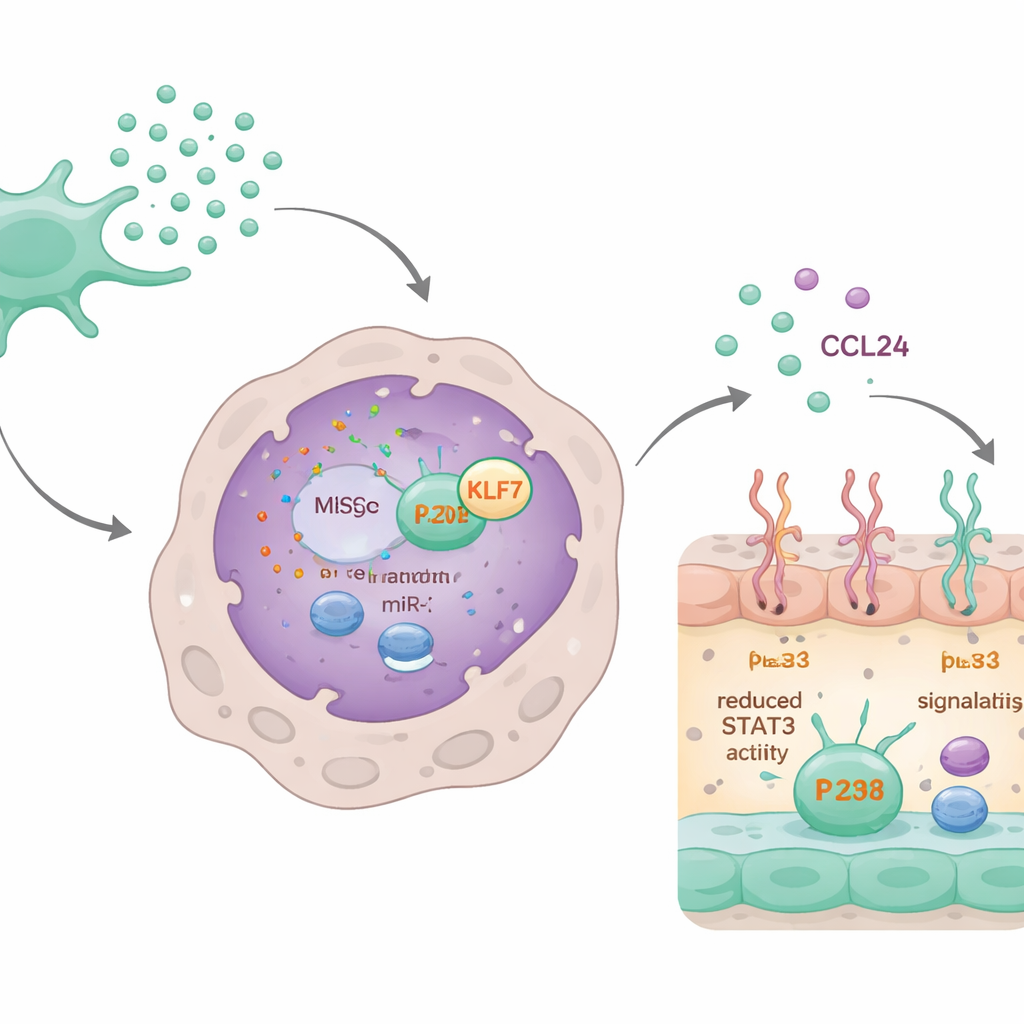
Der microRNA‑Kreislauf, der Vernarbung ausschaltet
Bei genauerer Untersuchung entdeckten die Wissenschaftler, dass eine spezifische microRNA, miR‑320d, die in den Exosomen enthalten ist, entscheidend ist. Makrophagen nahmen Exosomen, die diese microRNA enthielten, bereitwillig auf. Einmal innen, band miR‑320d an ein Protein namens KLF7 und senkte dessen Spiegel; KLF7 trägt normalerweise zur Aktivierung eines weiteren Proteins, STAT3, bei. Aktiviertes STAT3 bindet an das CCL24-Gen und steigert dessen Produktion. Durch die Verminderung von KLF7 reduzierte miR‑320d die Aktivierung von STAT3, was wiederum die Synthese und Sekretion von CCL24 senkte. Wurde miR‑320d blockiert oder KLF7 künstlich erhöht, verschwand der beruhigende Effekt der Exosomen auf CCL24 und das Verhalten der Makrophagen größtenteils.
Von der Zellkultur zum lebenden Organismus
Die Forschenden modifizierten Stammzellen so, dass sie Exosomen mit höherer miR‑320d-Beladung freisetzten, und verglichen diese mit unveränderten Exosomen. Die angereicherten Exosomen wurden von Makrophagen effizienter aufgenommen und bewirkten stärkere Abnahmen von KLF7-Spiegeln, STAT3-Aktivität und CCL24-Freisetzung. Bei Ratten, die einer dialyseähnlichen Behandlung unterzogen wurden, verringerten wöchentliche Injektionen entweder standardisierter oder miR‑320d‑reicher Exosomen die Verdickung und die Kollagenablagerung in der Peritonealmembran. Die verbesserten Exosomen boten den größten Schutz, erhielten ein normaleres Gewebeerscheinungsbild und dämpften die Schlüsselreaktionsschritte, die von der Makrophagenaktivierung zur Umwandlung der Auskleidungszellen und zur Vernarbung führen.
Was das für Peritonealdialyse-Patienten bedeuten könnte
Diese Arbeit beschreibt eine Ereigniskette, in der Makrophagen CCL24 freisetzen und die Dialysemembran in einen vernarbten, weniger funktionalen Zustand treiben. Exosomen aus peritonealen Stammzellen — insbesondere wenn sie mit miR‑320d beladen sind — durchtrennen diese Kette, indem sie den KLF7–STAT3‑Schalthebel stummschalten, der CCL24 einschaltet. Praktisch gesprochen deutet die Studie darauf hin, dass die aus den eigenen Stammzellen eines Patienten gewonnenen Exosomen eines Tages als personalisierte, zellfreie Therapie eingesetzt werden könnten, um Schäden an der Peritonealmembran zu verlangsamen oder zu verhindern und so Patienten zu helfen, länger und mit weniger Komplikationen an der Peritonealdialyse festzuhalten.
Zitation: Zhao, X., Xi, M., Qi, H. et al. Peritoneal MSCs-derived exosomes suppress CCL24 synthesis through miR-320d delivery contributing to the improvement of peritoneal dialysis-associated fibrosis. Sci Rep 16, 11998 (2026). https://doi.org/10.1038/s41598-026-42489-w
Schlüsselwörter: Peritonealdialyse, peritoneale Fibrose, Makrophagen, Exosomen, microRNA-Therapie