Clear Sky Science · pt
Exossomos derivados de CMs peritoneais suprimem a síntese de CCL24 através da entrega de miR-320d, contribuindo para a melhora da fibrose associada à diálise peritoneal
Por que proteger o revestimento da diálise é importante
Para pessoas com insuficiência renal, a diálise peritoneal oferece a liberdade de limpar o sangue em casa usando o próprio revestimento abdominal do corpo como um filtro natural. Mas, ao longo dos anos, essa membrana delicada pode cicatrizar e espessar, forçando eventualmente os pacientes a abandonar o tratamento. Este estudo investiga por que essa cicatrização ocorre e testa uma estratégia celular de ponta que usa pequenos pacotes biológicos para acalmar sinais imunes prejudiciais e ajudar a manter a membrana saudável.
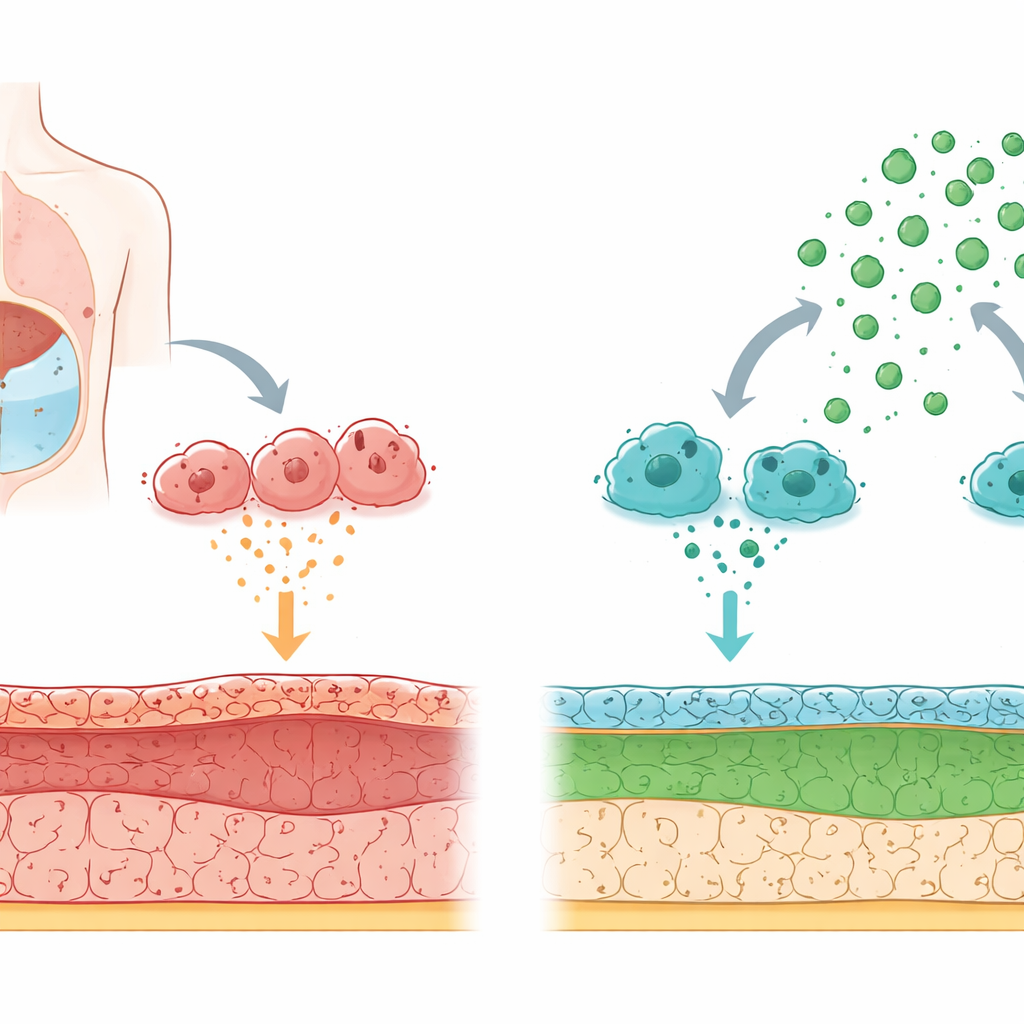
Como o filtro do corpo se danifica com o tempo
A diálise peritoneal funciona preenchendo o abdome com um fluido especial para que os resíduos possam passar do sangue através da membrana peritoneal. A exposição prolongada a fluido de diálise com alto teor de glicose e a inflamação repetida lesionam lentamente esse revestimento. As células voltadas para o fluido podem mudar de caráter: em vez de se comportarem como camadas suaves e protetoras, passam a agir mais como células formadoras de cicatriz que depositam fibras rígidas. Essa mudança, chamada de transição de células do revestimento para células semelhantes a cicatriz, impulsiona o espessamento e a perda de função da membrana.
Mensageiros imunes que empurram as células para a cicatrização
Os pesquisadores concentraram-se nos macrófagos, células do sistema imune que patrulham a cavidade peritoneal. Em um modelo de rato com lesão induzida por diálise, eles encontraram altos níveis de uma proteína sinalizadora chamada CCL24 principalmente nesses macrófagos. Quando os macrófagos produziam mais CCL24, as células do revestimento próximas perdiam sua estrutura ordenada e começavam a produzir proteínas fibrilares, um sinal característico de cicatrização. Bloquear a CCL24 nos macrófagos, ou bloquear seu receptor de superfície (conhecido como CCR3) ou seu interruptor químico a jusante (uma via envolvendo a proteína p38), impediu que as células do revestimento se transformassem em células formadoras de cicatriz. Isso colocou a CCL24 derivada de macrófagos no centro do processo de cicatrização.
Pacotes de células-tronco que silenciam sinais nocivos
A equipe então voltou-se para células-tronco mesenquimais coletadas do fluido residual de pacientes em diálise. Essas células liberam naturalmente exossomos — vesículas em escala nanométrica que transportam mensagens moleculares, como pequenos RNAs. Quando macrófagos foram expostos ao fluido dessas células-tronco, ou a exossomos purificados, a produção e liberação de CCL24 caiu drasticamente. Como resultado, a influência danosa das secreções dos macrófagos sobre o revestimento peritoneal foi reduzida, e as células do revestimento mantiveram mais de suas características protetoras. Remover os exossomos do fluido das células-tronco apagou em grande parte esse benefício, mostrando que esses pequenos pacotes são os principais mensageiros terapêuticos.
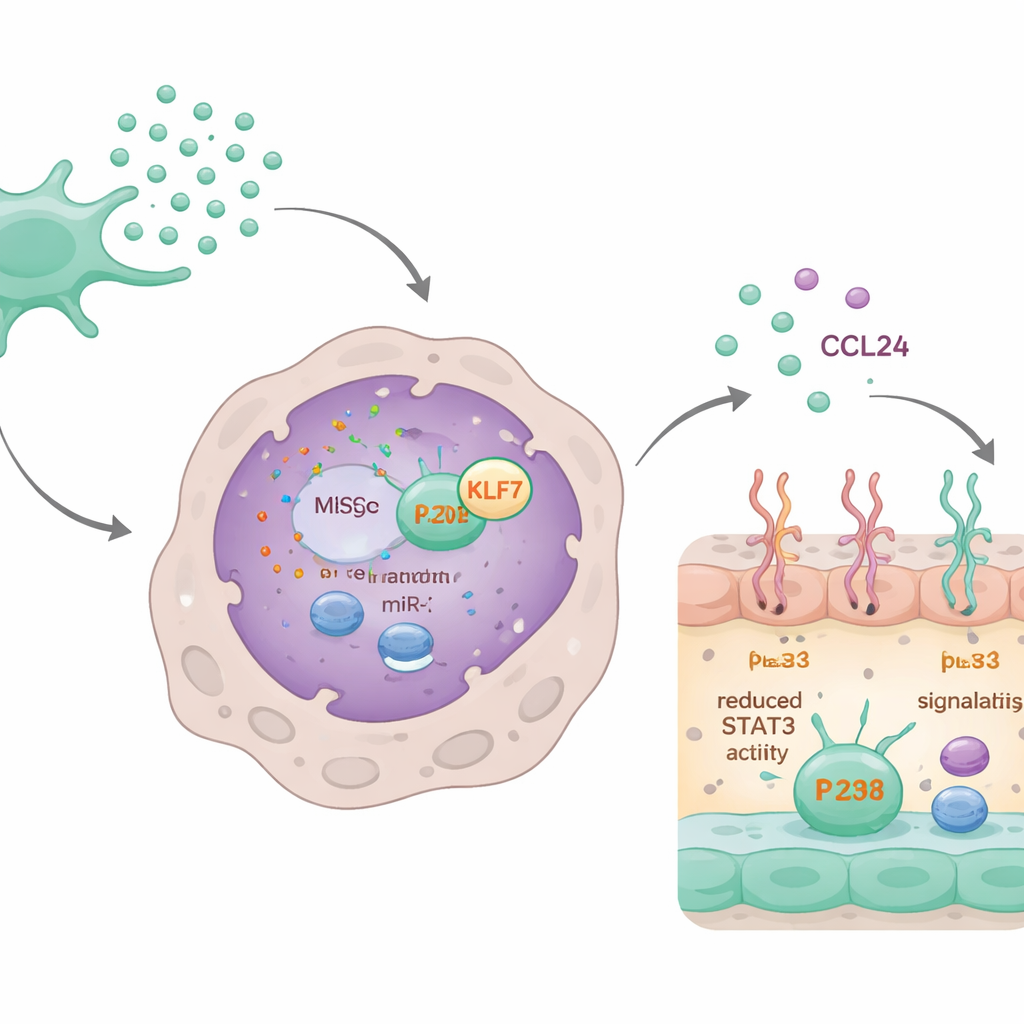
O circuito do microRNA que desliga a cicatrização
Aprofundando a investigação, os cientistas descobriram que um microRNA específico, miR-320d, transportado dentro dos exossomos, era fundamental. Os macrófagos incorporaram facilmente exossomos carregados com esse microRNA. Uma vez no interior, o miR-320d ligou-se e reduziu os níveis de uma proteína chamada KLF7, que normalmente ajuda a ativar outra proteína, STAT3. A STAT3 ativada liga-se ao gene CCL24 e aumenta sua produção. Ao reduzir o KLF7, o miR-320d diminuiu a ativação da STAT3, o que por sua vez reduziu a síntese e a secreção de CCL24. Quando o miR-320d foi bloqueado ou o KLF7 foi artificialmente aumentado, o efeito calmante dos exossomos sobre a CCL24 e o comportamento dos macrófagos desapareceu em grande parte.
Da cultura celular aos animais vivos
Os pesquisadores modificaram geneticamente células-tronco para liberar exossomos enriquecidos com miR-320d extra e os compararam com exossomos não modificados. Os exossomos enriquecidos foram captados com mais eficiência pelos macrófagos e produziram quedas mais fortes nos níveis de KLF7, na atividade da STAT3 e na liberação de CCL24. Em ratos submetidos a tratamento semelhante à diálise, injeções semanais de exossomos padrão ou enriquecidos com miR-320d reduziram o espessamento e o acúmulo de colágeno na membrana peritoneal. Os exossomos aprimorados forneceram a maior proteção, preservando a aparência mais próxima do tecido normal e atenuando os passos-chave de sinalização que levam da ativação dos macrófagos à transformação das células do revestimento e à cicatrização.
O que isso pode significar para pessoas em diálise
Este trabalho descreve uma cadeia de eventos em que macrófagos liberam CCL24, conduzindo o revestimento da diálise para um estado cicatrizado e menos funcional. Exossomos de células-tronco peritoneais, especialmente quando carregados com miR-320d, interrompem essa cadeia ao silenciar o interruptor de controle KLF7–STAT3 que liga a CCL24. Em termos práticos, o estudo sugere que os exossomos derivados das próprias células-tronco do paciente poderiam um dia ser usados como uma terapia personalizada e sem células para desacelerar ou prevenir danos à membrana peritoneal, ajudando as pessoas a permanecer mais tempo na diálise peritoneal com menos complicações.
Citação: Zhao, X., Xi, M., Qi, H. et al. Peritoneal MSCs-derived exosomes suppress CCL24 synthesis through miR-320d delivery contributing to the improvement of peritoneal dialysis-associated fibrosis. Sci Rep 16, 11998 (2026). https://doi.org/10.1038/s41598-026-42489-w
Palavras-chave: diálise peritoneal, fibrose peritoneal, macrófagos, exossomos, terapia com microRNA