Clear Sky Science · zh
乙酰化对衰老 htau 小鼠 tau 病理的性别特异性影响
这项脑研究为何重要
阿尔茨海默病影响数百万个家庭,女性的确诊率高于男性。本研究提出了一个简单却有力的问题:衰老的雌性大脑是否以不同于雄性大脑的方式处理一种与阿尔茨海默相关的关键蛋白?研究者使用携带该人源蛋白的小鼠模型,重点考察可使该蛋白更易聚集且更难清除的细微化学修饰。研究结果指向一种性别特异的脆弱性,可能有助于解释为何女性在阿尔茨海默及相关疾病中往往表现出更严重的大脑病变。
显微镜下的黏性脑蛋白
这项研究的核心是 tau,一种通常帮助稳定神经元内部“轨道”的蛋白,这些轨道用于运输营养和信号。在许多脑病中,tau 表现异常,在神经元内以小而有毒的聚集体形式堆积,随后形成更大的缠结。科学家早已知道向 tau 添加磷酸基(磷酸化)会促进这种聚集。本研究聚焦于另一类化学标记——乙酰化,定位于称为赖氨酸 174 的特定位点。早期研究表明,这种乙酰化标记在疾病早期出现,并能减慢 tau 从脑中被清除的速度。作者旨在探究在仅表达人人源 tau 的雌雄小鼠中,随着年龄增长该标记及相关蛋白清除系统如何变化。
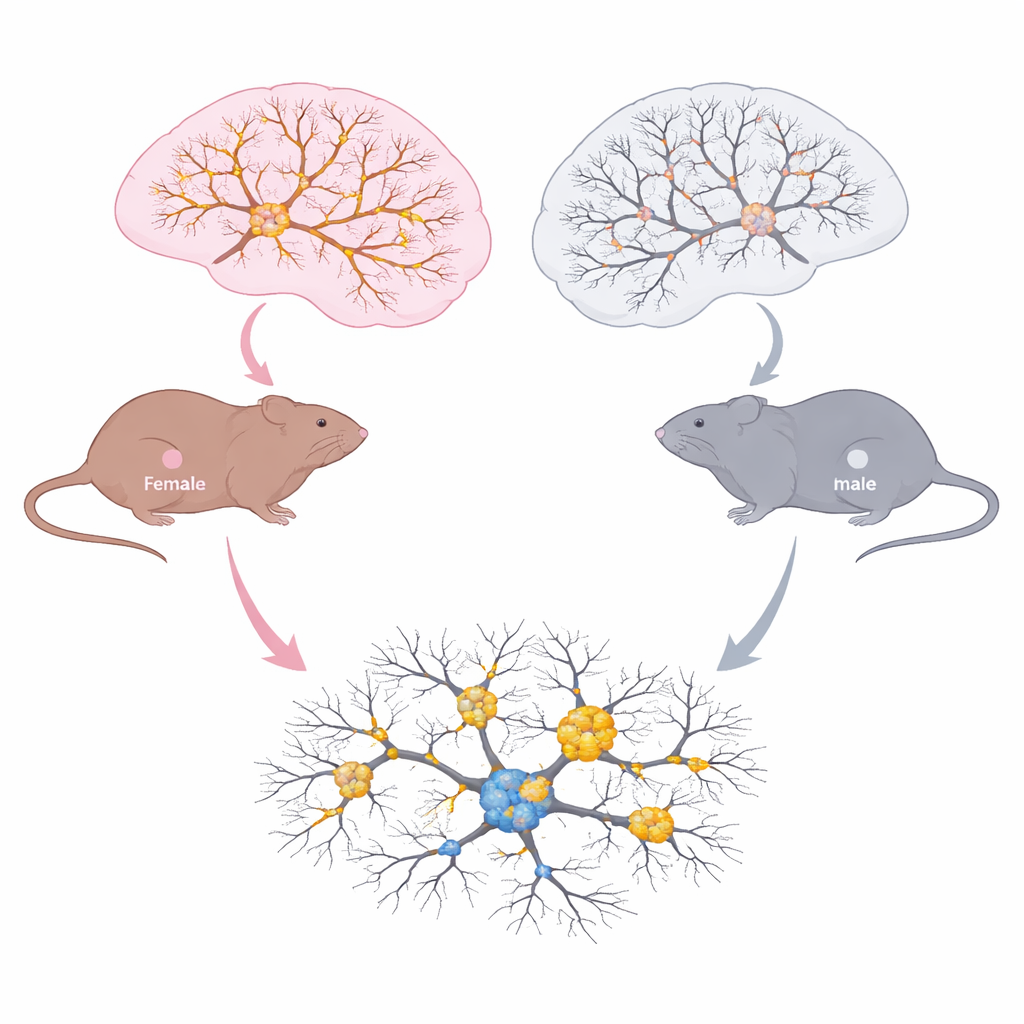
雄性与雌性大脑不同的衰老轨迹
研究团队在三个生命阶段(年轻成体、中年和出现症状的老年)检查了与记忆和决策相关的重要脑区。在海马和前额皮层,他们测量了总 tau、磷酸化 tau、赖氨酸 174 处的乙酰化 tau 以及称为寡聚体的小型 tau 聚集体。两性随年龄均出现更多的 tau 寡聚体,表明 tau 病理加重。但化学变化的模式明显不同。雌性中,总 tau 和在赖氨酸 174 带有乙酰标记的 tau 随年龄增加,这一增加与日益增多的 tau 负担相一致。雄性则表现为随年龄增加的 tau 磷酸化,但赖氨酸 174 的乙酰化未见同样上升。显微成像显示,老年雌鼠在关键海马区有更多扩散的乙酰化 tau,以及乙酰化与磷酸化 tau 的更大重叠,并伴有小胶质细胞(大脑免疫细胞)活化增强。
当大脑的清理队伍跟不上时
为了解为何 tau 在性别间出现不同的堆积,研究人员调查了大脑的蛋白质维护系统。他们考察了添加乙酰基的酶(尤指一对称为 CBP/p300 的乙酰转移酶)、去除乙酰基的酶(sirtuins)以及提供乙酰“燃料”乙酰辅酶 A 的酶。在雌性中,CBP/p300 水平随年龄上升,与乙酰化 tau 的增加相吻合,而产生乙酰辅酶 A 的酶和脱乙酰的 sirtuins 变化不大。这提示在雌性中,是乙酰转移酶活性过高,而非乙酰基燃料或去除机制,推动了更高的 tau 乙酰化。团队还检查了自噬——细胞吞噬并消化不需要的蛋白和结构的回收通路。随年龄增长,若干自噬标志物以复杂且性别依赖的方式发生变化。雌性显示出回收囊泡形成和通量减少的迹象,这些囊泡有助于清除 tau;而雄性则表现出不同模式,包括货物适配蛋白的堆积和对相关清除通路的更大依赖。
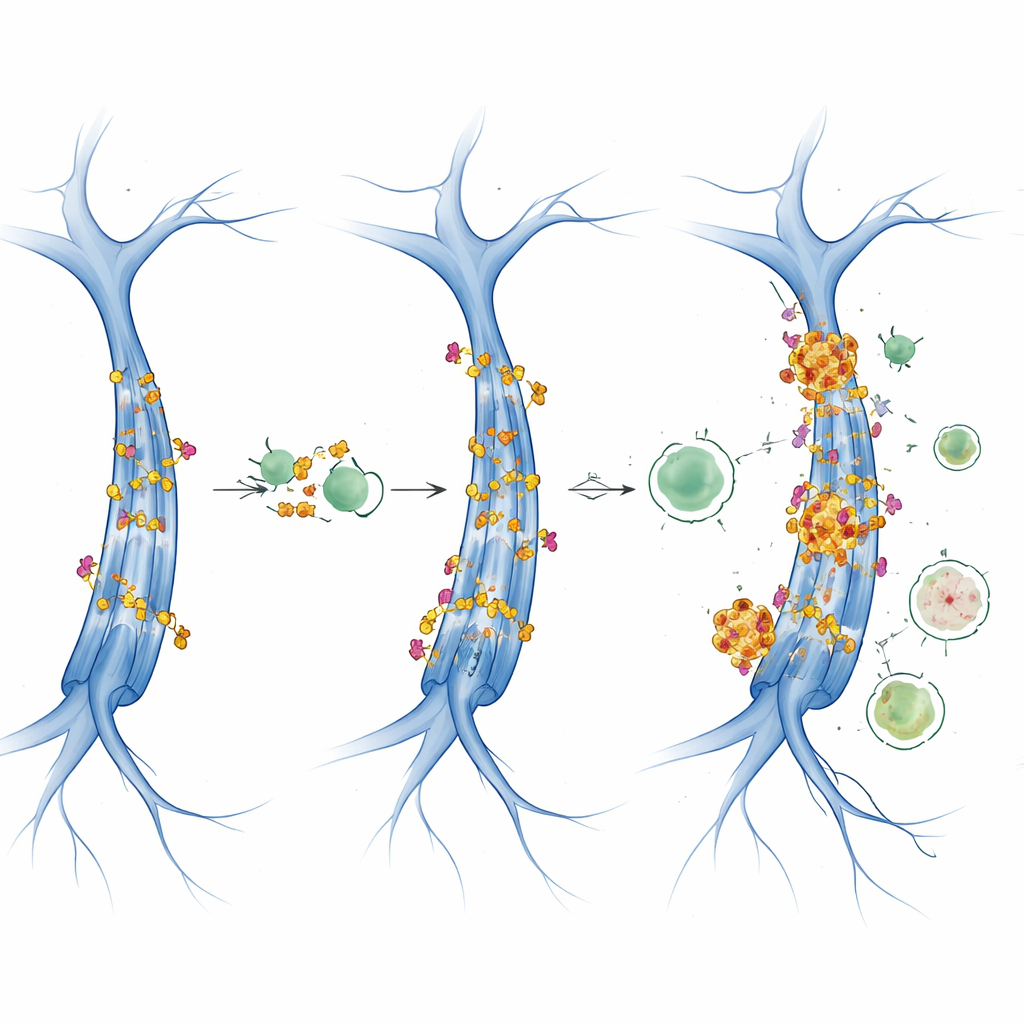
减缓细胞回收的信号
研究进一步探讨了细胞生长与能量利用的两大主控因子:mTOR 和 AMPK。当 mTOR 高度活跃时,它倾向于抑制自噬,而 AMPK 在能量压力下则促进自噬。在这些 tau 小鼠中,AMPK 活性随年龄和性别大体稳定,但与 mTOR 相关的信号以年龄和性别特异的方式发生改变。数据指向 mTOR 驱动的自噬抑制与乙酰化机制相交汇。在雌性中,上升的 CBP/p300 与乙酰化 tau 与被损害的自噬通量标志物同时出现,提示一种正反馈回路:更多的乙酰化 tau 被产生,同时本应清除它的系统效率下降,允许有毒的 tau 聚集体积累。
这对理解与治疗疾病意味着什么
对非专业读者而言,关键结论是雄性与雌性大脑在衰老过程中并不会以同样方式处理相同的致病蛋白。在这个人源化 tau 小鼠模型中,雌性尤其容易在 tau 上添加乙酰标签,这由特定酶活性增高驱动,并伴随细胞回收功能的衰退。相比之下,雄性更多表现出磷酸化方面的变化以及蛋白质清除途径的不同调整。尽管该研究在小鼠中进行且样本量相对有限,但它支持这样一种观点:乙酰化是 tau 堆积中的一个关键且受性别影响的步骤。这使得与乙酰化相关的酶和自噬调控因子成为有吸引力的治疗靶点,可用于基于生物性别定制的干预,最终目标是减缓或预防由 tau 驱动的大脑功能衰退。
引用: Sabir, U., Csubak, B.A., Ilchenko, S. et al. Sex-specific effects of acetylation on tauopathy in aging htau mice. Sci Rep 16, 11862 (2026). https://doi.org/10.1038/s41598-026-41691-0
关键词: tau 乙酰化, 性别差异, 自噬, 阿尔茨海默病, 神经退行性变