Clear Sky Science · sv
Könsspecifika effekter av acetylering på tauopati i åldrande htau-möss
Varför denna hjärnstudie är viktig
Alzheimers sjukdom berör miljontals familjer, och kvinnor diagnostiseras oftare än män. Denna studie ställer en enkel men kraftfull fråga: hanterar den åldrande kvinnliga hjärnan ett nyckelprotein relaterat till Alzheimer annorlunda än den manliga hjärnan? Genom att använda en musmodell som bär mänskliga versioner av detta protein fokuserar forskarna på subtila kemiska markörer som kan göra proteinet mer benäget att klumpa ihop sig och svårare att rensa bort. Deras resultat pekar på en könsspecifik sårbarhet som kan bidra till att förklara varför kvinnor tenderar att uppvisa mer uttalade hjärnförändringar vid Alzheimer och närliggande sjukdomar.
Ett klibbigt hjärnprotein under lupp
I centrum för detta arbete står tau, ett protein som normalt hjälper till att stabilisera neuroners inre “spår” som används för att transportera näring och signaler. I många hjärnsjukdomar beter sig tau illa, hopar sig inne i neuroner som små giftiga kluster och senare som större trassel. Forskare visste redan att tillsats av fosfatgrupper på tau (fosforylering) uppmuntrar denna klumpning. Denna studie koncentrerar sig på en annan sorts kemisk markering, acetylering, som placeras på en specifik plats på tau kallad lysin 174. Tidigare forskning föreslog att denna acetylmarkör dyker upp tidigt i sjukdomen och kan bromsa taus borttagning från hjärnan. Författarna undersökte hur denna markering, och relaterade proteinrensningssystem, förändras med åldern hos han- respektive honmöss som uttrycker enbart mänsklig tau.
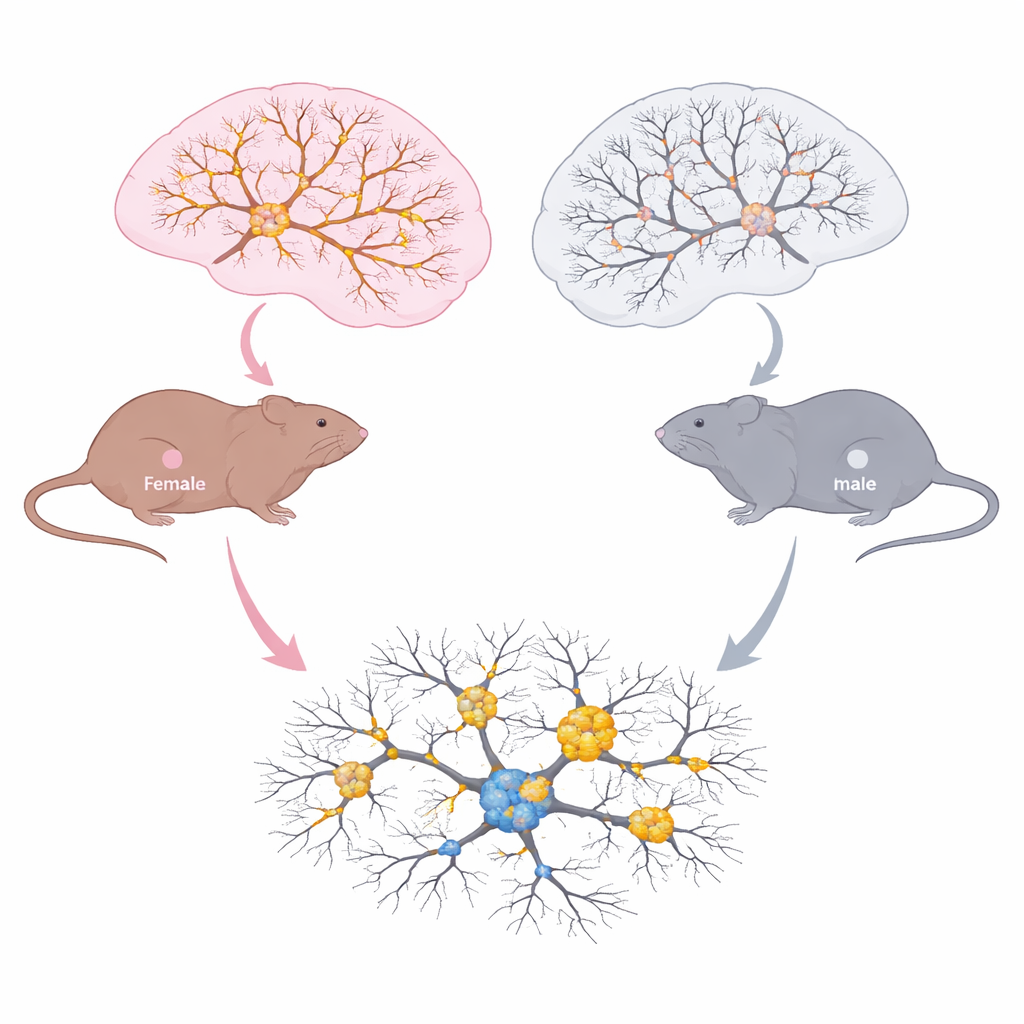
Hur manliga och kvinnliga hjärnor åldras olika
Teamet undersökte hjärnområden som är viktiga för minne och beslutsfattande i tre livsstadier: unga vuxna, medelålders och äldre symtomatiska djur. I hippocampus och prefrontala cortex mätte de total tau, fosforylerad tau, acetylerad tau vid lysin 174 och små taukluster kända som oligomerer. Båda könen samlade på sig fler tau-oligomerer med åldern, ett tecken på förvärrad tauopati. Men mönstret av kemiska förändringar skilde sig markant. Hos honor ökade total tau och tau med acetylmärket vid lysin 174 med åldern, och denna ökning följde den ökande taubördan. Hos hanar ökade taufosforylering med åldern, men acetylering vid lysin 174 gjorde det inte. Mikroskopi visade att åldrade honor hade mer acetylerad tau utspridd i viktiga hippocampuszoner och större överlappning mellan acetylerad och fosforylerad tau, tillsammans med ökad aktivering av mikroglia, hjärnans immunceller.
När hjärnans städbesättning halkar efter
För att förstå varför tau ackumulerades olika mellan könen undersökte forskarna hjärnans system för proteinunderhåll. De tittade på enzymer som lägger till acetylmärken (särskilt paret CBP/p300), enzymer som tar bort dem (sirtuiner) och enzymer som levererar acetyl-“bränslet” acetyl-CoA. Hos honor steg CBP/p300-nivåerna med åldern, i takt med ökningen av acetylerad tau, medan acetyl-CoA–producerande enzymer och deacetylerande sirtuiner förändrades lite. Detta tyder på att överaktiva acetyltransferaser, snarare än bränslelevernans eller borttagning, driver högre tau-acetylering hos honor. Teamet undersökte också autofagi, cellens återvinningsväg som omsluter och bryter ner oönskade proteiner och strukturer. Med åldern skiftade flera autofagimarkörer på komplexa, könsberoende sätt. Honor visade tecken på minskad bildning och flöde av de återvinningsvesiklar som hjälper till att rensa tau, medan hanar visade andra mönster, inklusive ansamling av en lastadapterprotein och ökat beroende av en relaterad städrutt.
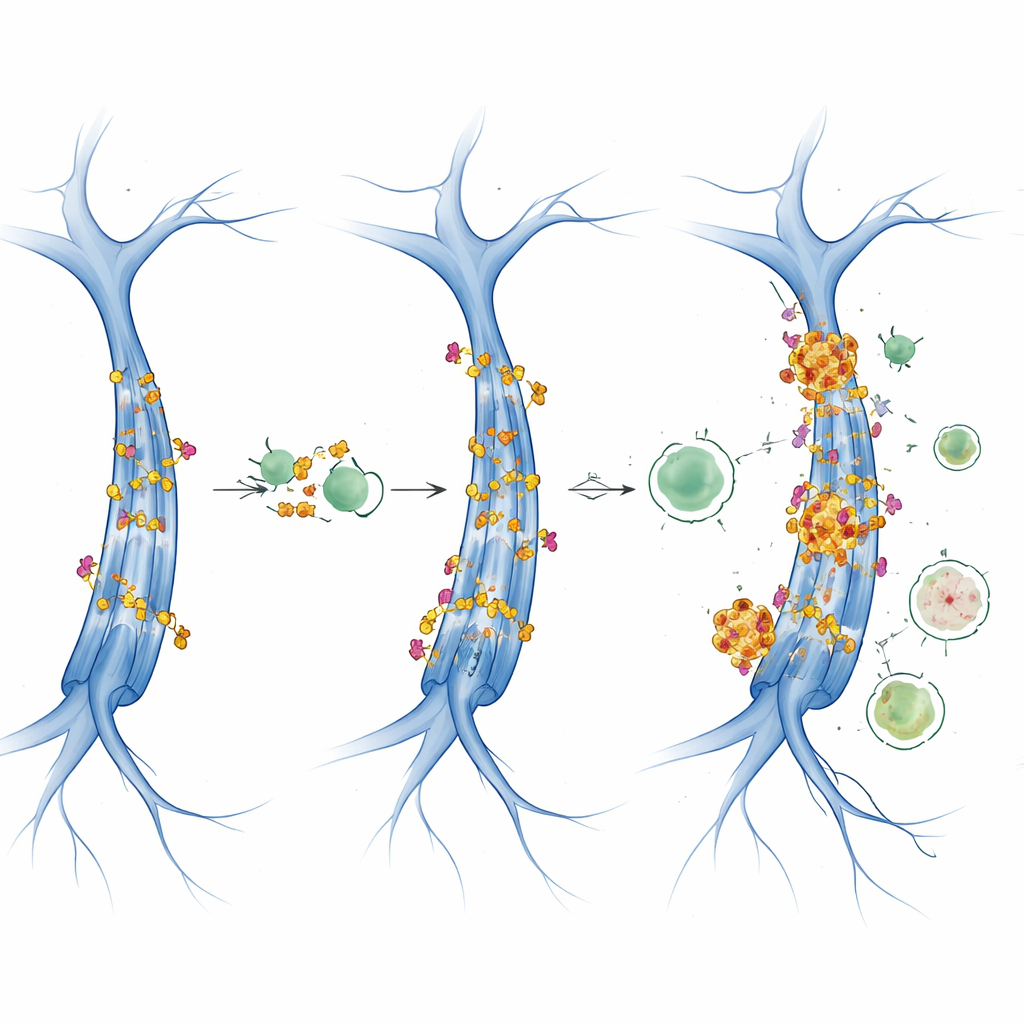
Signaler som bromsar cellernas återvinning
Studien utforskade vidare två huvudregulatorer av celltillväxt och energianvändning: mTOR och AMPK. När mTOR är mycket aktiv tenderar det att stänga av autofagi, medan AMPK främjar den vid energistress. I dessa taumus såg AMPK-aktiviteten i stort sett stabil ut över ålder och kön, men mTOR-relaterade signaler förändrades på ett ålders- och könsspecifikt sätt. Data pekar mot mTOR-driven hämning av autofagi, som korsar med acetyleringsmaskineriet. Hos honor sammanföll stigande CBP/p300 och acetylerad tau med markörer för försämrat autofagiskt flöde, vilket tyder på en självförstärkande loop: mer acetylerad tau produceras, samtidigt som systemet som borde avlägsna den blir mindre effektivt, vilket tillåter att giftiga taukluster ackumuleras.
Vad detta betyder för förståelse och behandling
För icke-specialister är huvudbudskapet att manliga och kvinnliga hjärnor inte hanterar samma sjukdomsprotein på samma sätt när de åldras. I denna humaniserade tau-musmodell är honor särskilt benägna att lägga till en acetylmärkning på tau, drivet av högre aktivitet hos specifika enzymer och åtföljt av sviktande cellulär återvinning. Hanar visar däremot fler förändringar i fosforylering och andra förändringar i proteinrensningsvägar. Även om arbetet är utfört i möss och med relativt små grupper stöder det idén att acetylering är ett kritiskt, könssensitivt steg i tauuppbyggnad. Det gör enzymer relaterade till acetylering och regulatorer av autofagi till attraktiva mål för behandlingar anpassade efter biologiskt kön, med det långsiktiga målet att sakta ner eller förebygga taudriven hjärnförsämring.
Citering: Sabir, U., Csubak, B.A., Ilchenko, S. et al. Sex-specific effects of acetylation on tauopathy in aging htau mice. Sci Rep 16, 11862 (2026). https://doi.org/10.1038/s41598-026-41691-0
Nyckelord: tau-acetylering, könsskillnader, autofagi, Alzheimers sjukdom, neurodegeneration