Clear Sky Science · de
Geschlechtsspezifische Effekte der Acetylierung auf Tauopathie bei alternden htau-Mäusen
Warum diese Gehirnstudie wichtig ist
Die Alzheimer-Krankheit betrifft Millionen von Familien, und Frauen erhalten häufiger die Diagnose als Männer. Diese Studie stellt eine einfache, aber kraftvolle Frage: Geht das alternde weibliche Gehirn mit einem für Alzheimer relevanten Protein anders um als das männliche Gehirn? An einem Mausmodell, das menschliche Versionen dieses Proteins trägt, untersuchen die Forschenden subtile chemische Markierungen, die das Protein anfälliger fürs Verklumpen und schwerer abbaubar machen können. Ihre Ergebnisse deuten auf eine geschlechtsspezifische Verwundbarkeit hin, die helfen könnte zu erklären, warum bei Frauen bei Alzheimer und verwandten Erkrankungen oft schwerere Hirnveränderungen beobachtet werden.
Ein klebriges Hirnprotein unter dem Mikroskop
Im Mittelpunkt dieser Arbeit steht Tau, ein Protein, das normalerweise die inneren "Gleise" von Neuronen stabilisiert, über die Nährstoffe und Signale transportiert werden. In vielen Hirnkrankheiten gerät Tau außer Kontrolle, sammelt sich in Neuronen als kleine toxische Aggregate und später als größere Verwicklungen. Bekannt ist bereits, dass das Hinzufügen von Phosphatgruppen zu Tau (Phosphorylierung) dieses Verklumpen fördert. Die Studie konzentriert sich auf eine andere chemische Markierung, die Acetylierung, an einer bestimmten Stelle von Tau, dem Lysin 174. Frühere Untersuchungen deuteten darauf hin, dass dieses Acetylzeichen früh in der Erkrankung auftritt und den Abbau von Tau verlangsamen kann. Die Autorinnen und Autoren wollten untersuchen, wie dieses Zeichen und die damit verbundenen Proteinräumungssysteme mit dem Alter bei männlichen und weiblichen Mäusen, die nur menschliches Tau exprimieren, verändert werden.
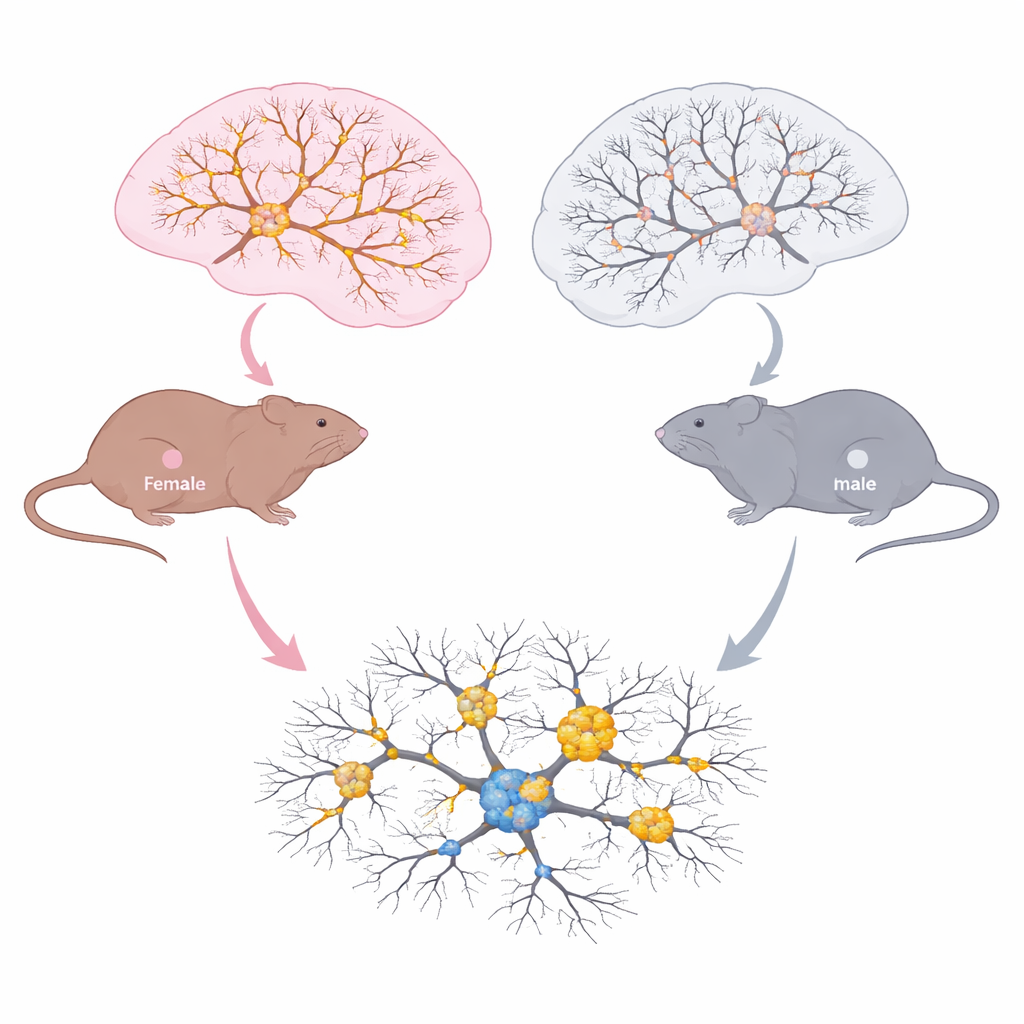
Wie männliche und weibliche Gehirne unterschiedlich altern
Das Team untersuchte Hirnregionen, die für Gedächtnis und Entscheidungsfindung wichtig sind, in drei Lebensphasen: junge Erwachsene, mittleres Alter und ältere, symptomatische Tiere. Im Hippocampus und im präfrontalen Kortex maßen sie Gesamt-Tau, phosphoryliertes Tau, acetyliertes Tau an Lysin 174 und kleine Tau-Aggregate, sogenannte Oligomere. Beide Geschlechter zeigten im Alter eine Zunahme von Tau-Oligomeren, ein Zeichen sich verschlechternder Tauopathie. Das Muster der chemischen Veränderungen unterschied sich jedoch deutlich. Bei weiblichen Tieren stiegen Gesamt-Tau und Tau mit der Acetylierung an Lysin 174 mit dem Alter, und dieser Anstieg korrelierte mit zunehmender Tau-Belastung. Bei männlichen Tieren nahm die Phosphorylierung von Tau mit dem Alter zu, doch die Acetylierung an Lysin 174 tat dies nicht. Die Mikroskopie zeigte, dass ältere Weibchen mehr acetyliertes Tau in wichtigen Hippocampus-Zonen aufwiesen und eine stärkere Überlappung von acetyliertem und phosphoryliertem Tau, zusammen mit erhöhter Aktivierung von Mikroglia, den Immunzellen des Gehirns.
Wenn die Reinigungsmannschaften des Gehirns hinterherhinken
Um zu verstehen, warum sich Tau geschlechtsspezifisch unterschiedlich ansammelte, untersuchten die Forschenden die proteinpflegenden Systeme des Gehirns. Sie betrachteten Enzyme, die Acetylgruppen anbringen (insbesondere das Paar CBP/p300), Enzyme, die sie entfernen (Sirtuine), und Enzyme, die die Acetyl-"Treibstoff"-Quelle Acetyl-CoA bereitstellen. Bei Weibchen stiegen die CBP/p300-Spiegel mit dem Alter und korrelierten mit dem Anstieg von acetyliertem Tau, während Enzyme zur Acetyl-CoA-Produktion und deacetylierende Sirtuine kaum Veränderungen zeigten. Das legt nahe, dass eine überaktive Acetyltransferase-Aktivität – und nicht ein veränderter Treibstoffvorrat oder mangelnder Abbau – die höhere Tau-Acetylierung bei Weibchen antreibt. Das Team untersuchte außerdem die Autophagie, den zellulären Recyclingweg, der unerwünschte Proteine und Strukturen umschließt und verdaut. Mit dem Alter verschoben sich mehrere Autophagie-Marker auf komplexe, geschlechtsspezifische Weise. Weibchen zeigten Hinweise auf reduzierte Bildung und Fluss von Recycling-Vesikeln, die Tau entfernen helfen, während Männchen andere Muster aufwiesen, einschließlich Anhäufung eines Cargo-Adapter-Proteins und vermehrter Nutzung eines verwandten Aufräumwegs.
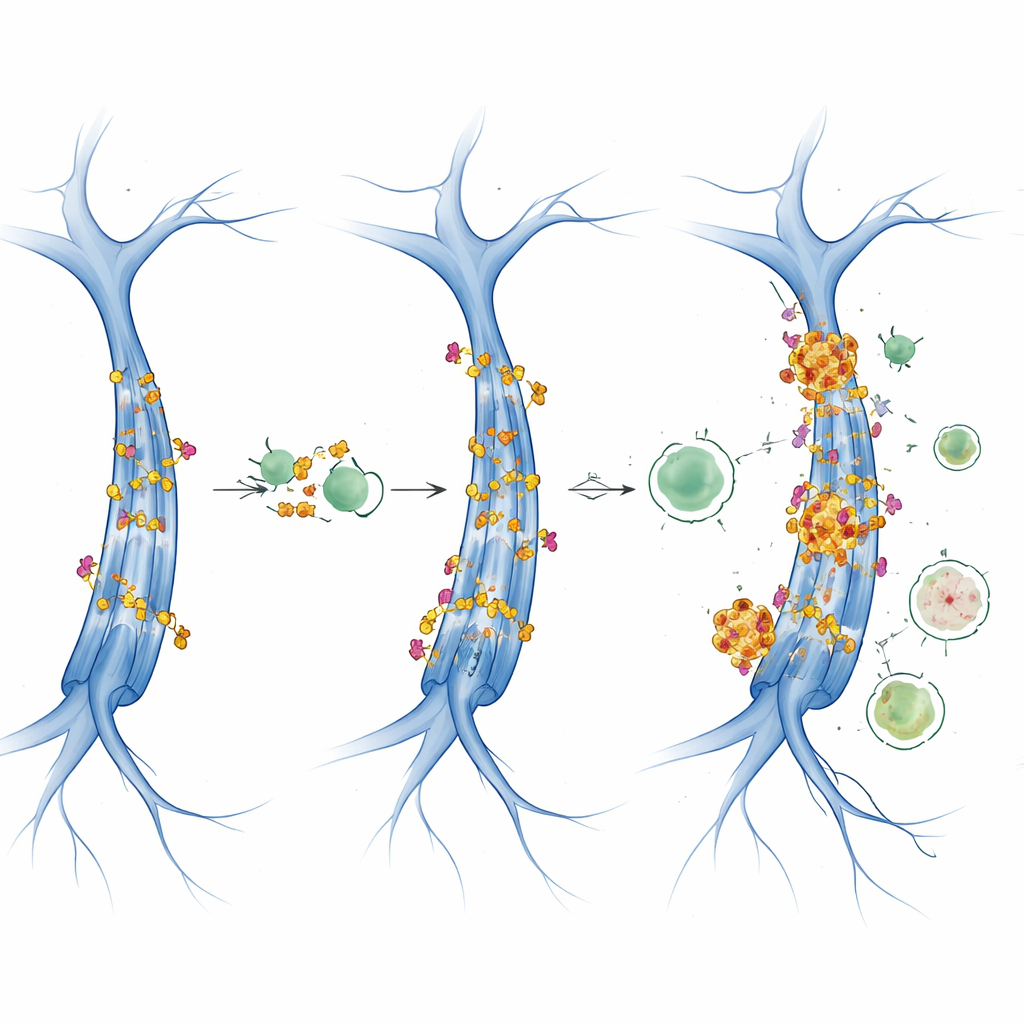
Signalwege, die das zelluläre Recycling bremsen
Die Studie untersuchte außerdem zwei zentrale Regulatoren von Zellwachstum und Energiehaushalt: mTOR und AMPK. Wenn mTOR stark aktiv ist, schaltet es tendenziell die Autophagie ab, während AMPK sie bei Energiestress fördert. Bei diesen Tau-Mäusen wirkte die AMPK-Aktivität weitgehend stabil über Alter und Geschlecht hinweg, aber mTOR-assoziierte Signale veränderten sich alters- und geschlechtsspezifisch. Die Daten deuten auf eine mTOR-getriebene Hemmung der Autophagie hin, die mit der Acetylierungsmaschinerie zusammenläuft. Bei Weibchen fielen steigende CBP/p300-Werte und acetyliertes Tau mit Markern für gestörten autophagischen Fluss zusammen, was auf eine Vorwärtskopplung hindeutet: Es wird mehr acetyliertes Tau erzeugt und gleichzeitig wird das System, das es entsorgen sollte, weniger effizient, sodass toxische Tau-Aggregate akkumulieren können.
Was das für Verständnis und Behandlung von Erkrankungen bedeutet
Für Nicht-Fachleute ist die Kernbotschaft, dass männliche und weibliche Gehirne im Alter nicht gleich mit demselben Krankheitsprotein umgehen. In diesem humanisierten Tau-Mausmodell neigen Weibchen besonders dazu, eine Acetylgruppe an Tau anzubringen, angetrieben durch höhere Aktivität spezifischer Enzyme und begleitet von schwächelndem zellulären Recycling. Männchen zeigen dagegen stärker Veränderungen in der Phosphorylierung und andere Modifikationen der Proteinräumungspfade. Obwohl die Arbeit an Mäusen und mit relativ kleinen Gruppen durchgeführt wurde, stützt sie die Idee, dass Acetylierung ein kritischer, geschlechtssensitiver Schritt bei der Tau-Akkumulation ist. Das macht Acetylierungs-bezogene Enzyme und Regulatoren der Autophagie zu attraktiven Zielstrukturen für geschlechtsspezifisch ausgerichtete Therapien mit dem langfristigen Ziel, taugetriebenen Hirnabbau zu verlangsamen oder zu verhindern.
Zitation: Sabir, U., Csubak, B.A., Ilchenko, S. et al. Sex-specific effects of acetylation on tauopathy in aging htau mice. Sci Rep 16, 11862 (2026). https://doi.org/10.1038/s41598-026-41691-0
Schlüsselwörter: Tau-Acetylierung, Geschlechtsunterschiede, Autophagie, Alzheimer-Krankheit, Neurodegeneration