Clear Sky Science · it
Effetti specifici del sesso dell’acetilazione sulla tauopatia nei topi htau invecchiati
Perché questo studio cerebrale è importante
La malattia di Alzheimer coinvolge milioni di famiglie e le donne ricevono la diagnosi più spesso degli uomini. Questo studio pone una domanda semplice ma potente: il cervello femminile invecchiato gestisce una proteina chiave legata all’Alzheimer in modo diverso rispetto a quello maschile? Utilizzando un modello murino che esprime versioni umane di questa proteina, i ricercatori si concentrano su sottili marche chimiche che possono rendere la proteina più propensa ad aggregarsi e più difficile da eliminare. I risultati indicano una vulnerabilità specifica per sesso che potrebbe aiutare a spiegare perché le donne tendono a mostrare cambiamenti cerebrali più gravi nell’Alzheimer e nei disturbi correlati.
Una proteina cerebrale appiccicosa sotto il microscopio
Al centro di questo lavoro c’è la tau, una proteina che normalmente contribuisce a stabilizzare i “binari” interni che i neuroni usano per spostare nutrienti e segnali. In molte malattie cerebrali la tau si comporta in modo scorretto, accumulandosi all’interno dei neuroni come piccoli aggregati tossici e, in seguito, come grovigli più grandi. Gli scienziati sapevano già che l’aggiunta di gruppi fosfato alla tau (fosforilazione) favorisce questa aggregazione. Questo studio si concentra su un altro tipo di marchio chimico, l’acetilazione, collocata su un sito specifico della tau chiamato lisina 174. Ricerche precedenti avevano suggerito che questa modifica acetilica compare precocemente nella malattia e può rallentare l’eliminazione della tau dal cervello. Gli autori hanno cercato di capire come questo marchio, e i sistemi di pulizia proteica correlati, cambino con l’età nei topi maschi e femmine che esprimono solo tau umana.
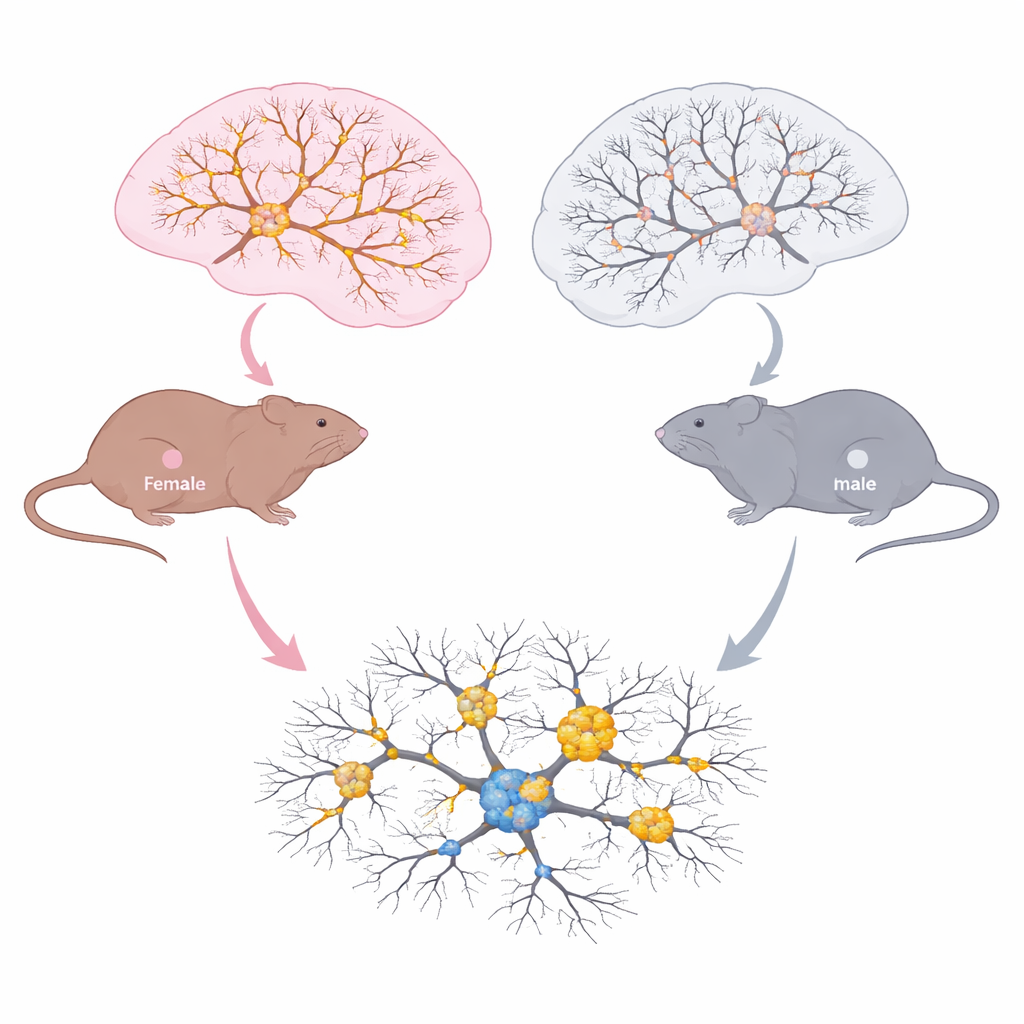
Come cervelli maschili e femminili invecchiano in modo diverso
Il gruppo ha esaminato regioni cerebrali importanti per memoria e decisione in tre fasi della vita: giovani adulti, mezza età e animali più anziani sintomatici. Nell’ippocampo e nella corteccia prefrontale hanno misurato la tau totale, la tau fosforilata, la tau acetilata sulla lisina 174 e piccoli aggregati di tau noti come oligomeri. Entrambi i sessi hanno accumulato più oligomeri di tau con l’età, segno di peggioramento della tauopatia. Ma il quadro delle modifiche chimiche differiva nettamente. Nelle femmine, la tau totale e la tau con il marchio acetilico sulla lisina 174 sono aumentate con l’età, e questo incremento è risultato correlato al carico di tau. Nei maschi, la fosforilazione della tau è aumentata con l’età, ma l’acetilazione sulla lisina 174 no. La microscopia ha mostrato che le femmine anziane presentavano più tau acetilata distribuita nelle principali zone dell’ippocampo e maggiore sovrapposizione tra tau acetilata e fosforilata, insieme a una maggiore attivazione delle microglia, le cellule immunitarie del cervello.
Quando le squadre di pulizia del cervello non tengono il passo
Per capire perché la tau si accumulasse in modo diverso a seconda del sesso, i ricercatori hanno esplorato i sistemi di manutenzione delle proteine nel cervello. Hanno esaminato gli enzimi che aggiungono i marchi acetilici (in particolare una coppia chiamata CBP/p300), gli enzimi che li rimuovono (sirtuine) e gli enzimi che forniscono il “carburante” dell’acetilazione, l’acetil-CoA. Nelle femmine, i livelli di CBP/p300 sono aumentati con l’età, in parallelo con l’aumento della tau acetilata, mentre gli enzimi produttrici di acetil-CoA e le sirtuine deacetilanti sono cambiati poco. Ciò suggerisce che l’iperattività degli acetil-transferasi, piuttosto che disponibilità del carburante o rimozione, guida la maggiore acetilazione della tau nelle femmine. Il team ha anche esaminato l’autofagia, la via di riciclo cellulare che ingloba e digerisce proteine e strutture indesiderate. Con l’età diversi marcatori dell’autofagia sono variati in modi complessi e dipendenti dal sesso. Le femmine hanno mostrato segnali di ridotta formazione e flusso dei vescicoli di riciclo che aiutano a eliminare la tau, mentre i maschi hanno mostrato schemi diversi, inclusi accumulo di una proteina adattatrice del carico e maggiore affidamento su una via di pulizia correlata.
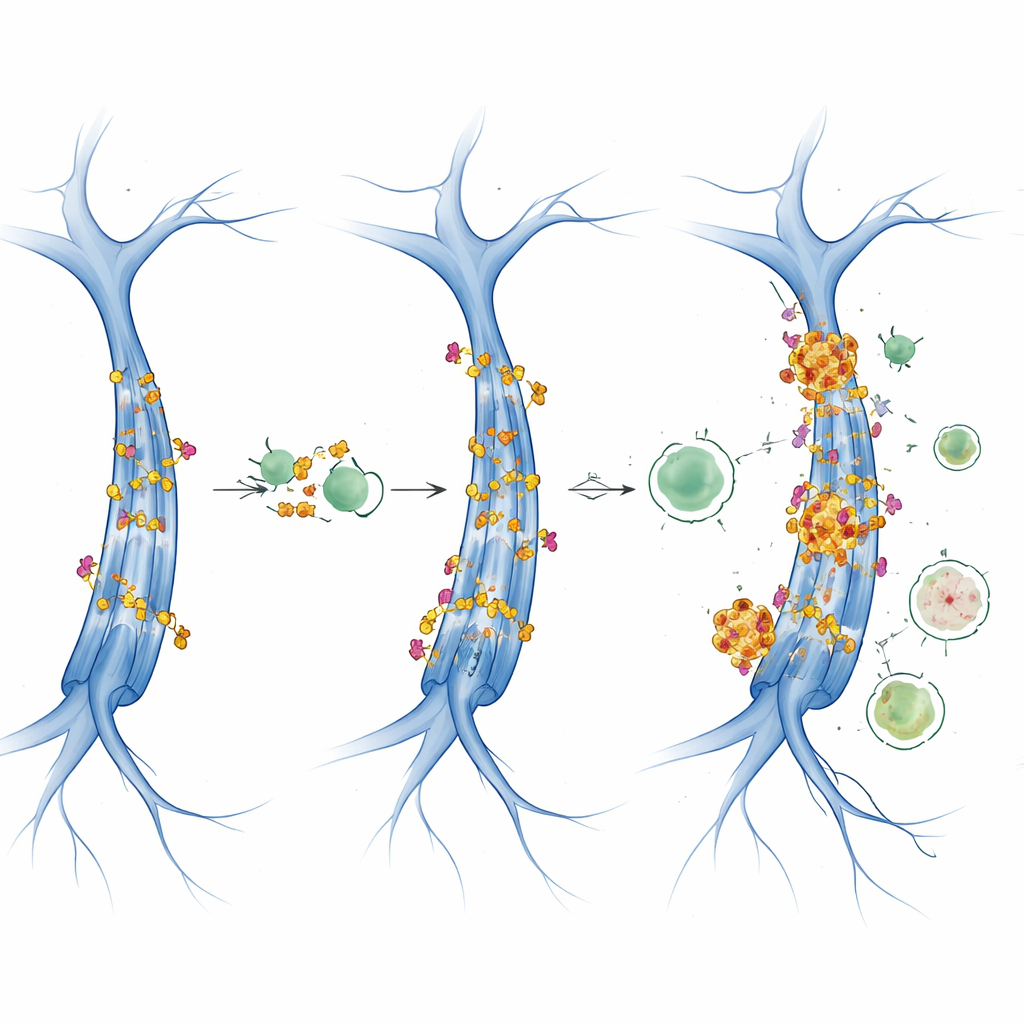
Segnali che rallentano il riciclo cellulare
Lo studio ha poi esplorato due regolatori principali della crescita cellulare e dell’uso energetico: mTOR e AMPK. Quando mTOR è molto attivo tende a spegnere l’autofagia, mentre AMPK la promuove in condizioni di stress energetico. In questi topi tau, l’attività di AMPK è sembrata sostanzialmente stabile attraverso età e sesso, ma i segnali legati a mTOR sono cambiati in modo specifico per età e sesso. I dati indicano un’inibizione dell’autofagia guidata da mTOR, che interseca la macchina dell’acetilazione. Nelle femmine, l’aumento di CBP/p300 e della tau acetilata è coinciso con marcatori di flusso autofagico compromesso, suggerendo un circuito autoalimentante: si produce più tau acetilata e, allo stesso tempo, il sistema che dovrebbe smaltirla diventa meno efficiente, permettendo l’accumulo di aggregati tossici di tau.
Cosa significa per comprendere e trattare la malattia
Per i non specialisti, il messaggio chiave è che cervelli maschili e femminili non gestiscono allo stesso modo la stessa proteina di malattia con l’invecchiamento. In questo modello murino con tau umanizzata, le femmine sono particolarmente inclini ad aggiungere un marchio acetilico alla tau, guidato da maggiore attività di enzimi specifici e accompagnato da un deterioramento del riciclo cellulare. I maschi, al contrario, mostrano più cambiamenti nella fosforilazione e alterazioni diverse nelle vie di smaltimento delle proteine. Pur essendo uno studio su topi e condotto con gruppi relativamente piccoli, supporta l’idea che l’acetilazione sia un passaggio critico e sensibile al sesso nell’accumulo di tau. Ciò rende gli enzimi legati all’acetilazione e i regolatori dell’autofagia bersagli attraenti per trattamenti tarati sul sesso biologico, con l’obiettivo a lungo termine di rallentare o prevenire il declino cerebrale guidato dalla tau.
Citazione: Sabir, U., Csubak, B.A., Ilchenko, S. et al. Sex-specific effects of acetylation on tauopathy in aging htau mice. Sci Rep 16, 11862 (2026). https://doi.org/10.1038/s41598-026-41691-0
Parole chiave: acetilazione della tau, differenze di sesso, autofagia, malattia di Alzheimer, neurodegenerazione