Clear Sky Science · pt
Efeitos específicos por sexo da acetilação na taupatia em camundongos htau envelhecidos
Por que este estudo cerebral é importante
A doença de Alzheimer afeta milhões de famílias, e mulheres recebem o diagnóstico com mais frequência que homens. Este estudo faz uma pergunta simples, porém poderosa: o cérebro feminino envelhecido lida de forma diferente com uma proteína chave relacionada ao Alzheimer em comparação ao cérebro masculino? Usando um modelo de camundongo que carrega versões humanas dessa proteína, os pesquisadores focam em marcas químicas sutis que podem tornar a proteína mais propensa a aglomerar-se e mais difícil de eliminar. As descobertas apontam para uma vulnerabilidade específica por sexo que pode ajudar a explicar por que mulheres tendem a apresentar alterações cerebrais mais severas no Alzheimer e em transtornos relacionados.
Uma proteína pegajosa sob o microscópio
No centro deste trabalho está a tau, uma proteína que normalmente ajuda a estabilizar os “trilhos” internos que os neurônios usam para transportar nutrientes e sinais. Em muitas doenças cerebrais, a tau se comporta mal, acumulando-se dentro dos neurônios como pequenos aglomerados tóxicos e, mais tarde, como emaranhados maiores. Já se sabia que a adição de grupos fosfato à tau (fosforilação) incentiva esse aglomeramento. Este estudo concentra-se em outro tipo de marca química, a acetilação, colocada em um sítio específico da tau chamado lisina 174. Pesquisas anteriores sugeriram que essa marca de acetil aparece cedo na doença e pode retardar a remoção da tau do cérebro. Os autores procuraram ver como essa marca, e os sistemas relacionados de limpeza de proteínas, mudam com a idade em camundongos do sexo masculino e feminino que expressam apenas a tau humana.
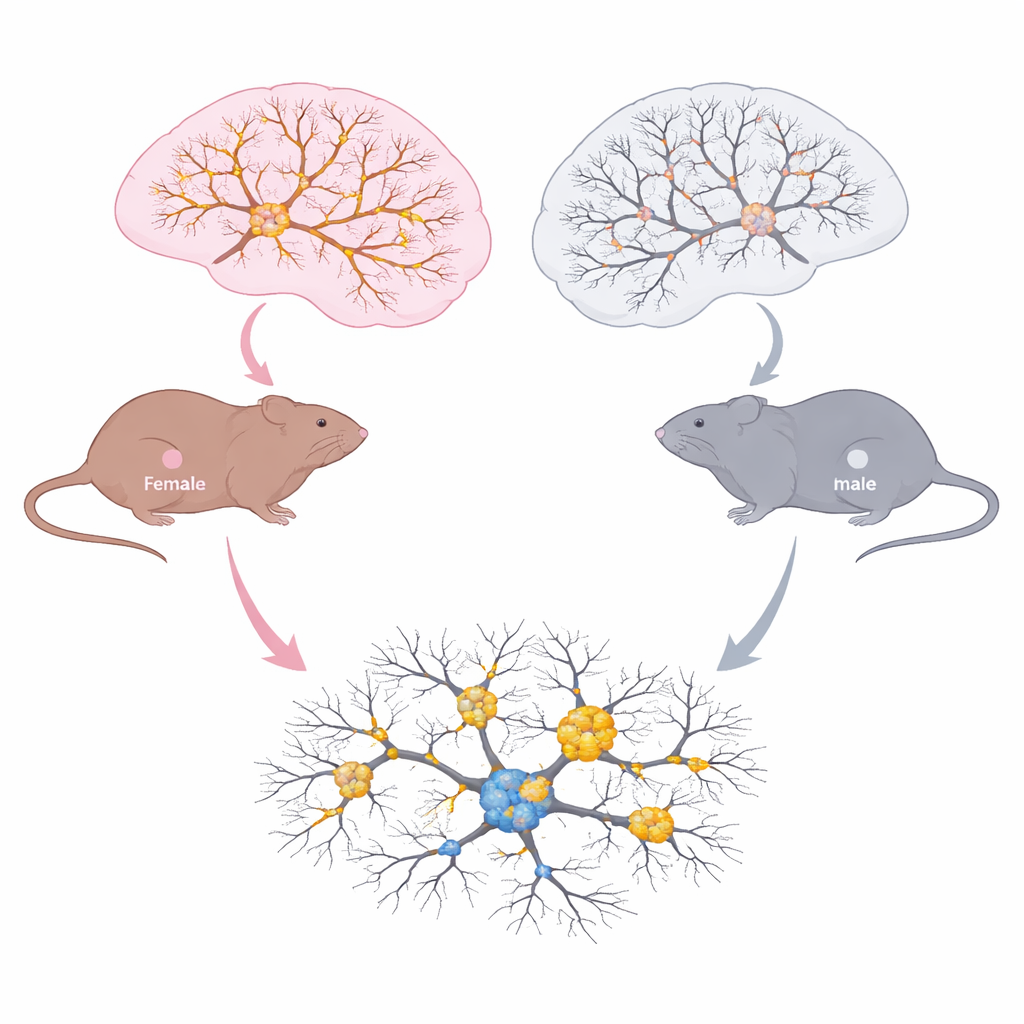
Como cérebros masculinos e femininos envelhecem de modo distinto
A equipe examinou regiões cerebrais importantes para memória e tomada de decisão em três estágios da vida: adultos jovens, meia-idade e animais mais velhos sintomáticos. No hipocampo e no córtex pré-frontal, mediram tau total, tau fosforilada, tau acetilada na lisina 174 e pequenos aglomerados de tau conhecidos como oligômeros. Ambos os sexos acumularam mais oligômeros de tau com a idade, sinal de piora da taupatia. Mas o padrão de mudanças químicas diferiu claramente. Nas fêmeas, a tau total e a tau com a marca de acetil na lisina 174 aumentaram com a idade, e esse aumento acompanhou a crescente carga de tau. Nos machos, a fosforilação da tau aumentou com o envelhecimento, mas a acetilação na lisina 174 não. A microscopia mostrou que fêmeas envelhecidas apresentavam mais tau acetilada espalhada por zonas-chave do hipocampo e maior sobreposição entre tau acetilada e fosforilada, além de maior ativação da microglia, as células imunes do cérebro.
Quando as equipes de limpeza do cérebro ficam para trás
Para entender por que a tau se acumulou de forma diferente por sexo, os pesquisadores investigaram os sistemas de manutenção de proteínas do cérebro. Eles olharam enzimas que adicionam marcas de acetil (notadamente um par chamado CBP/p300), enzimas que as removem (sirtuínas) e enzimas que fornecem o “combustível” acetil-CoA. Nas fêmeas, os níveis de CBP/p300 aumentaram com a idade, acompanhando a elevação da tau acetilada, enquanto as enzimas produtoras de acetil-CoA e as sirtuínas desacetilantes mudaram pouco. Isso sugere que enzimas acetil-transferases hiperativas, em vez de suprimento de combustível ou remoção, impulsionam a maior acetilação da tau nas fêmeas. A equipe também examinou a autofagia, a via de reciclagem celular que engloba e digere proteínas e estruturas indesejadas. Com o envelhecimento, vários marcadores de autofagia mudaram de maneiras complexas dependentes do sexo. As fêmeas mostraram sinais de redução na formação e no fluxo dos vesículos recicladores que ajudam a remover a tau, enquanto os machos exibiram padrões diferentes, incluindo acúmulo de uma proteína adaptadora de carga e maior dependência de uma rota de limpeza relacionada.
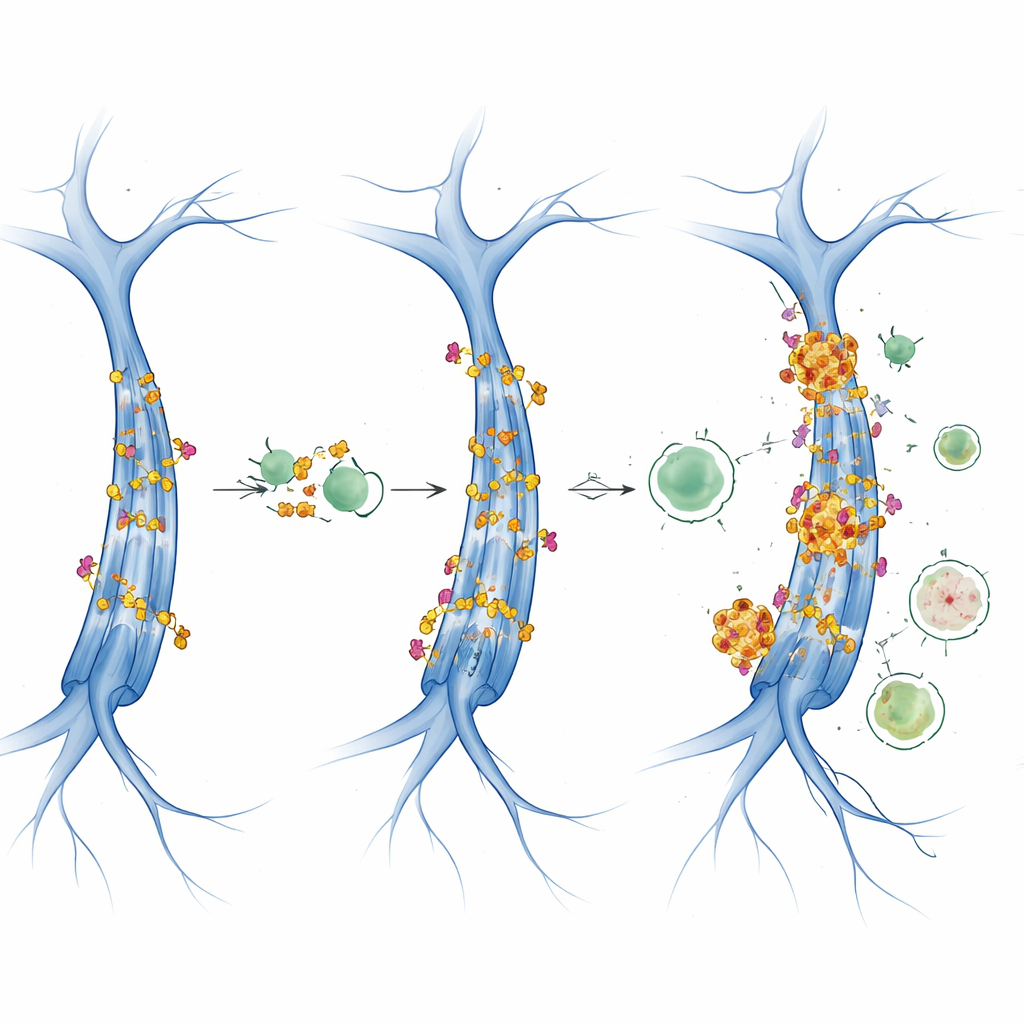
Sinais que desaceleram a reciclagem celular
O estudo explorou também dois reguladores mestres do crescimento celular e do uso de energia: mTOR e AMPK. Quando mTOR está altamente ativo, tende a desligar a autofagia, enquanto AMPK a promove sob estresse energético. Nestes camundongos com tau humana, a atividade de AMPK pareceu em grande parte estável ao longo da idade e entre os sexos, mas sinais relacionados ao mTOR mudaram de maneira específica por idade e sexo. Os dados apontam para uma inibição da autofagia dirigida por mTOR, que se cruza com a maquinaria de acetilação. Nas fêmeas, o aumento de CBP/p300 e da tau acetilada coincidiu com marcadores de fluxo autofágico prejudicado, sugerindo um ciclo de realimentação: mais tau acetilada é produzida e, ao mesmo tempo, o sistema que deveria descartá-la torna-se menos eficiente, permitindo que aglomerados tóxicos de tau se acumulem.
O que isso significa para compreender e tratar a doença
Para não especialistas, a mensagem-chave é que cérebros masculinos e femininos não lidam da mesma forma com a mesma proteína da doença à medida que envelhecem. Neste modelo de camundongo humanizado para tau, as fêmeas são particularmente propensas a adicionar uma marca de acetil à tau, impulsionadas por maior atividade de enzimas específicas e acompanhadas por uma reciclagem celular deficiente. Os machos, em contraste, mostram mais alterações na fosforilação e modificações diferentes nas vias de limpeza de proteínas. Embora o trabalho tenha sido realizado em camundongos e com grupos relativamente pequenos, ele apoia a ideia de que a acetilação é um passo crítico e sensível ao sexo na acumulação de tau. Isso torna enzimas relacionadas à acetilação e reguladores da autofagia alvos atraentes para tratamentos adaptados ao sexo biológico, com o objetivo a longo prazo de retardar ou prevenir o declínio cerebral dirigido pela tau.
Citação: Sabir, U., Csubak, B.A., Ilchenko, S. et al. Sex-specific effects of acetylation on tauopathy in aging htau mice. Sci Rep 16, 11862 (2026). https://doi.org/10.1038/s41598-026-41691-0
Palavras-chave: acetilação da tau, diferenças entre sexos, autofagia, doença de Alzheimer, neurodegeneração