Clear Sky Science · es
Efectos específicos por sexo de la acetilación en la tauopatía en ratones htau envejecidos
Por qué importa este estudio cerebral
La enfermedad de Alzheimer afecta a millones de familias, y las mujeres reciben el diagnóstico con más frecuencia que los hombres. Este estudio plantea una pregunta simple pero potente: ¿maneja el cerebro femenino envejecido una proteína clave relacionada con el Alzheimer de forma diferente al cerebro masculino? Usando un modelo de ratón que porta versiones humanas de esta proteína, los investigadores se centran en etiquetas químicas sutiles que pueden favorecer la agregación de la proteína y dificultar su eliminación. Sus hallazgos señalan una vulnerabilidad específica por sexo que podría ayudar a explicar por qué las mujeres tienden a mostrar cambios cerebrales más graves en el Alzheimer y trastornos relacionados.
Una proteína pegajosa bajo el microscopio
En el centro de este trabajo está la tau, una proteína que normalmente ayuda a estabilizar las “vías” internas que las neuronas usan para transportar nutrientes y señales. En muchas enfermedades cerebrales, la tau se comporta mal, acumulándose dentro de las neuronas como pequeños agregados tóxicos y, más tarde, como ovillos mayores. Ya se sabía que añadir grupos fosfato a la tau (fosforilación) favorece esa agregación. Este estudio se centra en otro tipo de etiqueta química, la acetilación, colocada en un sitio específico de la tau llamado lisina 174. Investigaciones previas sugirieron que esta marca de acetil aparece temprano en la enfermedad y puede ralentizar la eliminación de la tau del cerebro. Los autores se propusieron ver cómo cambia esta marca y los sistemas de limpieza de proteínas relacionados con la edad en ratones macho y hembra que expresan solo tau humana.
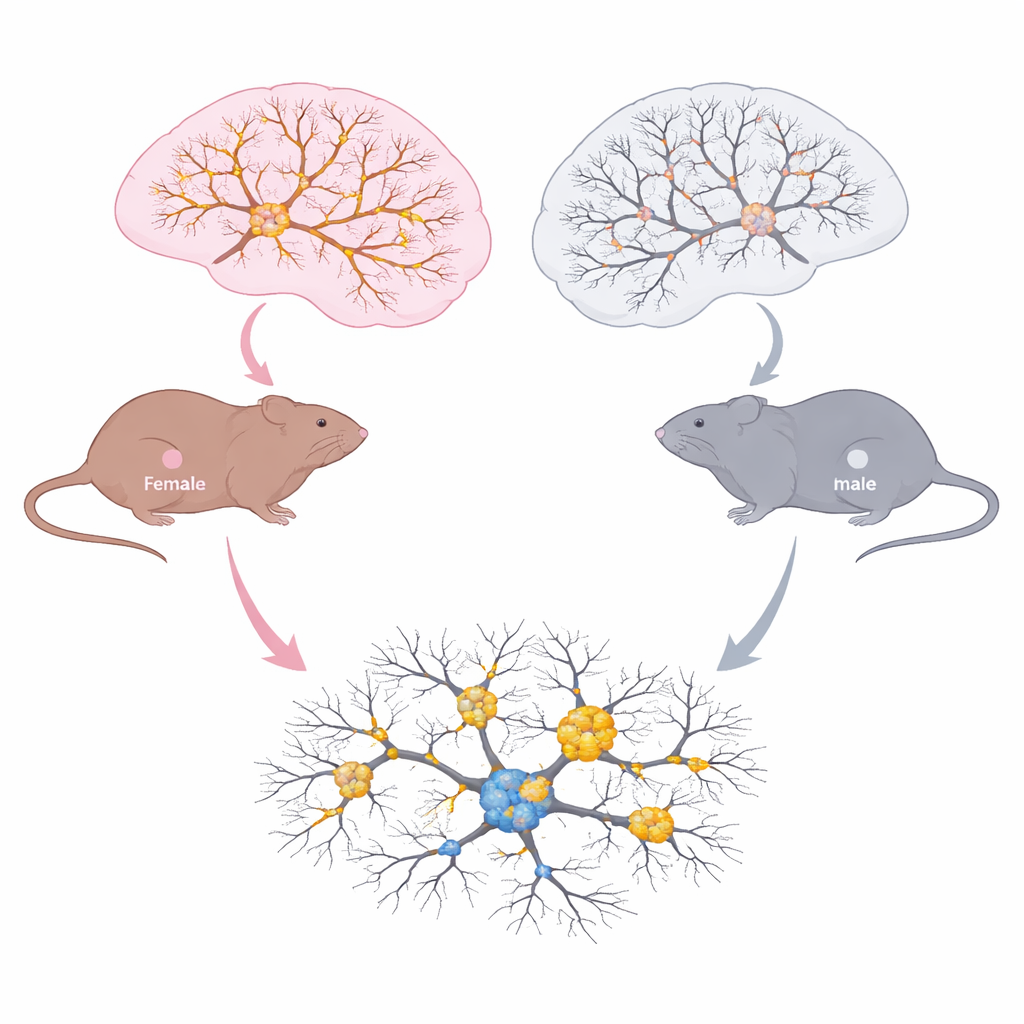
Cómo envejecen de forma diferente los cerebros masculinos y femeninos
El equipo examinó regiones cerebrales importantes para la memoria y la toma de decisiones en tres etapas de la vida: adultos jóvenes, mediana edad y animales mayores con síntomas. En el hipocampo y la corteza prefrontal midieron tau total, tau fosforilada, tau acetilada en la lisina 174 y pequeños agregados de tau conocidos como oligómeros. Ambos sexos acumularon más oligómeros de tau con la edad, un signo de empeoramiento de la tauopatía. Pero el patrón de cambios químicos difirió notablemente. En las hembras, la tau total y la tau con la marca de acetil en la lisina 174 aumentaron con la edad, y este aumento se correlacionó con la creciente carga de tau. En los machos, la fosforilación de la tau aumentó con la edad, pero la acetilación en la lisina 174 no lo hizo. La microscopía mostró que las hembras envejecidas tenían más tau acetilada distribuida por zonas clave del hipocampo y mayor solapamiento entre tau acetilada y fosforilada, junto con una mayor activación de la microglía, las células inmunitarias del cerebro.
Cuando las brigadas de limpieza del cerebro se quedan atrás
Para entender por qué la tau se acumuló de forma diferente según el sexo, los investigadores exploraron los sistemas de mantenimiento de proteínas del cerebro. Analizaron enzimas que añaden marcas de acetil (en particular un par llamado CBP/p300), enzimas que las eliminan (sirtuinas) y enzimas que suministran el “combustible” acetilo: acetil-CoA. En las hembras, los niveles de CBP/p300 aumentaron con la edad, coincidiendo con el incremento de tau acetilada, mientras que las enzimas productoras de acetil-CoA y las sirtuinas desacetilantes cambiaron poco. Esto sugiere que enzimas acetiltransferasas sobreactivas, más que la disponibilidad de combustible o la eliminación, impulsan una mayor acetilación de la tau en las hembras. El equipo también examinó la autofagia, la vía de reciclaje celular que engloba y digiere proteínas y estructuras no deseadas. Con el envejecimiento, varios marcadores de autofagia cambiaron de manera compleja y dependiente del sexo. Las hembras mostraron señales de reducción en la formación y el flujo de los vesículas de reciclaje que ayudan a eliminar la tau, mientras que los machos exhibieron patrones diferentes, incluyendo acumulación de una proteína adaptadora de carga y una mayor dependencia de una vía de limpieza relacionada.
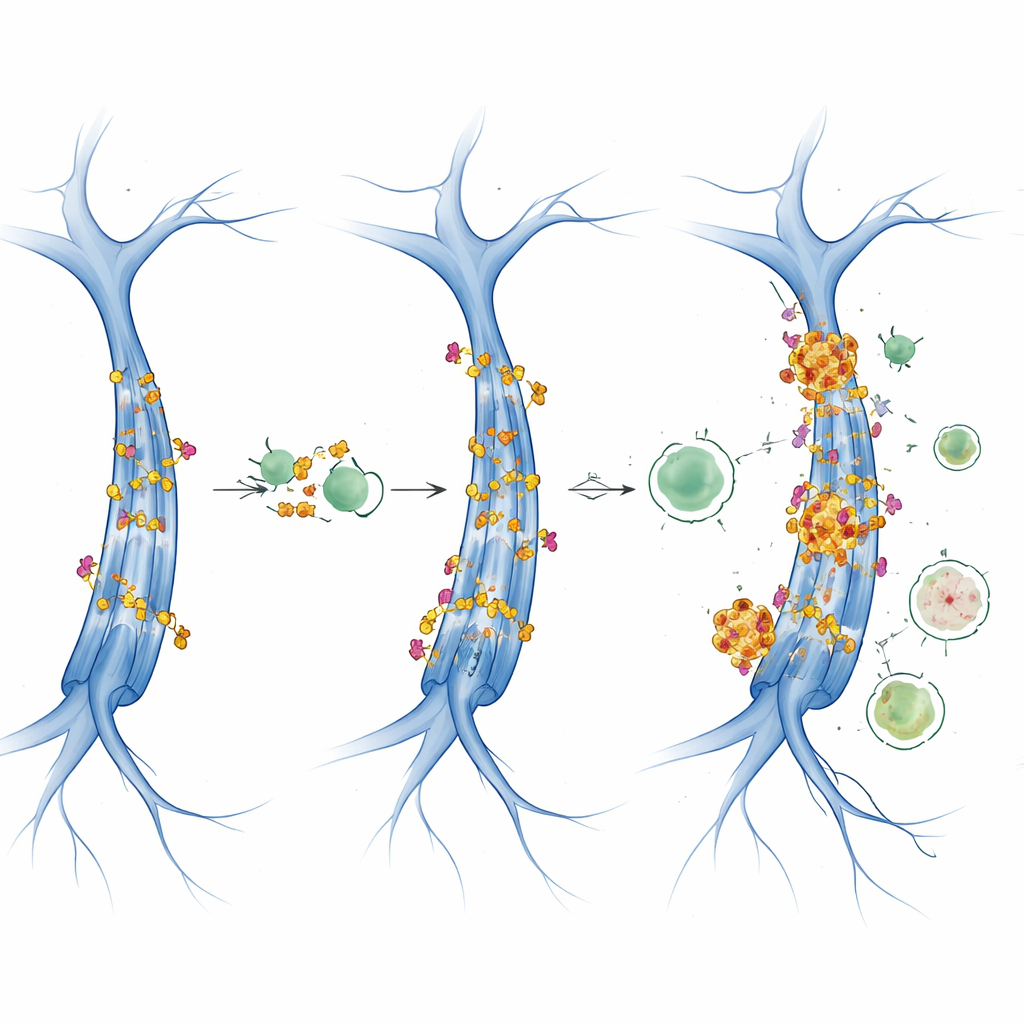
Señales que ralentizan el reciclaje celular
El estudio exploró además dos reguladores maestros del crecimiento celular y el uso de energía: mTOR y AMPK. Cuando mTOR está muy activo, tiende a apagar la autofagia, mientras que AMPK la promueve bajo estrés energético. En estos ratones con tau humana, la actividad de AMPK pareció en gran medida estable a través de la edad y el sexo, pero las señales relacionadas con mTOR cambiaron de forma dependiente de la edad y el sexo. Los datos apuntan hacia una inhibición de la autofagia motivada por mTOR que intersecta con la maquinaria de acetilación. En las hembras, el aumento de CBP/p300 y de tau acetilada coincidió con marcadores de flujo autofágico deteriorado, lo que sugiere un circuito de retroalimentación: se produce más tau acetilada y, al mismo tiempo, el sistema que debería descartarla se vuelve menos eficiente, permitiendo que los agregados tóxicos de tau se acumulen.
Qué significa esto para comprender y tratar la enfermedad
Para el público general, el mensaje clave es que los cerebros masculinos y femeninos no manejan la misma proteína patológica de igual forma a medida que envejecen. En este modelo de ratón humanizado para tau, las hembras son especialmente propensas a añadir una marca de acetil a la tau, impulsadas por una mayor actividad de enzimas específicas y acompañadas de un deterioro del reciclaje celular. Los machos, en contraste, muestran más cambios en la fosforilación y alteraciones diferentes en las vías de limpieza de proteínas. Aunque el trabajo se realizó en ratones y con grupos relativamente pequeños, respalda la idea de que la acetilación es un paso crítico y sensible al sexo en la acumulación de tau. Eso convierte a las enzimas relacionadas con la acetilación y a los reguladores de la autofagia en dianas atractivas para tratamientos adaptados al sexo biológico, con el objetivo a largo plazo de desacelerar o prevenir el deterioro cerebral impulsado por la tau.
Cita: Sabir, U., Csubak, B.A., Ilchenko, S. et al. Sex-specific effects of acetylation on tauopathy in aging htau mice. Sci Rep 16, 11862 (2026). https://doi.org/10.1038/s41598-026-41691-0
Palabras clave: acetilación de tau, diferencias sexuales, autofagia, enfermedad de Alzheimer, neurodegeneración