Clear Sky Science · tr
Yaşlanan htau farelerinde tauopati üzerine asetilemenin cinsiyete özgü etkileri
Bu beyin çalışması neden önemli
Alzheimer hastalığı milyonlarca aileyi etkiliyor ve kadınlar erkeklerden daha sık tanı alıyor. Bu çalışma basit ama güçlü bir soruyu gündeme getiriyor: yaşlanan dişi beyni, Alzheimer ile ilişkili anahtar bir proteini erkek beyninden farklı mı ele alıyor? İnsan versiyonlarını taşıyan bir fare modeli kullanarak, araştırmacılar proteinin kümelenme eğilimini artırıp temizlenmesini zorlaştırabilen ince kimyasal işaretlere odaklanıyor. Bulgular, kadınlarda daha şiddetli beyin değişikliklerinin görülmesini açıklamaya yardımcı olabilecek cinsiyete özgü bir savunmasızlığa işaret ediyor.
İnceleme altındaki yapışkan beyin proteini
Bu çalışmanın merkezinde, nöronların besin ve sinyalleri hareket ettirmek için kullandığı iç “rayları” normalde stabilize etmeye yardımcı olan tau proteini var. Birçok beyin hastalığında tau yanlış davranır; nöron içinde küçük toksik kümeler ve daha sonra daha büyük düğümler halinde birikir. Bilim insanları zaten tauya fosfat grupları eklenmesinin (fosforilasyon) bu kümelenmeyi teşvik ettiğini biliyordu. Bu çalışma, lysin 174 adı verilen belirli bir yerde oluşan başka bir kimyasal işaret olan asetilasyona odaklanıyor. Önceki araştırmalar bu asetil işaretinin hastalığın erken döneminde ortaya çıktığını ve tau’nun beyinden temizlenmesini yavaşlatabileceğini öne sürmüştü. Yazarlar, bu işaretin ve ilişkili protein-temizleme sistemlerinin erkek ve dişi yalnızca insan tau’su ifade eden farelerde yaşa bağlı olarak nasıl değiştiğini görmek için yola çıktı.
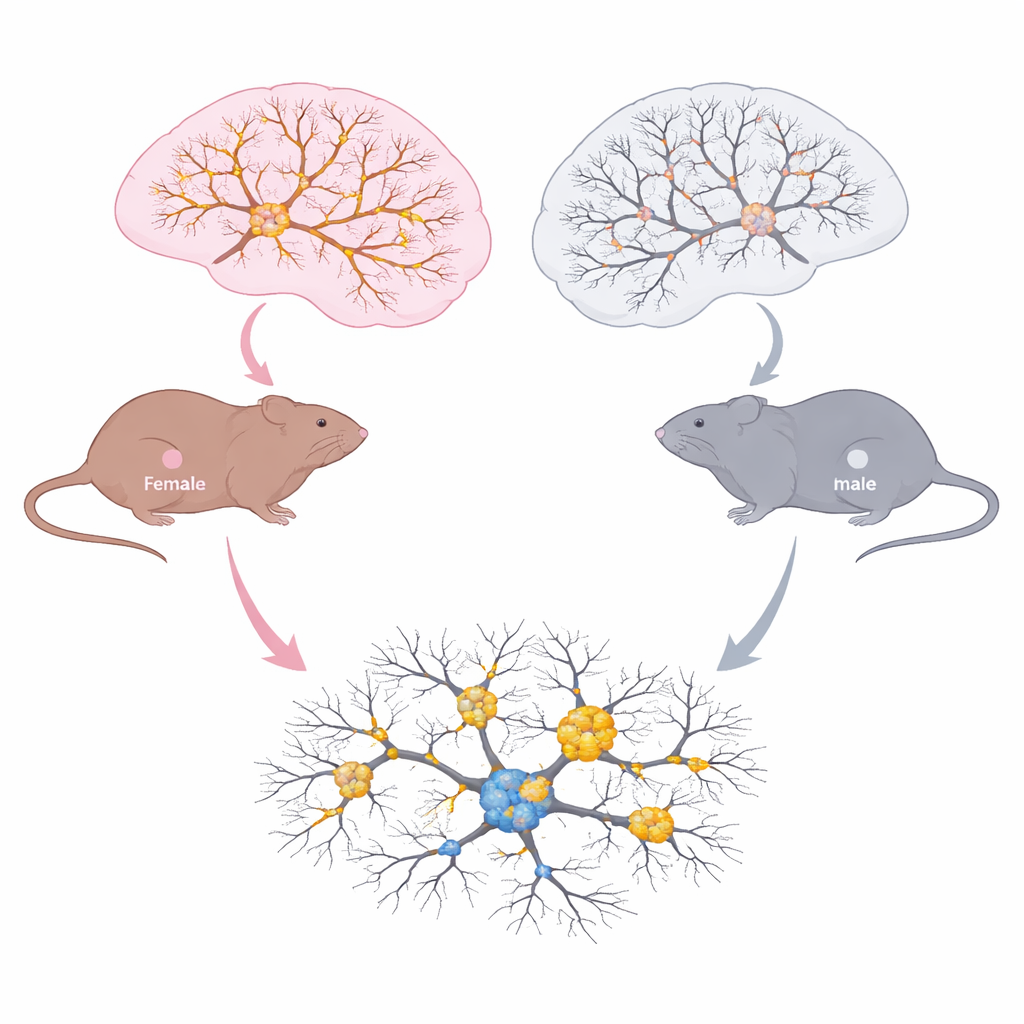
Erkek ve dişi beyinlerin farklı yaşlanma biçimleri
Ekip, bellek ve karar verme için önemli beyin bölgelerini üç yaşam evresinde inceledi: genç erişkinler, orta yaş ve ileri semptomatik hayvanlar. Hipokampus ve prefrontal kortekste toplam tau, fosforile tau, lysin 174’te asetile tau ve oligomer olarak bilinen küçük tau kümeleri ölçüldü. Her iki cinsiyette de yaşla birlikte daha fazla tau oligomeri birikti; bu, tauopatinin kötüleştiğinin bir işareti. Ancak kimyasal değişimlerin deseni keskin şekilde farklıydı. Dişilerde toplam tau ve lysin 174’teki asetil işareti taşıyan tau yaşla arttı ve bu artış artan tau yükü ile paralel ilerledi. Erkeklerde ise tau’nun fosforilasyonu yaşla birlikte yükseldi, ancak lysin 174’teki asetilasyon artmadı. Mikroskopi, yaşlı dişilerde asetile tau’nun önemli hipokampal bölgelerde daha yaygın olduğunu ve asetile ile fosforile tau arasında daha fazla örtüşme ile birlikte beyin bağışıklık hücreleri olan mikroglia aktivasyonunun arttığını gösterdi.
Beynin temizlik ekipleri geride kaldığında
Tau’nun cinsiyete göre neden farklı biriktiğini anlamak için araştırmacılar beynin protein bakım sistemlerini inceledi. Asetil işaretlerini ekleyen enzimleri (özellikle CBP/p300 çiftini), bunları kaldıran enzimleri (sirtuinler) ve asetil “yakıtı” olan asetil-CoA’yı sağlayan enzimleri incelediler. Dişilerde CBP/p300 düzeyleri yaşla birlikte yükseldi ve bu, asetile tau’daki artışla örtüştü; oysa asetil-CoA üreten enzimler ve deasetilasyon yapan sirtuinler çok az değişti. Bu durum, yakıt tedariki veya kaldırmadan ziyade aşırı aktif asetil-transferaz enzimlerinin dişilerde daha yüksek tau asetilasyonuna yol açtığını düşündürüyor. Ekip ayrıca otofajiyi, istenmeyen proteinleri ve yapıları yakalayıp sindiren hücresel geri dönüşüm yolunu inceledi. Yaşlanmayla birlikte birkaç otofaji işareti karmaşık, cinsiyete bağlı değişimler gösterdi. Dişiler, tau’yu temizlemeye yardımcı olan geri dönüşüm veziküllerinin oluşumunda ve akışında azalma belirtileri gösterirken; erkekler farklı desenler sergiledi; bunlar arasında bir taşıyıcı adaptör proteinin birikmesi ve ilişkili bir temizleme yoluna artan bağımlılık yer aldı.
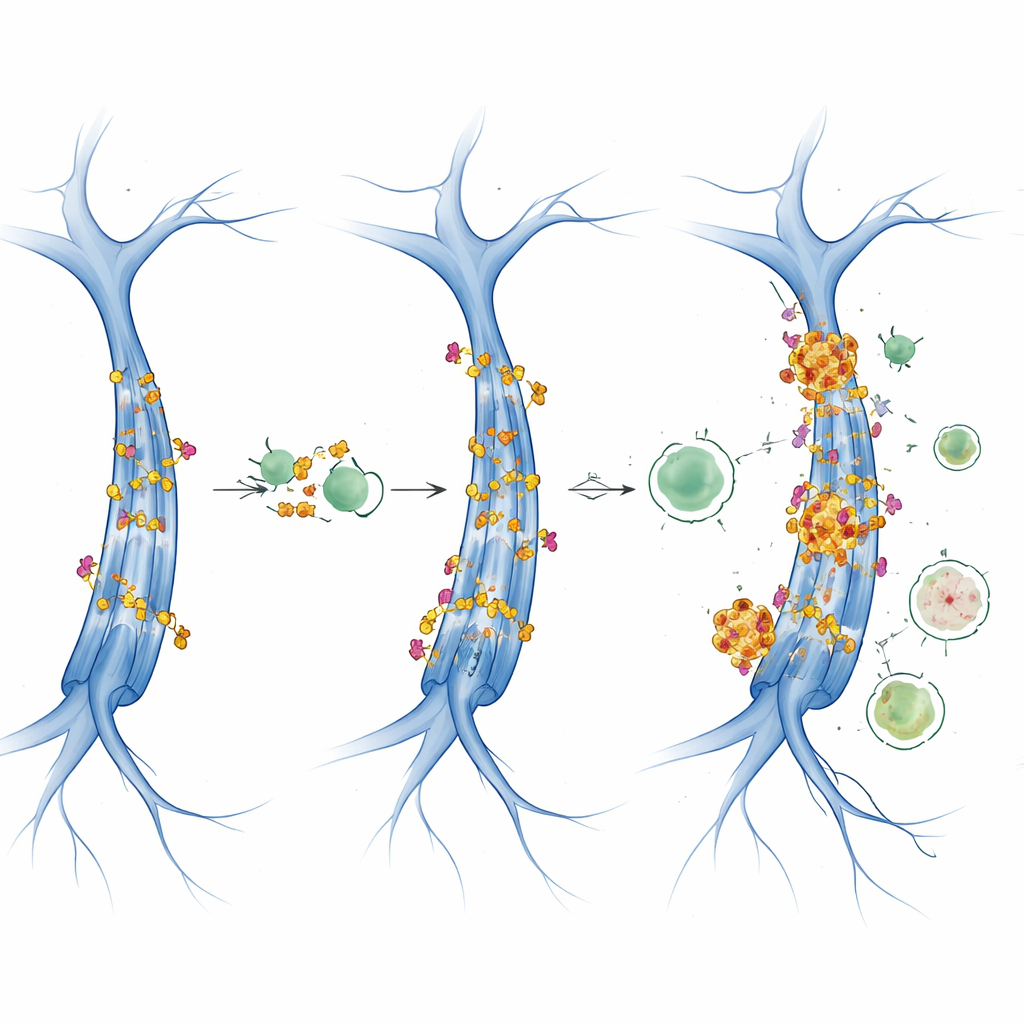
Hücresel geri dönüşümü yavaşlatan sinyaller
Çalışma ayrıca hücre büyümesinin ve enerji kullanımının iki ana düzenleyicisini, mTOR ve AMPK’yı daha ayrıntılı inceledi. mTOR yüksek derecede aktif olduğunda genellikle otofajiyi kapatırken, AMPK enerji stresi altında otofajiyi teşvik eder. Bu tau farelerinde AMPK aktivitesi yaş ve cinsiyet boyunca büyük ölçüde sabit görünürken, mTOR ile ilişkili sinyaller yaşa ve cinse özgü şekilde değişti. Veriler, asetilasyon mekanizması ile kesişen mTOR kaynaklı otofaji inhibisyonuna işaret ediyor. Dişilerde artan CBP/p300 ve asetile tau, bozulmuş otofagik akış belirteçleriyle eş zamanlı görüldü; bu da bir ileri besleme döngüsünü düşündürüyor: daha fazla asetile tau üretiliyor ve aynı zamanda onu atması gereken sistem daha az verimli hale geliyor, toksik tau kümelerinin birikmesine olanak tanıyor.
Hastalığı anlamak ve tedavi etmek için ne anlama geliyor
Uzman olmayanlar için ana mesaj, erkek ve dişi beyinlerin yaşlanırken aynı hastalık proteiniyle aynı şekilde başa çıkmadığıdır. Bu insanlaştırılmış tau fare modelinde, dişiler özellikle belirli enzimlerin daha yüksek aktivitesi tarafından yönlendirilen bir asetil etiketi tau’ya eklemeye yatkın ve bu durum başarısız olan hücresel geri dönüşümle birlikte görülüyor. Buna karşılık erkekler daha çok fosforilasyonda ve protein temizleme yollarındaki farklı değişimlerde belirginlik gösteriyor. Çalışma farelerde ve nispeten küçük gruplarla yapılmış olmasına rağmen, asetilasyonun tau birikiminde kritik ve cinsiyete duyarlı bir adım olduğu fikrini destekliyor. Bu da asetilasyonla ilişkili enzimleri ve otofaji düzenleyicilerini biyolojik cinsiyete göre uyarlanmış tedaviler için çekici hedefler haline getiriyor; uzun vadeli amaç, tau kaynaklı beyin gerilemeyi yavaşlatmak veya önlemektir.
Atıf: Sabir, U., Csubak, B.A., Ilchenko, S. et al. Sex-specific effects of acetylation on tauopathy in aging htau mice. Sci Rep 16, 11862 (2026). https://doi.org/10.1038/s41598-026-41691-0
Anahtar kelimeler: tau asetilasyonu, cinsiyet farkları, otofaji, Alzheimer hastalığı, nörodejenerasyon