Clear Sky Science · pl
Płeć a acetylacja i ich wpływ na tauopatię u starzejących się myszy htau
Dlaczego to badanie mózgu ma znaczenie
Choroba Alzheimera dotyka miliony rodzin, a kobiety otrzymują diagnozę częściej niż mężczyźni. W tym badaniu zadano proste, lecz istotne pytanie: czy starzejący się mózg kobiety radzi sobie z kluczowym białkiem związanym z Alzheimerem inaczej niż mózg mężczyzny? Używając modelu mysiego z ludzką wersją tego białka, badacze skupili się na subtelnych chemicznych znacznikach, które mogą zwiększać skłonność białka do agregacji i utrudniać jego usuwanie. Wyniki wskazują na wrażliwość specyficzną dla płci, która może pomóc wyjaśnić, dlaczego u kobiet częściej obserwuje się bardziej nasilone zmiany mózgowe w przebiegu choroby Alzheimera i powiązanych zaburzeń.
Lepkie białko mózgu pod mikroskopem
W centrum tego badania znajduje się tau — białko, które normalnie pomaga stabilizować wewnętrzne «tory», po których neurony transportują składniki odżywcze i sygnały. W wielu chorobach mózgu tau źle się zachowuje, gromadząc się w neuronach jako małe toksyczne skupiska, a później jako większe splątania. Naukowcy wiedzieli już, że dodanie grup fosforanowych do tau (fosforylacja) sprzyja temu procesowi. To badanie skupia się na innym rodzaju chemicznego markera — acetylacji — umiejscowionej w specyficznym miejscu tau zwanym lizyną 174. Wcześniejsze badania sugerowały, że ta acetylacja pojawia się we wczesnym stadium choroby i może hamować usuwanie tau z mózgu. Autorzy postanowili sprawdzić, jak ten znak i powiązane systemy „czyszczenia” białek zmieniają się z wiekiem u samców i samic myszy wyrażających wyłącznie ludzki tau.
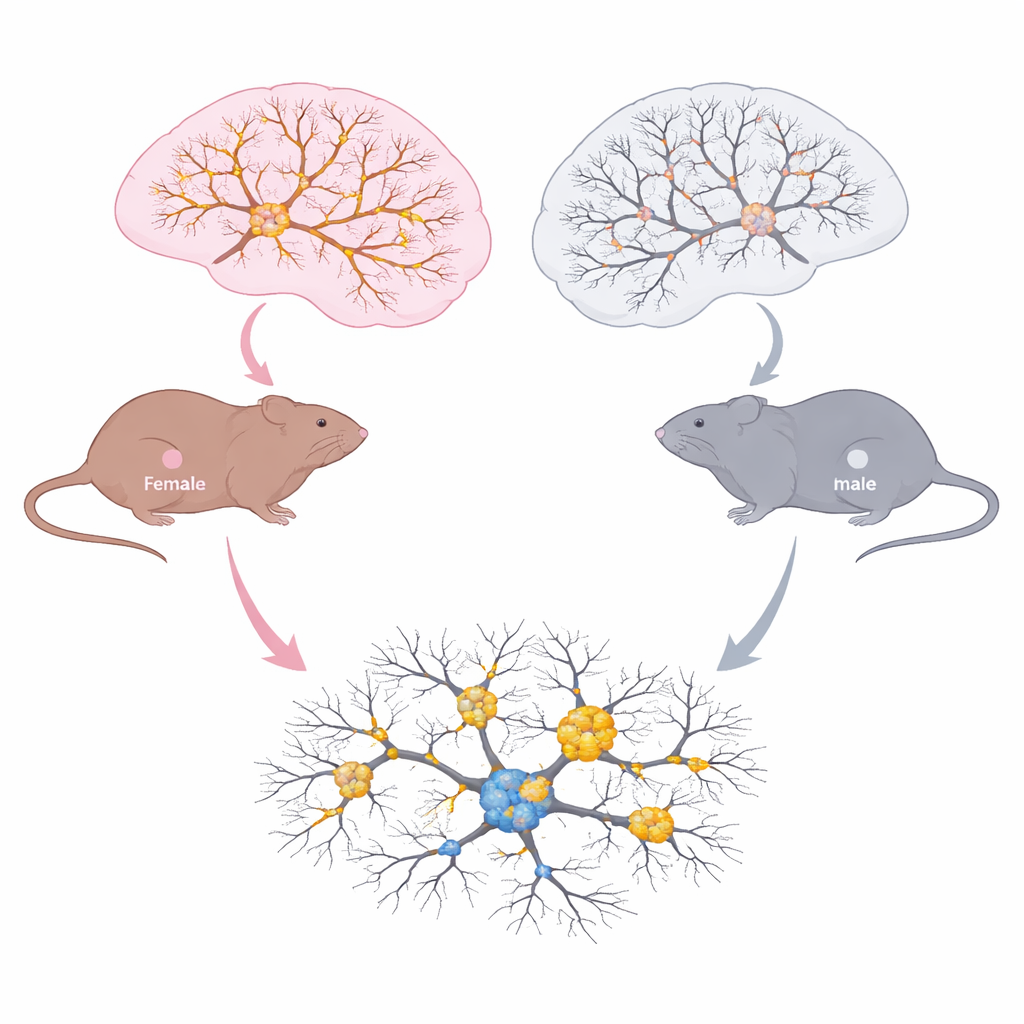
Jak różnie starzeją się mózgi samców i samic
Zespół badał obszary mózgu istotne dla pamięci i podejmowania decyzji w trzech etapach życia: młodych dorosłych, w średnim wieku i starszych osobników z objawami. W hipokampie i korze przedczołowej mierzyli całkowity poziom tau, fosforylowany tau, acetylowany tau przy lizynie 174 oraz małe skupiska tau zwane oligomerami. U obu płci wraz z wiekiem narastała liczba oligomerów tau — znak pogarszającej się tauopatii. Jednak wzory zmian chemicznych różniły się wyraźnie. U samic całkowity poziom tau i tau z acetylacją przy lizynie 174 wzrastały z wiekiem, a ten wzrost korelował ze zwiększonym obciążeniem tau. U samców natomiast fosforylacja tau nasilała się z wiekiem, podczas gdy acetylacja przy lizynie 174 nie ulegała zmianie. Mikroskopia wykazała, że u starych samic acetylowany tau był bardziej rozprzestrzeniony w kluczowych obszarach hipokampa i częściej współwystępował z fosforylowanym tau, wraz z nasileniem aktywacji mikrogleju — komórek odpornościowych mózgu.
Kiedy zespoły sprzątające mózgu nie nadążają
Aby zrozumieć, dlaczego tau gromadził się różnie w zależności od płci, badacze przeanalizowali systemy utrzymania białek w mózgu. Przyglądali się enzymom dodającym grupy acetylowe (w szczególności enzymom CBP/p300), enzymom je usuwającym (sirtuiny) oraz enzymom dostarczającym «paliwa» do acetylacji — acetyl-CoA. U samic poziomy CBP/p300 rosły z wiekiem, co odpowiadało wzrostowi acetylowanego tau, podczas gdy enzymy produkujące acetyl-CoA i deacetylujące sirtuiny zmieniały się nieznacznie. To sugeruje, że to nadmierna aktywność transferaz acetylowych, a nie dostępność paliwa czy usuwanie, napędza wyższą acetylację tau u samic. Zespół badał także autofagię — komórkową ścieżkę recyklingu, która otacza i trawi niechciane białka i struktury. W miarę starzenia kilka markerów autofagii zmieniało się w złożony, zależny od płci sposób. U samic zaobserwowano oznaki zmniejszonego tworzenia i przepływu pęcherzyków recyklingowych pomagających usuwać tau, podczas gdy u samców występowały inne wzory, w tym kumulacja białka-adaptora ładunku i zwiększone poleganie na powiązanej drodze oczyszczania.
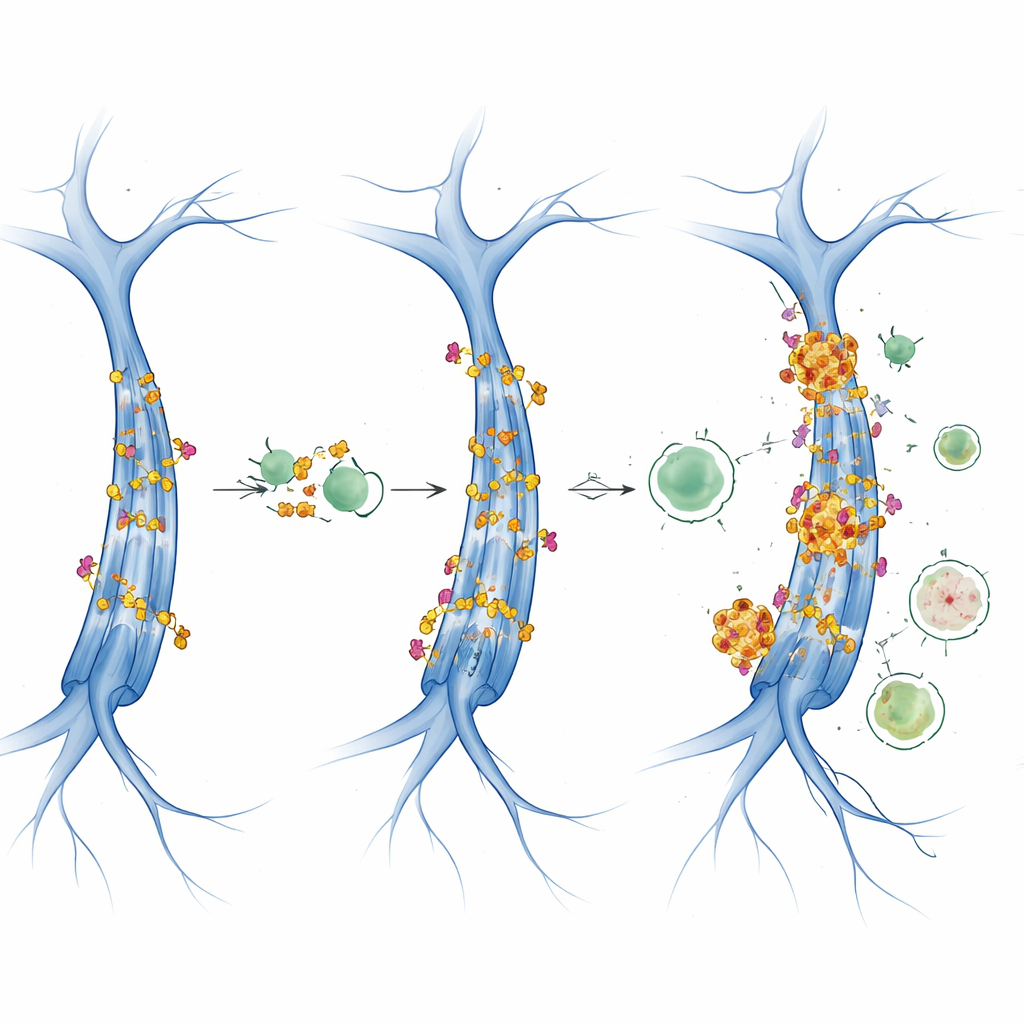
Sygnały, które spowalniają komórkowy recykling
Badanie dodatkowo zgłębiło dwie główne regulujące szlaki wzrostu komórek i wykorzystania energii: mTOR i AMPK. Kiedy mTOR jest mocno aktywny, ma tendencję do hamowania autofagii, podczas gdy AMPK ją promuje w warunkach niedoboru energii. U tych myszy z ludzkim tau aktywność AMPK wydawała się w dużej mierze stabilna w zależności od wieku i płci, natomiast sygnały związane z mTOR zmieniały się w sposób zależny od wieku i płci. Dane wskazują na hamowanie autofagii przez mTOR, które przecina się z mechanizmami acetylacji. U samic rosnące poziomy CBP/p300 i acetylowanego tau współwystępowały z markerami upośledzonego przepływu autofagicznego, sugerując pętlę sprzężenia zwrotnego: produkowane jest więcej acetylowanego tau, a jednocześnie system, który powinien je usuwać, staje się mniej wydajny, co pozwala toksycznym agregatom tau narastać.
Co to oznacza dla zrozumienia i leczenia choroby
Dla osób niebędących specjalistami kluczowy przekaz brzmi: mózgi samców i samic nie radzą sobie tak samo z tym samym białkiem chorobowym w miarę starzenia się. W tym modelu myszy z ludzkim tau samice są szczególnie podatne na dodawanie znacznika acetylowego do tau, napędzane wyższą aktywnością określonych enzymów i towarzyszące temu osłabienie komórkowego recyklingu. Samce z kolei wykazują więcej zmian w fosforylacji i inne modyfikacje dróg oczyszczania białek. Choć badanie przeprowadzono na myszach i na stosunkowo małych grupach, wspiera ono pogląd, że acetylacja jest kluczowym, wrażliwym na płeć etapem w nagromadzaniu tau. To czyni enzymy związane z acetylacją i regulatory autofagii atrakcyjnymi celami terapeutycznymi, które można dostosować do biologicznej płci, z długoterminowym celem spowolnienia lub zapobiegania spadkowi funkcji mózgu wywołanemu przez tau.
Cytowanie: Sabir, U., Csubak, B.A., Ilchenko, S. et al. Sex-specific effects of acetylation on tauopathy in aging htau mice. Sci Rep 16, 11862 (2026). https://doi.org/10.1038/s41598-026-41691-0
Słowa kluczowe: acetylacja tau, różnice związane z płcią, autofagia, choroba Alzheimera, neurodegeneracja