Clear Sky Science · ru
Половые различия в эффектах ацетилирования на тау-патологию у стареющих мышей htau
Почему это исследование мозга важно
Болезнь Альцгеймера затрагивает миллионы семей, и женщины получают диагноз чаще, чем мужчины. Это исследование задаёт простой, но важный вопрос: по‑разному ли стареющий женский мозг справляется с ключевым белком, связанным с Альцгеймером, по сравнению с мужским мозгом? Используя модель мыши, несущую человеческие варианты этого белка, исследователи сосредотачиваются на тонких химических метках, которые делают белок более склонным к слипанию и труднее удаляемым. Их выводы указывают на половую уязвимость, которая может помочь объяснить, почему у женщин чаще наблюдаются более серьёзные изменения мозга при болезни Альцгеймера и родственных расстройствах.
Клеящийся белок под микроскопом
В центре этого исследования — тау, белок, который обычно помогает стабилизировать внутренние «рельсы», по которым нейроны транспортируют питательные вещества и сигналы. При многих заболеваниях мозга тау ведёт себя неправильно, накапливаясь в нейронах сперва в виде мелких токсичных скоплений, а затем в виде более крупных клубков. Учёным уже было известно, что фосфорилирование тау способствует этому слипанию. В этой работе внимание сосредоточено на другом типе химической метки — ацетилировании, нанесённом на конкретный участок тау, лизин 174. Ранние исследования указывали, что эта ацетильная метка появляется на ранних стадиях болезни и может замедлять выведение тау из мозга. Авторы стремились выяснить, как эта метка и связанные с ней системы очистки белков меняются с возрастом у самцов и самок мышей, экспрессирующих только человеческий тау.
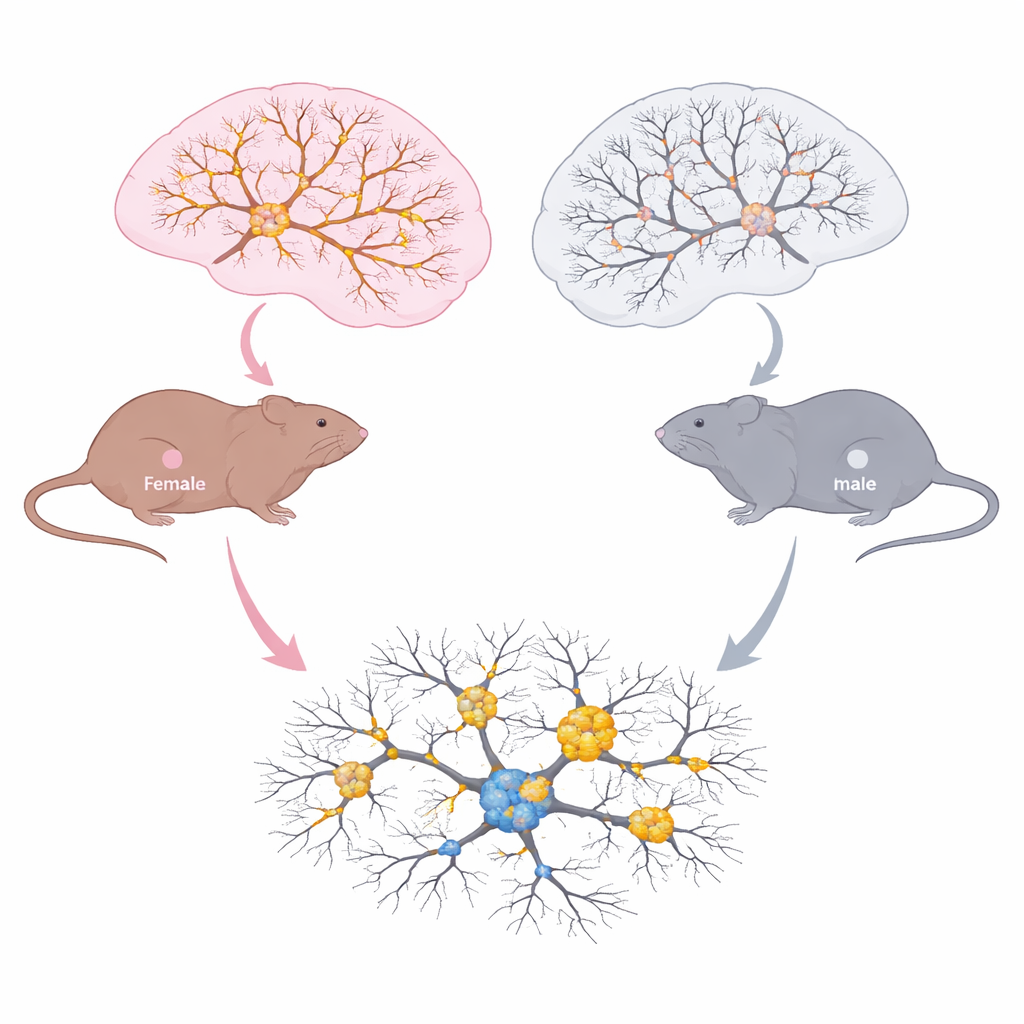
Как мужские и женские мозги стареют по‑разному
Команда исследовала области мозга, важные для памяти и принятия решений, на трёх этапах жизни: молодых взрослых, среднего возраста и старых животных с симптомами. В гиппокампе и префронтальной коре они измеряли общий тау, фосфорилированный тау, ацетилированный тау на лизине 174 и мелкие кластеры тау, известные как олигомеры. У обоих полов с возрастом увеличивалось накопление олигомеров тау — признак прогрессирующей тау-патологии. Но картина химических изменений резко отличалась по полу. У самок общий тау и тау с ацетильной меткой на лизине 174 возрастали с возрастом, и это увеличение соответствовало росту нагрузки тау. У самцов наблюдалось возрастание фосфорилирования тау с возрастом, тогда как ацетилирование на лизине 174 не изменялось. Микроскопия показала, что в старых самках ацетилированный тау шире распространялся по ключевым зонам гиппокампа и чаще совпадал с фосфорилированным тау, наряду с усиленной активацией микроглии — иммунных клеток мозга.
Когда уборщики мозга отстают
Чтобы понять, почему тау накапливался по‑разному у самцов и самок, исследователи изучили системы поддержания белков в мозге. Они рассмотрели ферменты, добавляющие ацетильные метки (в частности пару CBP/p300), ферменты, удаляющие их (сиртуины), и ферменты, обеспечивающие «топливо» для ацетилирования — ацетил‑CoA. У самок уровни CBP/p300 повышались с возрастом, что соответствовало росту ацетилированного тау, тогда как ферменты, производящие ацетил‑CoA, и деацетилазные сиртуины изменялись мало. Это говорит о том, что повышенная активность ацетилтрансфераз, а не дефицит «топлива» или снижение удаления, приводит к более высокому ацетилированию тау у самок. Команда также изучала аутофагию — путь внутриклеточного рециркулирования, который захватывает и переваривает ненужные белки и структуры. С возрастом несколько маркеров аутофагии смещались сложным образом, зависящим от пола. У самок наблюдались признаки уменьшения образования и динамики везикул рециркуляции, помогающих очищать тау, тогда как у самцов отмечались иные изменения, включая накопление адапторного белка груза и увеличенную зависимость от родственного пути очистки.
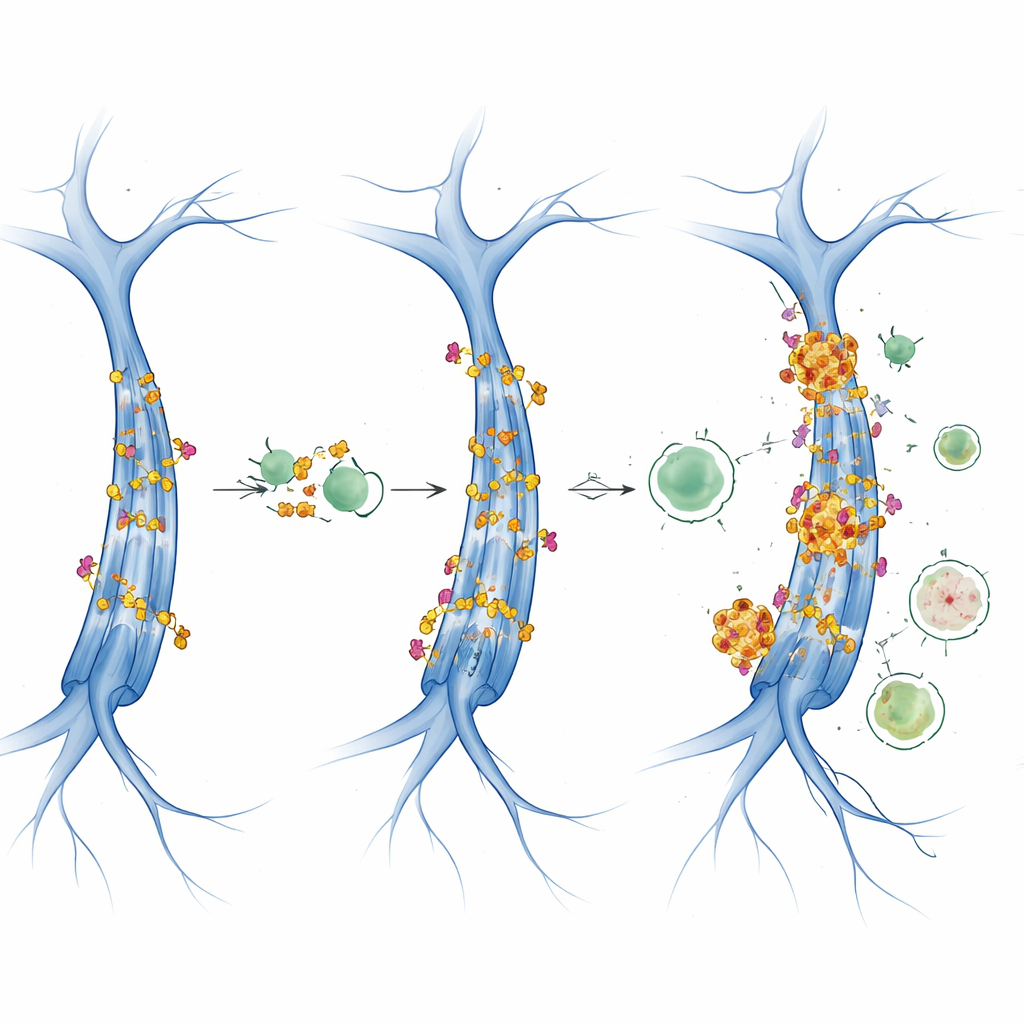
Сигналы, замедляющие клеточное рециркулирование
В исследовании дополнительно рассмотрели двух ключевых регуляторов роста клетки и использования энергии: mTOR и AMPK. При высокой активности mTOR аутофагия обычно подавляется, тогда как AMPK стимулирует её при энергетическом стрессе. В этих мышах с тау активность AMPK в целом оставалась стабильной независимо от возраста и пола, но сигналы, связанные с mTOR, менялись в зависимости от возраста и пола. Данные указывают на подавление аутофагии, опосредованное mTOR, пересекающееся с механизмом ацетилирования. У самок рост CBP/p300 и ацетилированного тау совпадал с маркерами нарушенного аутофагического потока, что предполагает петлю положительной обратной связи: производится больше ацетилированного тау, а одновременно система его удаления становится менее эффективной, позволяя токсичным кластерам тау накапливаться.
Что это значит для понимания и лечения болезни
Для неспециалистов ключевая мысль в том, что мужской и женский мозг по‑разному обращаются с одним и тем же патологическим белком в ходе старения. В этой «очеловеченной» модели тау самки особенно склонны к добавлению ацетильной метки на тау, что вызвано повышенной активностью определённых ферментов и сопровождается ослаблением внутриклеточного рециркуливания. У самцов, напротив, больше изменений связано с фосфорилированием и иными модификациями путей очистки белков. Хотя работа выполнена на мышах и с относительно небольшими группами животных, она поддерживает идею, что ацетилирование — критический, чувствительный к полу этап в накоплении тау. Это делает ферменты, связанные с ацетилированием, и регуляторы аутофагии привлекательными целями для терапий, адаптированных к биологическому полу, с долгосрочной целью замедления или предотвращения дегенерации мозга, вызванной тау.
Цитирование: Sabir, U., Csubak, B.A., Ilchenko, S. et al. Sex-specific effects of acetylation on tauopathy in aging htau mice. Sci Rep 16, 11862 (2026). https://doi.org/10.1038/s41598-026-41691-0
Ключевые слова: ацетилирование тау, половые различия, аутопфагия, болезнь Альцгеймера, нейродегенерация