Clear Sky Science · zh
M $$\vphantom{0}^2$$ DGAT:基于多视角多尺度动态图注意力网络(GAT)利用全血RNA测序数据预测帕金森病(PD)进展
为什么血液可以帮助追踪大脑疾病
帕金森病最为人所知的是震颤和运动障碍,但在这些症状出现之前,大脑内已经发生了多年的隐性损伤。医生迫切需要预测个体帕金森病恶化速度的方法,以便更好地把握治疗时机并实现个体化治疗。本研究表明,一次简单的抽血,结合先进的人工智能系统,可以揭示微弱的分子信号,从而预测帕金森患者在运动和认知方面的变化。
从血液读出大脑的故事
研究者没有直接扫描大脑,而是聚焦于全血RNA测序,这种方法测量血细胞中哪些基因被上调或下调。尽管血液距离大脑很远,但早期研究显示免疫活动和其他全身性过程在某种程度上反映了神经系统的状态。挑战在于这些基因活性读数极其嘈杂:成千上万基因随时间波动,重要的疾病信号很容易被淹没。团队的目标是构建一个模型,能够从这种复杂性中筛选并追踪帕金森在个体患者中的演变。
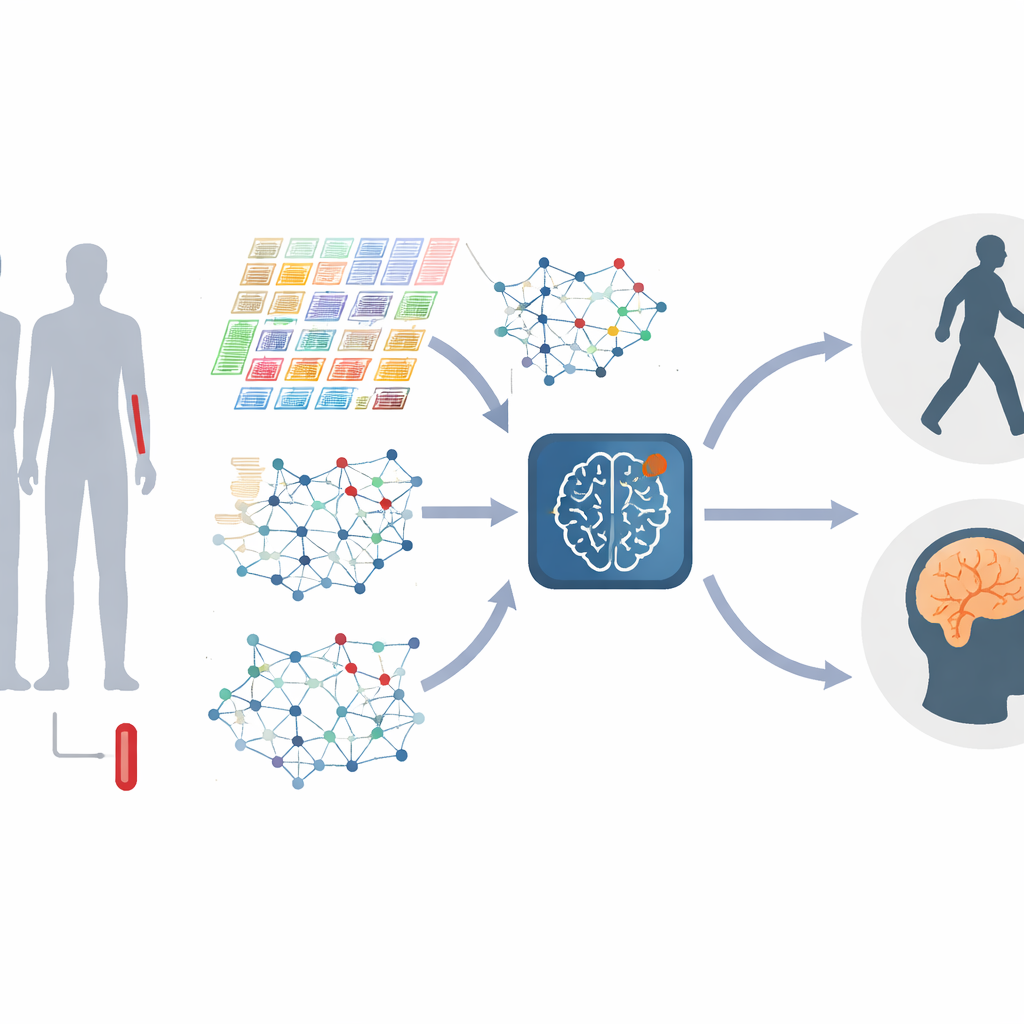
把基因变成“活着”的网络
作者并非将每个基因孤立对待,而是把基因表示为网络,将行为相似的基因连接在一起。随着疾病进展,这些网络会发生变化,某些基因簇——常与免疫反应、蛋白质处理或细胞死亡相关——在重要性上放大或缩小。研究在全局层面构建这些“基因图”,以捕捉整体结构,同时在局部层面关注紧密相关的基因模块。通过跨多尺度合并信息,模型能检测到基因相互作用中的细微失调,这些失调可能标志着不同阶段或类型的帕金森病。
追踪疾病随时间的演变,而不仅仅是快照
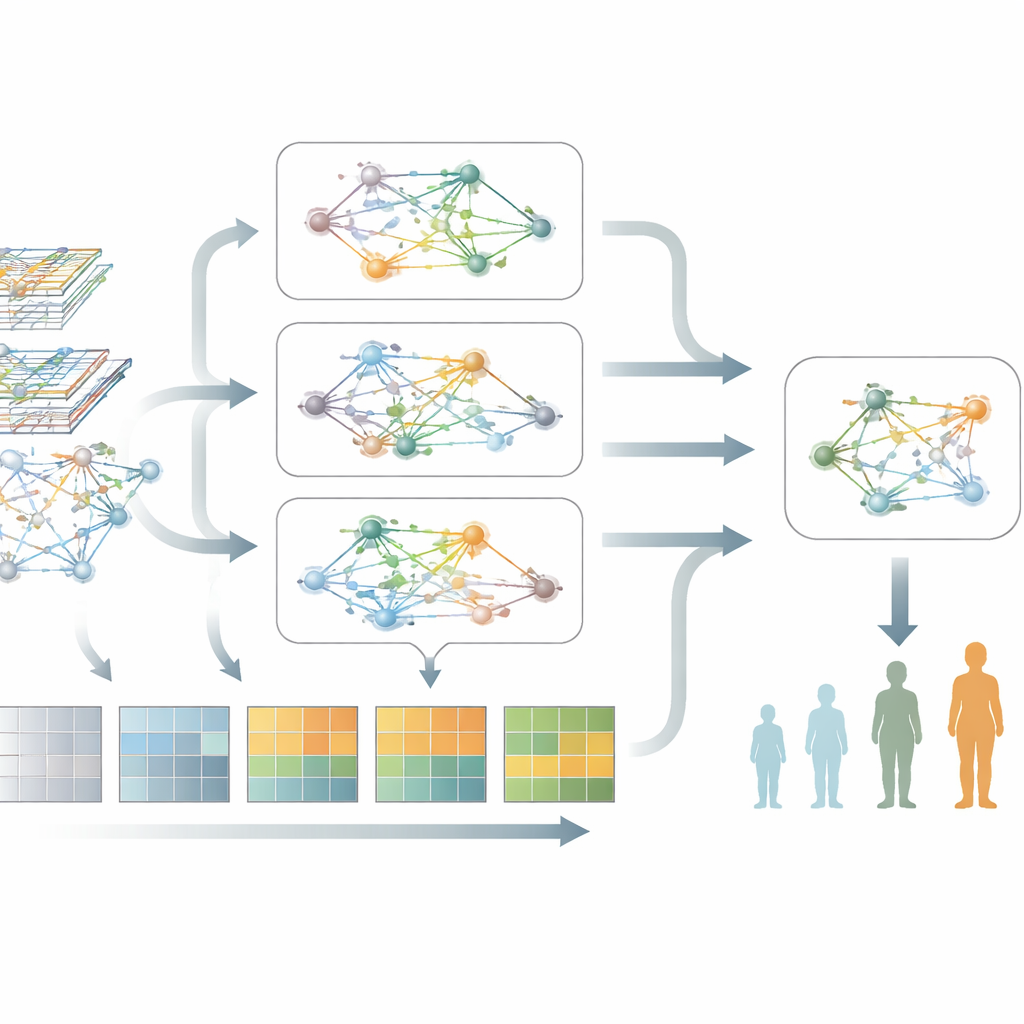
帕金森病不是静止的,因此模型也需要理解变化。为此,研究者输入了来自同一患者在多个门诊随访时点的重复血样,将每位患者的数据变成一部短片而不是一张照片。系统的一部分关注基因活性随时间的升降,学习哪些时间模式最重要并滤除随机波动。另一部分则关注基因网络本身如何随着疾病进展而重构。一个专门的“动态图注意力”引擎随后学习在这些演变的网络中,哪些连接最能区分不同的疾病阶段。
将两种视角融合为单一图景
这项新方法的核心,称为M2DGAT,是将两种视角——基因活性的时间变化和基因网络结构的变化——组合成每位患者和每个时点的联合表示。模型并非简单地把两类数据堆叠在一起,而是使用巧妙的数学方法将它们融合,捕捉“何时”与“如何”出现基因失常之间的复杂相互作用。生成的指纹随后与标准临床量表相关联:用于运动问题的Hoehn和Yahr量表以及用于认知和记忆的蒙特利尔认知评估(MoCA)。在两个大型帕金森队列中,该方法在分级疾病阶段和预测认知评分方面,持续优于若干领先的深度学习方法。
模型揭示的帕金森生物学线索
除了预测能力外,模型还凸显出与帕金森病恶化最强相关的基因组和通路。当作者对这些基因进行检验时,发现重复出现的信号指向蛋白质生成与处理受损、慢性免疫激活以及与程序性细胞死亡和细胞应激相关的通路。值得注意的是,这些生物学主题在两个独立患者群中都出现,表明模型捕捉到的是稳健的、与疾病相关的生物学特征,而非随机模式。这种基于网络的视角有助于将血液标志物与正在损害神经元的底层过程联系起来。
从复杂代码到更清晰的预测
通俗地说,这项工作表明,可以将血液基因活性的复杂混杂信息转化为紧凑且易读的帕金森进展指纹。通过同时考察基因随时间的波动和它们在不断变化的网络中的相互作用,M2DGAT系统能够比现有工具更准确地评估运动和认知衰退。虽然在用于临床决策前仍需更多验证,但该方法指向了一个未来:借助复杂的基于网络的人工智能解读,常规血液检测可能在严重症状出现很久之前就帮助医生预测帕金森的病程并定制治疗方案。
引用: Wei, Z., Zeqi, X., Chenjun, W. et al. M\(\vphantom{0}^2\)DGAT: Multi-view multi-scale dynamic graph attention network(GAT) based prediction of Parkinson’s disease(PD) progression using whole-blood RNA sequencing data. Sci Rep 16, 11777 (2026). https://doi.org/10.1038/s41598-026-40636-x
关键词: 帕金森病, 血液转录组学, 图神经网络, 疾病进展, 精准医学