Clear Sky Science · ru
M $$\vphantom{0}^2$$ DGAT: Многовидовая многошкальная динамическая сеть внимания на графах (GAT) для прогнозирования прогрессирования болезни Паркинсона (БП) с использованием данных секвенирования РНК цельной крови
Почему кровь может помочь отслеживать заболевания мозга
Болезнь Паркинсона наиболее известна тремором и двигательными нарушениями, но к моменту появления этих симптомов в мозге уже произошли годы скрытого повреждения. Врачам срочно нужны способы прогнозировать, с какой скоростью у человека будет прогрессировать Паркинсон, чтобы лучше подбирать и вовремя назначать лечение. В этом исследовании показано, что простое взятие крови в сочетании с продвинутой системой искусственного интеллекта может выявить тонкие молекулярные сигналы, предсказывающие как изменения в движении, так и когнитивные нарушения у пациентов с Паркинсоном.
Чтение истории мозга по крови
Вместо прямого сканирования мозга исследователи сосредоточились на секвенировании РНК цельной крови, которое измеряет, какие гены в клетках крови включены или выключены. Хотя кровь далека от мозга, предыдущие работы показали, что иммунная активность и другие системные процессы отражают происходящее в нервной системе. Проблема в том, что эти показатели активности генов чрезвычайно шумные: десятки тысяч генов изменяют уровень экспрессии во времени, и важные сигналы болезни легко могут быть заглушены. Команда поставила цель построить модель, способную просеять эту сложность и отслеживать, как Паркинсон развивается у отдельных пациентов.
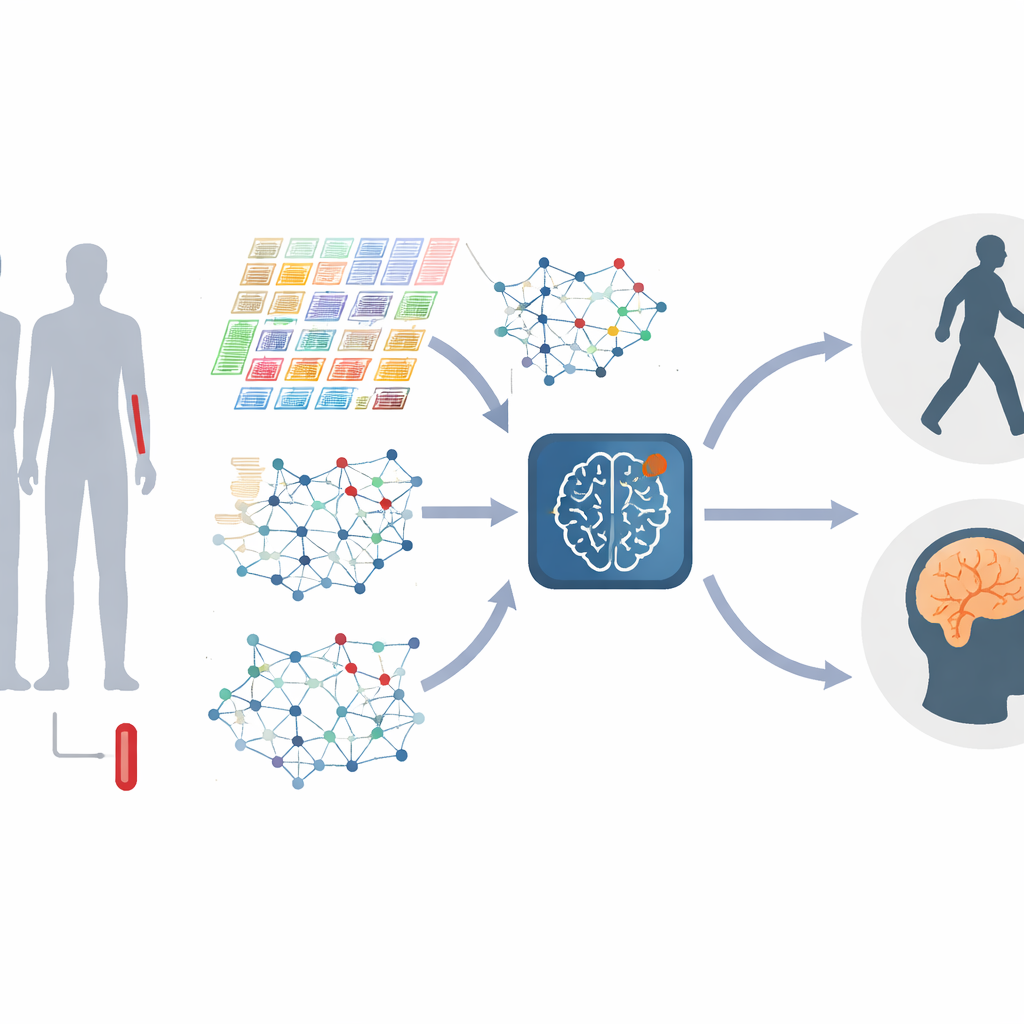
Преобразование генов в живые сети
Вместо того чтобы рассматривать каждый ген по отдельности, авторы представляют гены в виде сети, где между собой связаны гены с похожим поведением. Эти сети меняются по мере прогрессирования болезни: кластеры генов — часто связанные с иммунным ответом, обработкой белков или программируемой гибелью клеток — увеличиваются или уменьшают свою значимость. Исследование строит такие «графы генов» как на глобальном уровне, фиксируя общую структуру, так и на локальном уровне, сосредотачиваясь на тесно связанных модулях родственных генов. Комбинируя информацию на разных масштабах, модель может обнаруживать тонкие искажения во взаимодействиях генов, которые могут отмечать разные стадии или типы Паркинсона.
Отслеживание болезни во времени, а не только по снимкам
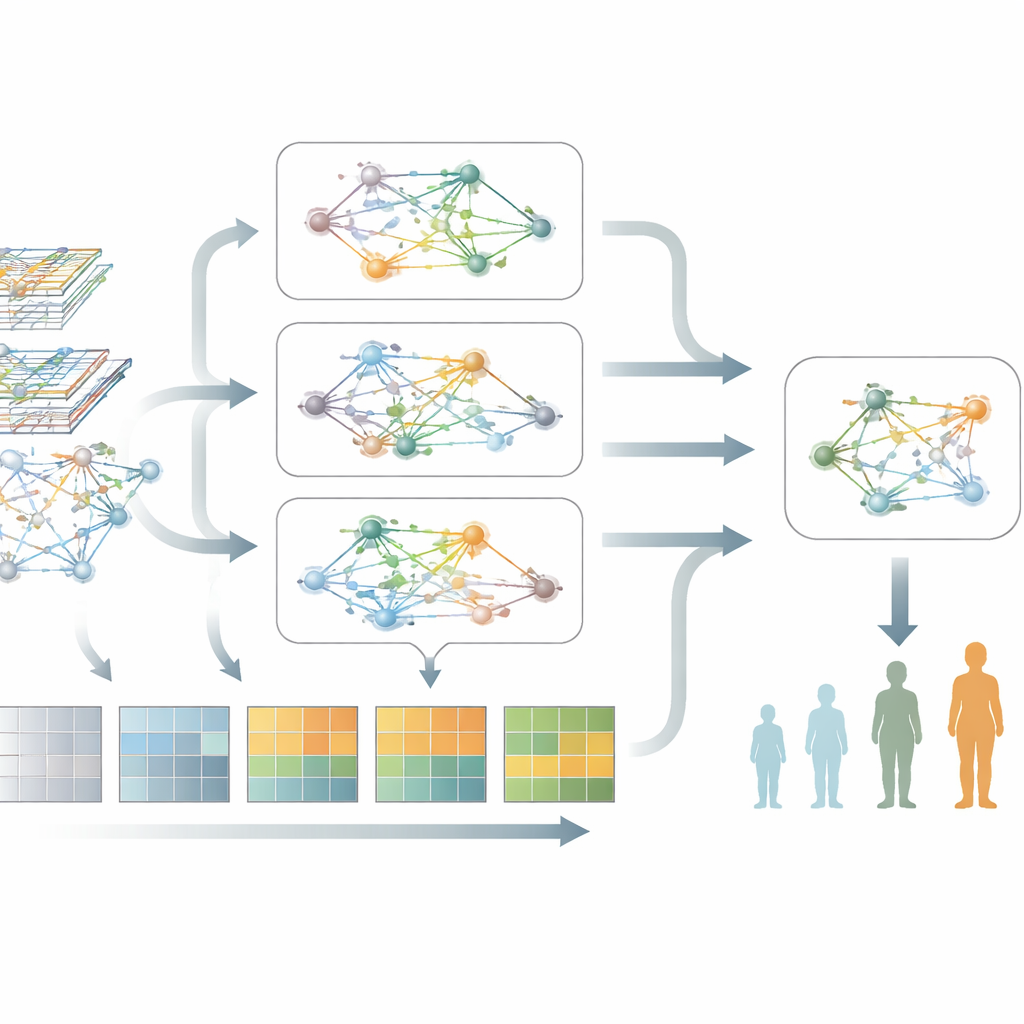
Паркинсон не стоит на месте, поэтому модель также должна понимать изменения. Для этого исследователи используют повторные образцы крови от одних и тех же людей, взятые на нескольких визитах в клинику, превращая данные каждого пациента в короткий фильм, а не в единичное фото. Одна часть их системы фокусируется на том, как уровни активности генов повышаются и понижаются со временем, изучая, какие временные паттерны имеют значение и отфильтровывая случайные колебания. Другая часть сосредоточена на том, как сами генетические сети перестраиваются по мере прогрессирования болезни. Специализированный механизм «динамического внимания на графах» затем учится выделять те связи в этих меняющихся сетях, которые лучше всего различают стадии заболевания.
Слияние двух взглядов в единую картину
Суть нового метода, названного M2DGAT, в том, что он объединяет эти два взгляда — временные изменения активности генов и изменение структуры генетических сетей — в единое совместное представление для каждого пациента и временной точки. Вместо простого сложения двух типов данных модель использует продуманный математический приём для их слияния, улавливая сложные взаимодействия между «когда» и «как» гены ведут себя ненормально. Полученные сигнатуры затем сопоставляют со стандартными клиническими мерами: шкалой Хойна и Яра для двигательных нарушений и Монреальской шкалой когнитивной оценки для мышления и памяти. На двух больших когортных выборках пациентов с Паркинсоном этот подход последовательно превосходил несколько ведущих методов глубокого обучения в задачах классификации стадии болезни и прогнозирования когнитивных показателей.
Что модель раскрывает о биологии Паркинсона
Помимо прогнозирования, модель выделяет группы генов и пути, наиболее тесно связанные с усугублением болезни Паркинсона. При изучении этих генов авторы обнаружили повторяющиеся сигналы, указывающие на нарушения синтеза и обработки белков, хроническую активацию иммунной системы и пути, связанные с программируемой гибелью клеток и клеточным стрессом. Поразительно, что эти биологические темы проявлялись в двух независимых группах пациентов, что говорит о том, что модель улавливает устойчивую, связанную с заболеванием биологию, а не случайные паттерны. Такой сетевой взгляд помогает связать маркеры в крови с основными процессами, повреждающими нейроны.
От сложного кода к более точным прогнозам
Проще говоря, эта работа показывает, что можно превратить ошеломляющую сложность активности генов в крови в компактный, читаемый отпечаток прогрессирования Паркинсона. Одновременное рассмотрение того, как гены колеблются во времени, и как они взаимодействуют в меняющихся сетях позволяет системе M2DGAT точнее оценивать как двигательное, так и когнитивное снижение по сравнению с существующими инструментами. Хотя перед внедрением в клинику потребуется дополнительная валидация, подход указывает на будущее, где рутинный анализ крови, интерпретируемый с помощью сложного сетевого ИИ, сможет помочь врачам прогнозировать ход болезни Паркинсона и персонализировать лечение задолго до появления выраженных симптомов.
Цитирование: Wei, Z., Zeqi, X., Chenjun, W. et al. M\(\vphantom{0}^2\)DGAT: Multi-view multi-scale dynamic graph attention network(GAT) based prediction of Parkinson’s disease(PD) progression using whole-blood RNA sequencing data. Sci Rep 16, 11777 (2026). https://doi.org/10.1038/s41598-026-40636-x
Ключевые слова: болезнь Паркинсона, транскриптомика крови, графовые нейронные сети, прогрессирование заболевания, персонализированная медицина