Clear Sky Science · pt
M $$\vphantom{0}^2$$ DGAT: Rede de atenção dinâmica por grafos multiescala e multivisual (GAT) para previsão da progressão da doença de Parkinson (DP) usando dados de sequenciamento de RNA de sangue total
Por que o sangue pode ajudar a acompanhar doenças cerebrais
A doença de Parkinson é mais conhecida por seus tremores e problemas de movimento, mas quando esses sintomas aparecem, já ocorreram anos de dano oculto no cérebro. Médicos precisam com urgência de maneiras de prever quão rápido o Parkinson de uma pessoa irá piorar, para que os tratamentos possam ser melhor programados e personalizados. Este estudo mostra que uma simples coleta de sangue, combinada a um sistema avançado de inteligência artificial, pode revelar sinais moleculares sutis que preveem tanto alterações motoras quanto cognitivas em pessoas com Parkinson.
Lendo a história do cérebro a partir do sangue
Em vez de escanear o cérebro diretamente, os pesquisadores concentraram-se no sequenciamento de RNA de sangue total, que mede quais genes estão aumentados ou reduzidos nas células sanguíneas. Embora o sangue esteja longe do cérebro, trabalhos anteriores demonstraram que a atividade imune e outros processos sistêmicos espelham o que acontece no sistema nervoso. O desafio é que essas leituras de atividade gênica são extremamente ruidosas: dezenas de milhares de genes flutuam ao longo do tempo, e sinais importantes da doença podem ser facilmente ofuscados. A equipe buscou construir um modelo capaz de peneirar essa complexidade e acompanhar como o Parkinson se desenvolve em pacientes individuais.
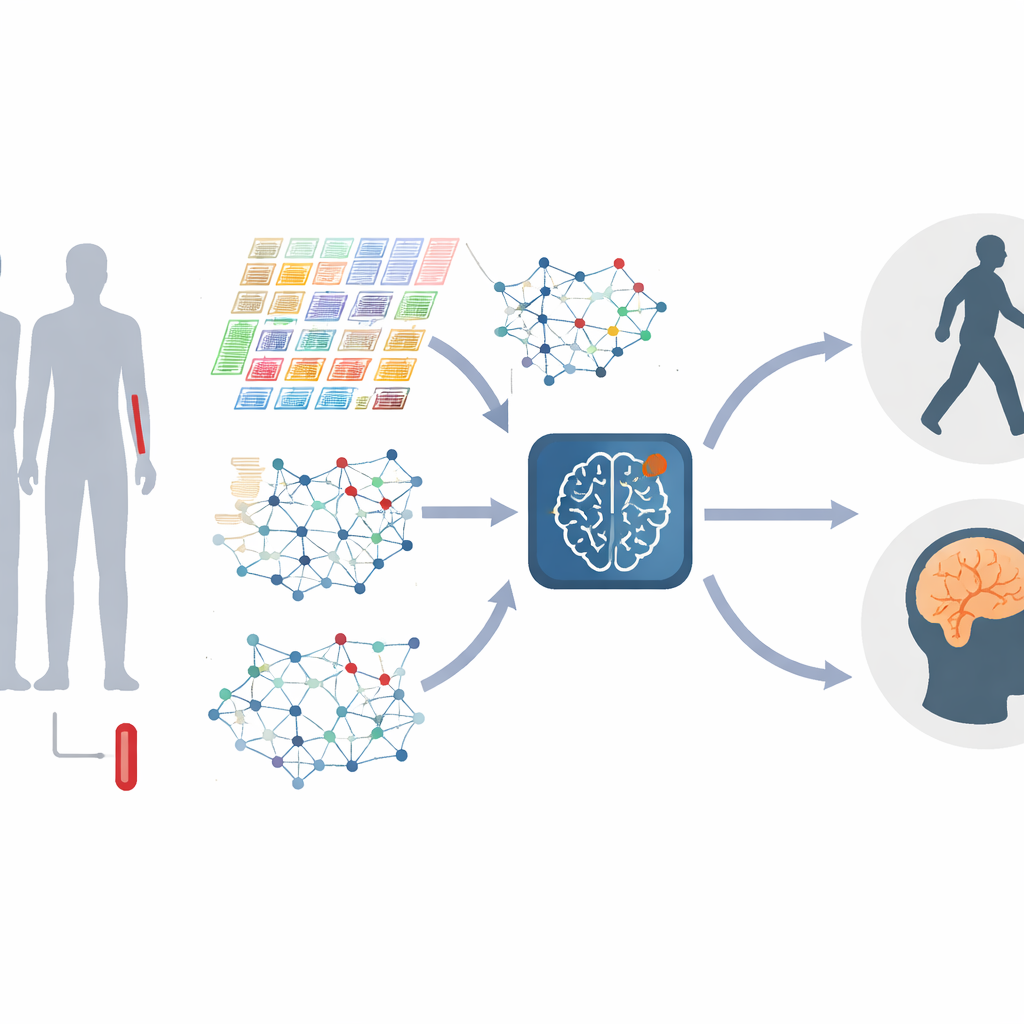
Transformando genes em redes vivas
Em vez de tratar cada gene separadamente, os autores representam os genes como uma rede, onde genes que se comportam de forma semelhante estão conectados. Essas redes mudam à medida que a doença progride, com grupos de genes — frequentemente ligados a respostas imunes, ao manejo de proteínas ou à morte celular — aumentando ou diminuindo em importância. O estudo constrói esses “grafos gênicos” tanto em um nível global, capturando a estrutura geral, quanto em um nível local, focando em módulos bem conectados de genes relacionados. Ao combinar informações em várias escalas, o modelo pode detectar distorções finas em como os genes interagem, que podem marcar diferentes estágios ou tipos de Parkinson.
Acompanhando a doença ao longo do tempo, não apenas em instantâneos
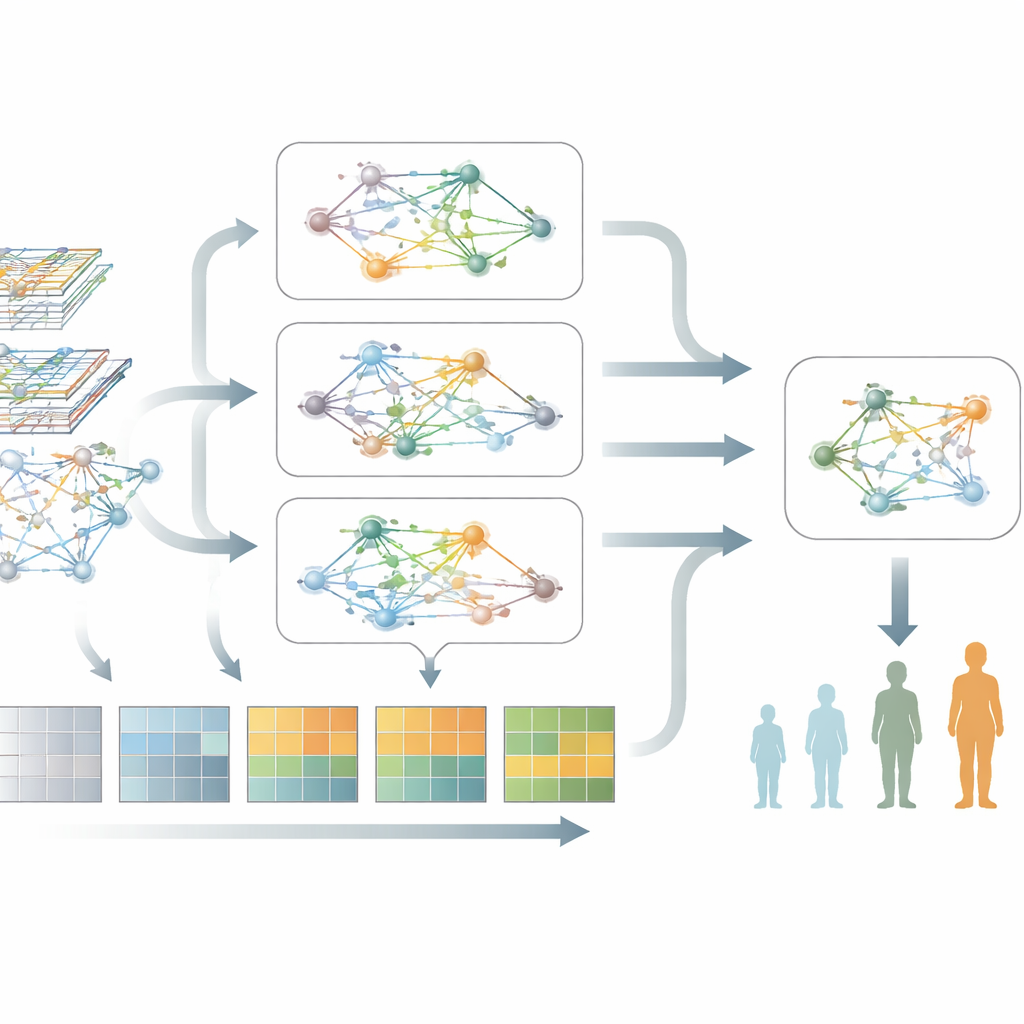
O Parkinson não permanece estático, portanto o modelo também precisa compreender a mudança. Para isso, os pesquisadores alimentam o sistema com amostras de sangue repetidas das mesmas pessoas em várias visitas clínicas, transformando os dados de cada pessoa em um pequeno filme em vez de uma única foto. Uma parte do sistema foca em como os níveis de atividade gênica sobem e descem ao longo do tempo, aprendendo quais padrões temporais são mais relevantes e filtrando flutuações aleatórias. Outra parte focaliza como as próprias redes gênicas se remodelam à medida que a doença avança. Um mecanismo especializado de “atenção dinâmica por grafos” aprende então quais conexões nessas redes em evolução distinguem melhor um estágio da doença de outro.
Misturando duas visões em uma única imagem
O cerne do novo método, chamado M2DGAT, é que ele combina essas duas visões — mudanças temporais na atividade gênica e transformação da estrutura da rede gênica — em uma representação conjunta para cada paciente e ponto temporal. Em vez de simplesmente empilhar os dois tipos de dados, o modelo usa um recurso matemático engenhoso para fundi-los, capturando interações complexas entre o “quando” e o “como” os genes se comportam mal. As assinaturas resultantes são então vinculadas a medidas clínicas padrão: a escala de Hoehn e Yahr para problemas de movimento e o Montreal Cognitive Assessment para funções cognitivas e memória. Em dois grandes coortes de Parkinson, essa abordagem superou de forma consistente vários métodos de deep learning líderes na classificação do estágio da doença e na previsão de pontuações cognitivas.
O que o modelo revela sobre a biologia do Parkinson
Além da previsão, o modelo destaca grupos de genes e vias que estão mais fortemente associados ao agravamento do Parkinson. Quando os autores examinaram esses genes, encontraram sinais repetidos apontando para produção e manejo de proteínas perturbados, ativação imune crônica e vias ligadas à morte celular programada e ao estresse celular. Notavelmente, esses temas biológicos apareceram em dois grupos independentes de pacientes, sugerindo que o modelo captura biologia relacionada à doença de forma robusta, e não padrões aleatórios. Esse tipo de visão em nível de rede ajuda a conectar marcadores sanguíneos aos processos subjacentes que danificam os neurônios.
Do código complexo a previsões mais claras
Em termos práticos, este trabalho mostra que é possível transformar a complexidade desconcertante da atividade gênica no sangue em uma impressão digital compacta e legível da progressão do Parkinson. Ao observar simultaneamente como os genes flutuam ao longo do tempo e como eles interagem em redes em mudança, o sistema M2DGAT pode avaliar com mais precisão tanto o declínio motor quanto o cognitivo do que as ferramentas existentes. Embora mais validação seja necessária antes que possa orientar o cuidado clínico, a abordagem aponta para um futuro em que um exame de sangue rotineiro, interpretado por IA sofisticada baseada em redes, poderia ajudar médicos a prever o curso do Parkinson e personalizar tratamentos muito antes do aparecimento de sintomas graves.
Citação: Wei, Z., Zeqi, X., Chenjun, W. et al. M\(\vphantom{0}^2\)DGAT: Multi-view multi-scale dynamic graph attention network(GAT) based prediction of Parkinson’s disease(PD) progression using whole-blood RNA sequencing data. Sci Rep 16, 11777 (2026). https://doi.org/10.1038/s41598-026-40636-x
Palavras-chave: Doença de Parkinson, transcritômica sanguínea, redes neurais por grafos, progressão da doença, medicina personalizada