Clear Sky Science · sv
M $$\vphantom{0}^2$$ DGAT: Multi-view multi-scale dynamic graph attention network (GAT) baserat förutsägelse av Parkinsons sjukdoms (PD) progression med hjälp av helblods-RNA-sekvenseringsdata
Varför blod kan hjälpa till att spåra hjärnsjukdom
Parkinsons sjukdom är mest känd för sina skakningar och rörelsestörningar, men när dessa symtom uppträder har hjärnan redan utsatts för år av dold skada. Läkare behöver snabbt metoder för att förutse hur snabbt en persons Parkinson kommer att förvärras, så att behandlingar kan sättas in och anpassas bättre. Denna studie visar att ett enkelt blodprov, i kombination med ett avancerat artificiellt intelligenssystem, kan avslöja subtila molekylära signaler som förutsäger både rörelse- och kognitiva förändringar hos personer med Parkinsons.
Att läsa hjärnans berättelse från blodet
I stället för att skanna hjärnan direkt fokuserade forskarna på helblods-RNA-sekvensering, som mäter vilka gener som är upp- eller nedreglerade i blodceller. Även om blodet ligger långt från hjärnan har tidigare arbete visat att immunaktivitet och andra kroppsomfattande processer speglar vad som händer i nervsystemet. Utmaningen är att dessa genaktivitetsavläsningar är extremt brusiga: tiotusentals gener varierar över tid, och viktiga sjukdomssignaler kan enkelt dränkas ut. Teamet gav sig därför i kast med att bygga en modell som kan sålla igenom denna komplexitet och följa hur Parkinson utvecklas hos individer.
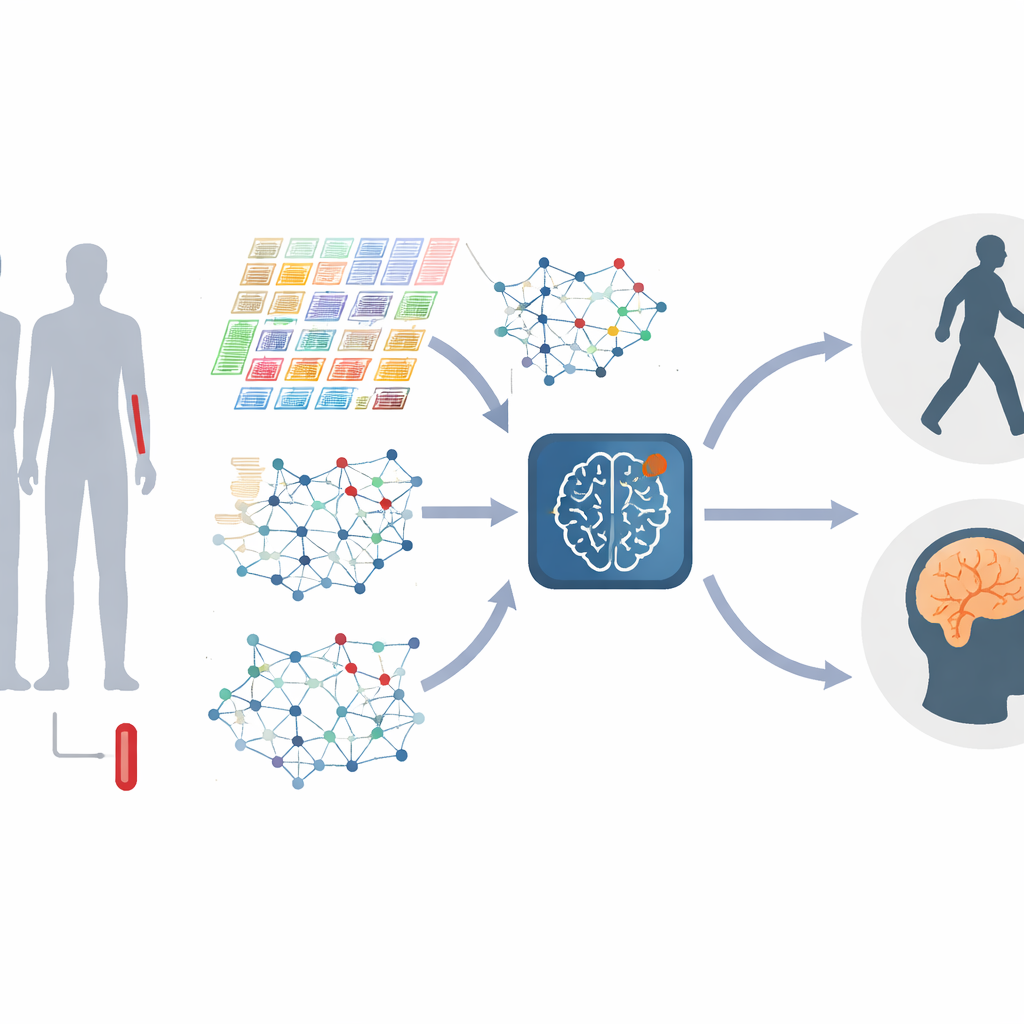
Att förvandla gener till levande nätverk
I stället för att behandla varje gen separat representerar författarna gener som ett nätverk, där gener som beter sig likartat länkas ihop. Dessa nätverk förändras när sjukdomen fortskrider, med kluster av gener—ofta kopplade till immunsvar, proteinhantering eller celldöd—som ökar eller minskar i betydelse. Studien bygger dessa ”gengrafer” både på global nivå, för att fånga den övergripande strukturen, och på lokal nivå, med fokus på tätt sammanbundna moduler av relaterade gener. Genom att kombinera information över flera skalor kan modellen upptäcka finkorniga störningar i hur gener interagerar, vilket kan markera olika stadier eller typer av Parkinsons.
Följa sjukdomen över tid, inte bara i stillbilder
Parkinsons står inte stilla, så modellen måste också förstå förändring. För att göra detta matar forskarna in upprepade blodprover från samma personer vid flera klinikbesök och förvandlar varje persons data till en kort film snarare än ett enda fotografi. En del av systemet fokuserar på hur genaktivitetsnivåer stiger och faller över tid, lär sig vilka tidsmässiga mönster som är viktigast och filtrerar bort slumpmässiga fluktuationer. En annan del fokuserar på hur gengraferna själva omformas när sjukdomen framskrider. En specialiserad ”dynamisk graph attention”-motor lär sig sedan vilka kopplingar i dessa förändrade nätverk som bäst skiljer ett sjukdomsstadium från ett annat.
Att blanda två vyer till en bild
Kärnan i den nya metoden, kallad M2DGAT, är att den kombinerar dessa två vyer—temporal förändring i genaktivitet och skiftande gengrafstruktur—till en gemensam representation för varje patient och tidpunkt. I stället för att bara stapla de två datatyperna använder modellen ett smart matematiskt trick för att smälta samman dem och fånga komplexa interaktioner mellan ”när” och ”hur” gener beter sig felaktigt. De resulterande signaturerna kopplas sedan till standardiserade kliniska mått: Hoehn och Yahr-skalan för rörelsestörningar och Montreal Cognitive Assessment för kognition och minne. I två stora Parkinsons-kohorter överträffade denna metod konsekvent flera ledande djupa inlärningsmetoder vid klassificering av sjukdomsstadium och vid förutsägelse av kognitiva poäng.
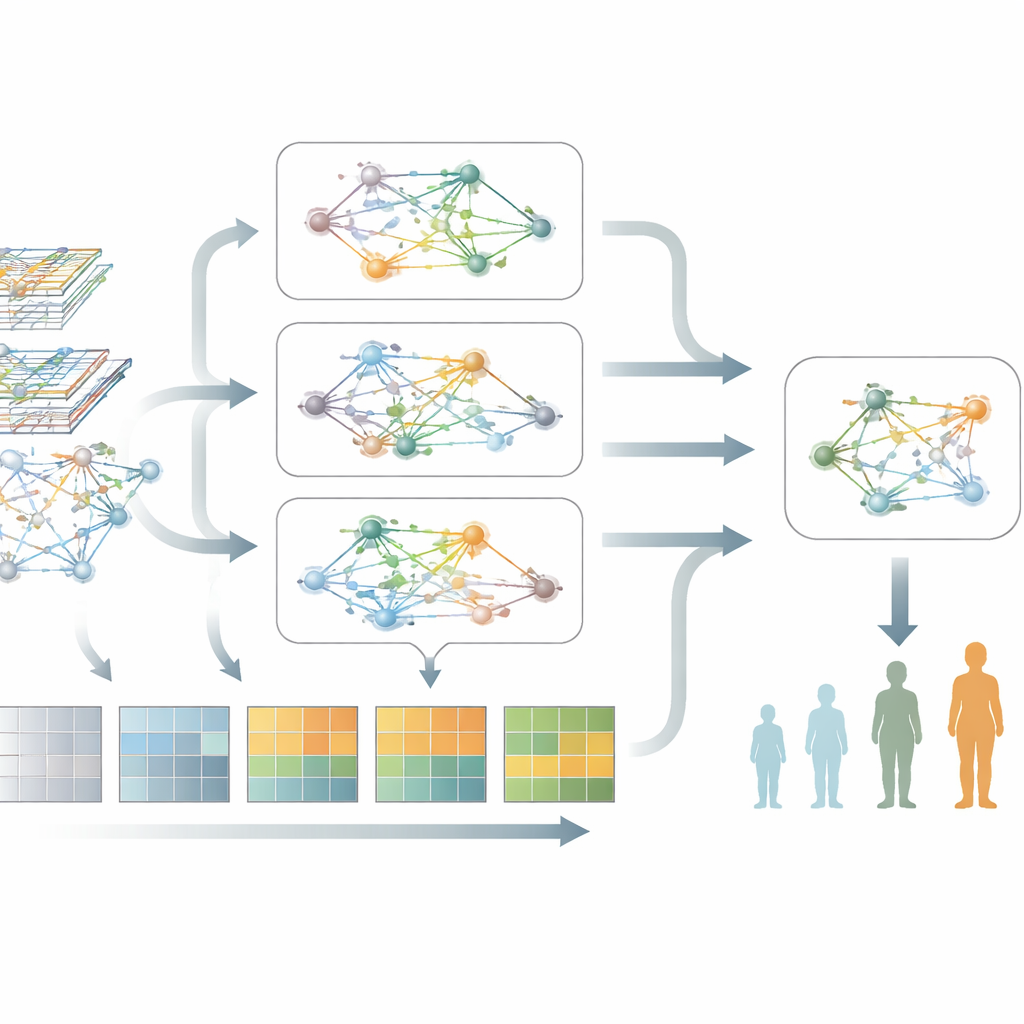
Vad modellen avslöjar om Parkinsons biologi
Utöver prediktion framhäver modellen grupper av gener och vägar som starkast associeras med försämrad Parkinsons. När författarna granskade dessa gener fann de återkommande signaler som pekade mot störd proteinproduktion och -hantering, kronisk immunaktivering samt vägar kopplade till programmerad celldöd och cellulär stress. Anmärkningsvärt nog framträdde dessa biologiska teman i två oberoende patientgrupper, vilket tyder på att modellen fångar robust, sjukdomsrelaterad biologi snarare än slumpmässiga mönster. Denna typ av nätverksnivåvy hjälper till att koppla blodmarkörer tillbaka till de underliggande processer som skadar neuroner.
Från komplex kod till tydligare prognoser
Enkelt uttryckt visar detta arbete att det är möjligt att omvandla den förvirrande komplexiteten i blodets genaktivitet till ett kompakt, läsbart fingeravtryck för Parkinsons progression. Genom att samtidigt betrakta hur gener fluktuerar över tid och hur de interagerar i skiftande nätverk kan M2DGAT-systemet mer exakt bedöma både motorisk och kognitiv försämring än befintliga verktyg. Även om ytterligare validering krävs innan metoden kan styra vård pekar angreppssättet mot en framtid där ett rutinmässigt blodprov, tolkas genom sofistikerad nätverksbaserad AI, kan hjälpa läkare att förutse Parkinsons förlopp och skräddarsy behandlingar långt innan svåra symtom uppträder.
Citering: Wei, Z., Zeqi, X., Chenjun, W. et al. M\(\vphantom{0}^2\)DGAT: Multi-view multi-scale dynamic graph attention network(GAT) based prediction of Parkinson’s disease(PD) progression using whole-blood RNA sequencing data. Sci Rep 16, 11777 (2026). https://doi.org/10.1038/s41598-026-40636-x
Nyckelord: Parkinsons sjukdom, blodtranskriptomik, grafneuronätverk, sjukdomsprogression, precision medicine