Clear Sky Science · nl
M $$\vphantom{0}^2$$ DGAT: Multi-view multi-scale dynamic graph attention network (GAT) gebaseerde voorspelling van de progressie van de ziekte van Parkinson (PD) met behulp van gehele-bloed RNA-sequencinggegevens
Waarom bloed kan helpen bij het volgen van hersenziekte
De ziekte van Parkinson staat het meest bekend om tremoren en bewegingsproblemen, maar tegen de tijd dat deze symptomen zichtbaar worden, heeft er al jaren van verborgen schade in de hersenen plaatsgevonden. Artsen hebben dringend manieren nodig om te voorspellen hoe snel iemands Parkinson zal verslechteren, zodat behandelingen beter getimed en aangepast kunnen worden. Deze studie toont aan dat een eenvoudige bloedafname, gecombineerd met een geavanceerd kunstmatig-intelligentiesysteem, subtiele moleculaire signalen kan onthullen die zowel motorische als cognitieve veranderingen bij mensen met Parkinson voorspellen.
Het verhaal van de hersenen lezen uit bloed
In plaats van de hersenen rechtstreeks te scannen, richtten de onderzoekers zich op gehele-bloed RNA-sequencing, waarmee wordt gemeten welke genen in bloedcellen omhoog- of omlaaggereguleerd zijn. Hoewel bloed ver van de hersenen staat, hebben eerdere studies aangetoond dat immuunactiviteit en andere lichaamsbrede processen weerspiegelen wat er in het zenuwstelsel gebeurt. De uitdaging is dat deze genactiviteitsmetingen extreem lawaaierig zijn: tienduizenden genen fluctueren in de tijd en belangrijke ziekte- signalen kunnen gemakkelijk worden overstemd. Het team wilde een model bouwen dat door deze complexiteit kan zeven en kan volgen hoe Parkinson zich bij individuele patiënten ontwikkelt.
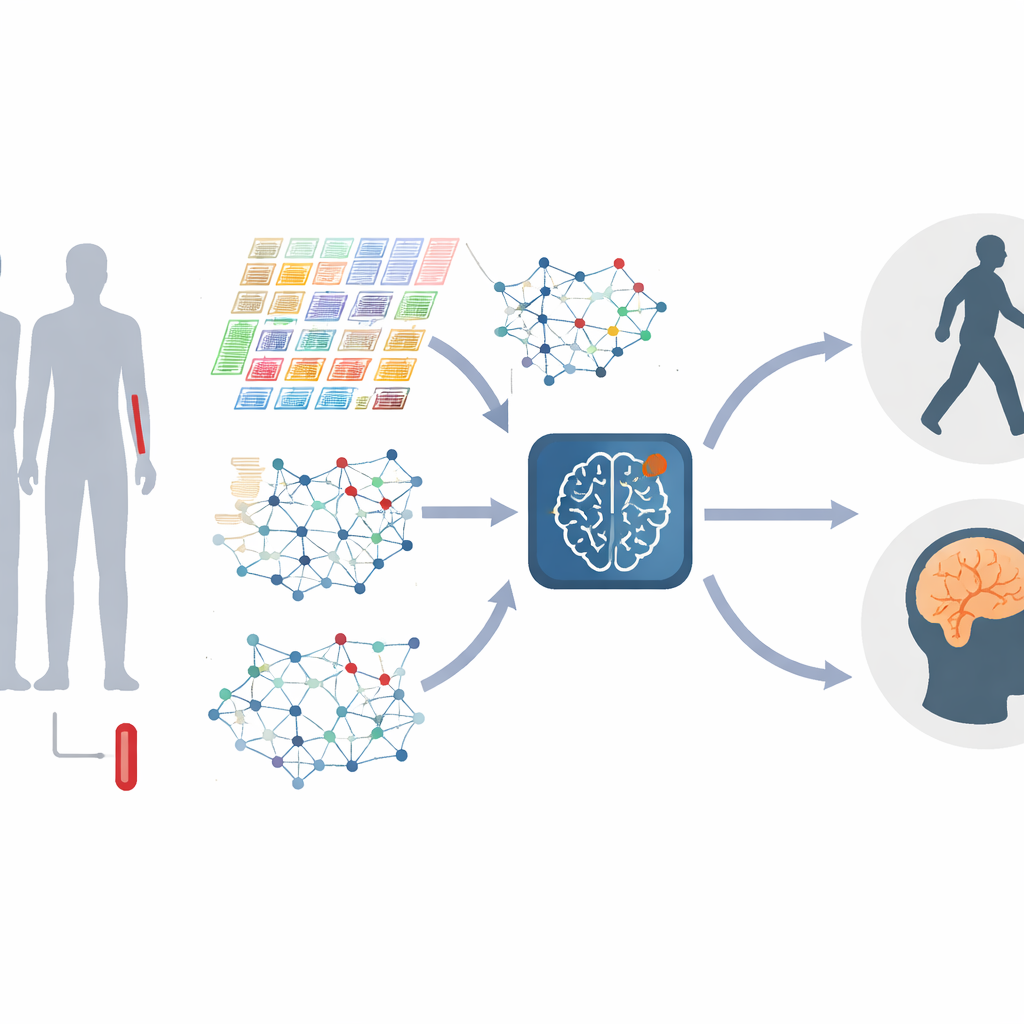
Genen omzetten in levende netwerken
In plaats van elk gen afzonderlijk te behandelen, vertegenwoordigen de auteurs genen als een netwerk, waarbij genen die zich vergelijkbaar gedragen met elkaar verbonden zijn. Deze netwerken veranderen naarmate de ziekte vordert, waarbij clusters van genen—vaak gerelateerd aan immuunresponsen, eiwitbehandeling of celdood—in belang toenemen of afnemen. De studie bouwt deze "gen-grafen" zowel op globaal niveau, die de algemene structuur vastleggen, als op lokaal niveau, gericht op hechte modules van verwante genen. Door informatie over meerdere schalen te combineren, kan het model fijnmazige verstoringen detecteren in hoe genen met elkaar interageren, wat verschillende stadia of typen Parkinson kan markeren.
De ziekte in de tijd volgen, niet alleen in momentopnames
Parkinson staat niet stil, dus het model moet ook verandering begrijpen. Daarom voerden de onderzoekers herhaalde bloedmonsters van dezelfde personen in bij meerdere polikliniekbezoeken en veranderden ze de gegevens van elke persoon in een korte film in plaats van een enkele foto. Een deel van hun systeem richt zich op hoe genactiviteitsniveaus in de tijd stijgen en dalen, leert welke temporele patronen het belangrijkst zijn en filtert toevallige fluctuaties weg. Een ander deel richt zich op hoe de gen-netwerken zelf zich herstructureren naarmate de ziekte vordert. Een gespecialiseerde "dynamic graph attention"-motor leert vervolgens welke verbindingen in deze zich ontwikkelende netwerken het beste onderscheid maken tussen de verschillende ziektefasen.
Twee gezichtspunten samenvoegen tot één beeld
Het hart van de nieuwe methode, M2DGAT genoemd, is dat het deze twee gezichtspunten—temporele veranderingen in genactiviteit en verschuivende gen-netwerkstructuur—combineert tot één gezamenlijke representatie voor elke patiënt en tijdpunt. In plaats van de twee datatypes simpelweg op elkaar te stapelen, gebruikt het model een slimme wiskundige truc om ze te versmelten, waardoor complexe interacties tussen "wanneer" en "hoe" genen zich verkeerd gedragen worden vastgelegd. De resulterende signaturen worden vervolgens gekoppeld aan standaard klinische metingen: de Hoehn en Yahr-schaal voor bewegingsproblemen en de Montreal Cognitive Assessment voor cognitie en geheugen. In twee grote Parkinson-cohorten presteerde deze aanpak consequent beter dan verschillende toonaangevende deep-learningmethoden bij het classificeren van ziektestadia en het voorspellen van cognitieve scores.
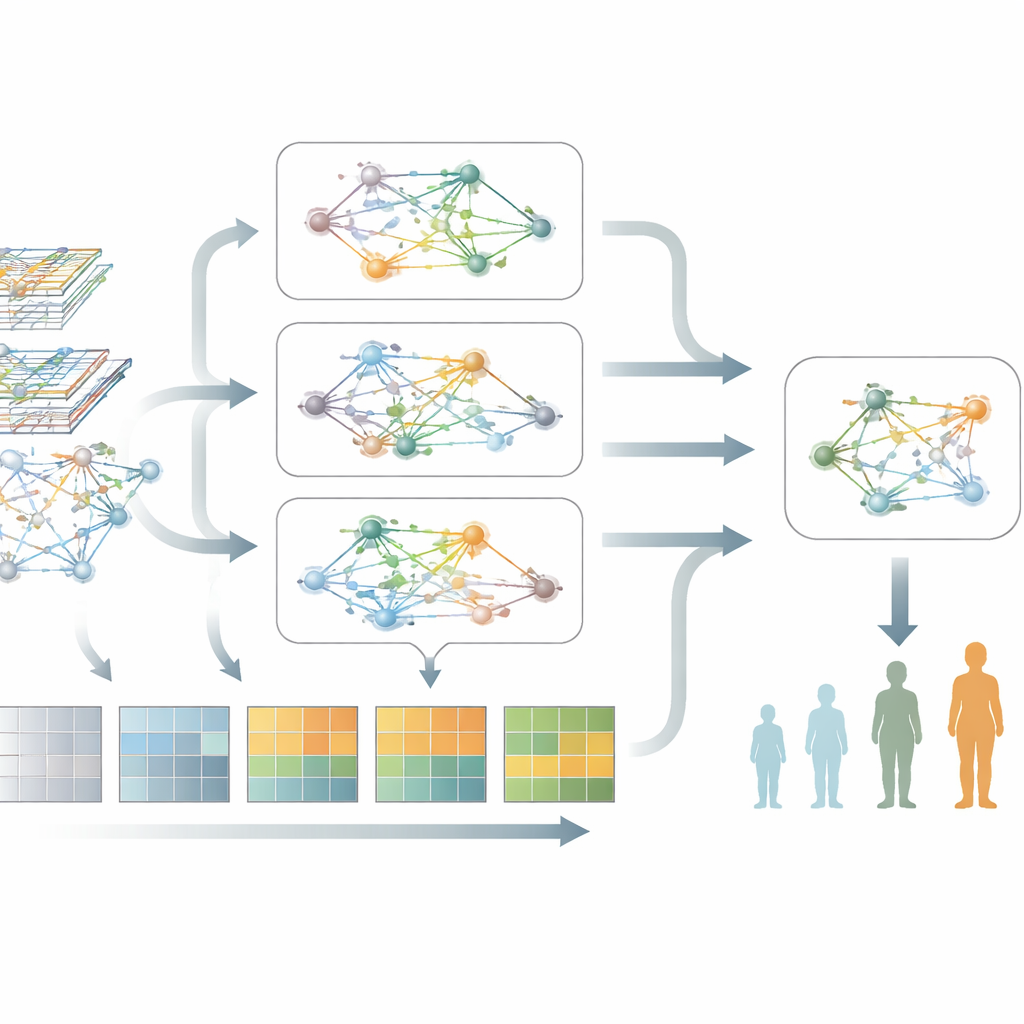
Wat het model onthult over de biologie van Parkinson
Buiten voorspelling benadrukt het model groepen genen en paden die het sterkst geassocieerd zijn met verslechterende Parkinson. Toen de auteurs deze genen onderzochten, vonden ze terugkerende signalen die wezen op verstoorde eiwitproductie en -afhandeling, chronische immuunactivatie en paden die samenhangen met geprogrammeerde celdood en cellulaire stress. Opvallend genoeg verschenen deze biologische thema's in twee onafhankelijke patiëntengroepen, wat suggereert dat het model robuuste, ziektegerelateerde biologie vastlegt in plaats van willekeurige patronen. Dit soort netwerkniveau-inzicht helpt bloedmarkers te koppelen aan de onderliggende processen die neuronen beschadigen.
Van complexe code naar helderdere voorspellingen
Simpel gezegd laat dit werk zien dat het mogelijk is de verwarrende complexiteit van genactiviteit in bloed om te zetten in een compacte, leesbare vingerafdruk van de progressie van Parkinson. Door gelijktijdig te kijken naar hoe genen in de tijd fluctueren en hoe ze in verschuivende netwerken met elkaar interageren, kan het M2DGAT-systeem zowel motorische als cognitieve achteruitgang nauwkeuriger inschatten dan bestaande hulpmiddelen. Hoewel meer validatie nodig is voordat het de zorg kan sturen, wijst de aanpak op een toekomst waarin een routinematig bloedonderzoek, geïnterpreteerd met behulp van geavanceerde netwerkgebaseerde AI, artsen kan helpen het verloop van Parkinson te voorspellen en behandelingen aan te passen lang voordat ernstige symptomen optreden.
Bronvermelding: Wei, Z., Zeqi, X., Chenjun, W. et al. M\(\vphantom{0}^2\)DGAT: Multi-view multi-scale dynamic graph attention network(GAT) based prediction of Parkinson’s disease(PD) progression using whole-blood RNA sequencing data. Sci Rep 16, 11777 (2026). https://doi.org/10.1038/s41598-026-40636-x
Trefwoorden: Ziekte van Parkinson, transcriptomica van bloed, graaf neurale netwerken, ziekteprogressie, precisiemedicine