Clear Sky Science · fr
M $$\vphantom{0}^2$$ DGAT : réseau d’attention de graphe dynamique multi-vues et multi-échelles (GAT) pour la prédiction de la progression de la maladie de Parkinson (MP) à partir de données d’ARN en sang total
Pourquoi le sang peut aider à suivre une maladie cérébrale
La maladie de Parkinson est surtout connue pour ses tremblements et ses troubles du mouvement, mais lorsque ces symptômes apparaissent, des années de dommages silencieux se sont déjà produits dans le cerveau. Les cliniciens ont un besoin urgent de moyens pour prévoir la vitesse à laquelle la maladie d’une personne va s’aggraver afin d’adapter et de mieux chronométrer les traitements. Cette étude montre qu’un simple prélèvement sanguin, associé à un système d’intelligence artificielle avancé, peut révéler des signaux moléculaires subtils qui prédisent tant les altérations motrices que cognitives chez des patients parkinsoniens.
Lire l’histoire du cerveau à partir du sang
Plutôt que de scanner directement le cerveau, les chercheurs se sont concentrés sur le séquençage de l’ARN en sang total, qui mesure quels gènes sont activés ou réprimés dans les cellules sanguines. Bien que le sang soit loin du cerveau, des travaux antérieurs ont montré que l’activité immunitaire et d’autres processus systémiques reflètent ce qui se passe dans le système nerveux. Le défi est que ces profils d’activité génique sont extrêmement bruyants : des dizaines de milliers de gènes fluctuent au fil du temps, et les signaux importants liés à la maladie peuvent facilement être noyés. L’équipe a donc cherché à construire un modèle capable de trier cette complexité et de suivre la façon dont la maladie de Parkinson évolue chez chaque patient.
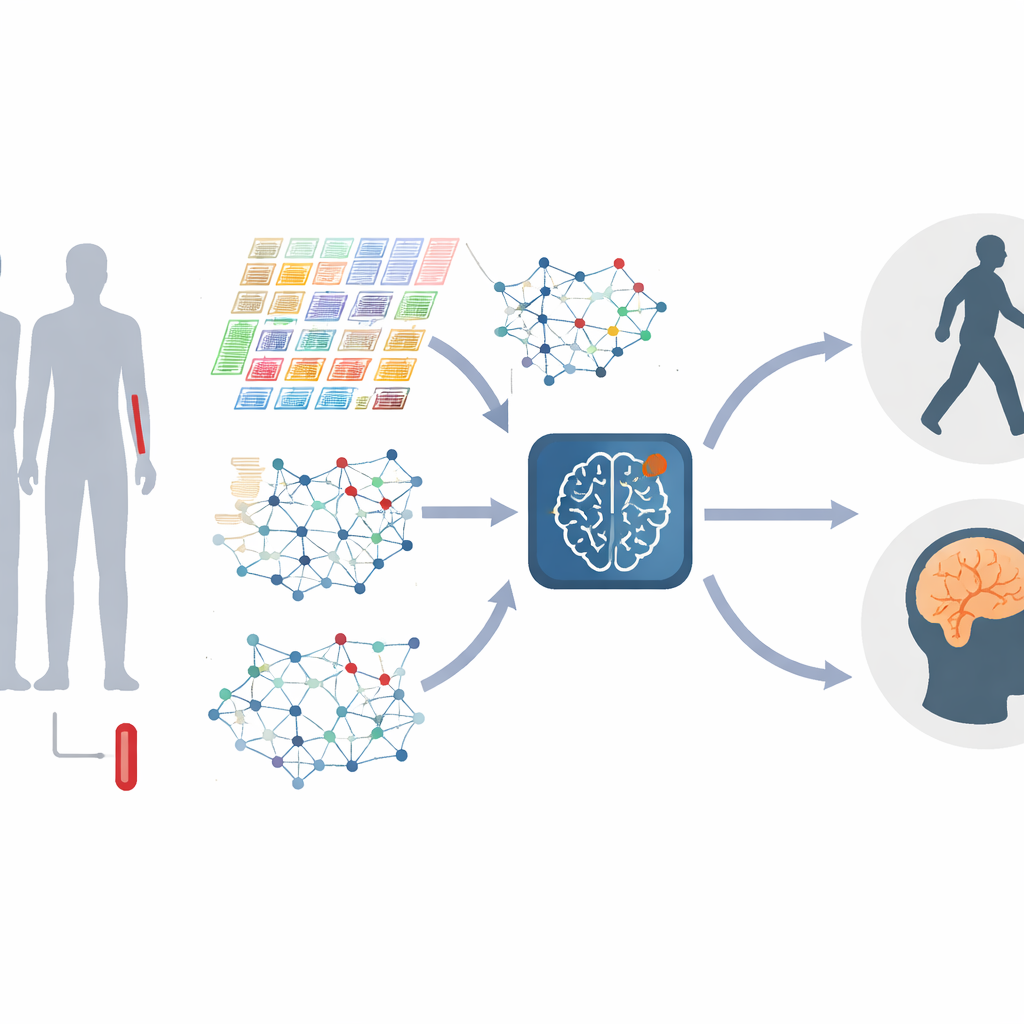
Transformer les gènes en réseaux vivants
Plutôt que de traiter chaque gène séparément, les auteurs représentent les gènes sous la forme d’un réseau, où les gènes qui se comportent de manière similaire sont reliés entre eux. Ces réseaux évoluent à mesure que la maladie progresse, avec des grappes de gènes — souvent liées aux réponses immunitaires, à la gestion des protéines ou à la mort cellulaire — qui gagnent ou perdent en importance. L’étude construit ces « graphes de gènes » à la fois à un niveau global, capturant la structure d’ensemble, et à un niveau local, se concentrant sur des modules étroitement liés de gènes apparentés. En combinant l’information à travers plusieurs échelles, le modèle peut détecter des distorsions fines dans les interactions géniques, susceptibles de marquer différents stades ou types de Parkinson.
Suivre la maladie dans le temps, pas seulement en instantanés
La maladie de Parkinson n’est pas statique, le modèle doit donc aussi saisir le changement. Pour cela, les chercheurs intègrent des prélèvements sanguins répétés des mêmes personnes lors de plusieurs visites cliniques, transformant les données de chaque patient en un court film plutôt qu’en une seule photo. Une partie de leur système se concentre sur la manière dont les niveaux d’activité génique montent et descendent au fil du temps, apprenant quels schémas temporels sont les plus pertinents et filtrant les fluctuations aléatoires. Une autre partie se focalise sur la façon dont les réseaux géniques eux-mêmes se remodèlent à mesure que la maladie avance. Un moteur spécialisé d’« attention de graphe dynamique » apprend ensuite quelles connexions dans ces réseaux évolutifs distinguent le mieux les différents stades de la maladie.
Fusionner deux points de vue en une seule image
Le cœur de la nouvelle méthode, appelée M2DGAT, est de combiner ces deux perspectives — les changements temporels de l’activité génique et la modification de la structure des réseaux géniques — en une représentation conjointe pour chaque patient et chaque moment. Plutôt que de simplement empiler les deux types de données, le modèle utilise une astuce mathématique pour les fusionner, capturant les interactions complexes entre le « quand » et le « comment » les gènes dysfonctionnent. Les signatures obtenues sont ensuite reliées à des mesures cliniques standard : l’échelle de Hoehn et Yahr pour les troubles moteurs et l’Évaluation cognitive de Montréal pour les fonctions cognitives et la mémoire. Sur deux grandes cohortes de Parkinson, cette approche a systématiquement surpassé plusieurs méthodes de pointe en apprentissage profond pour classer le stade de la maladie et prédire les scores cognitifs.
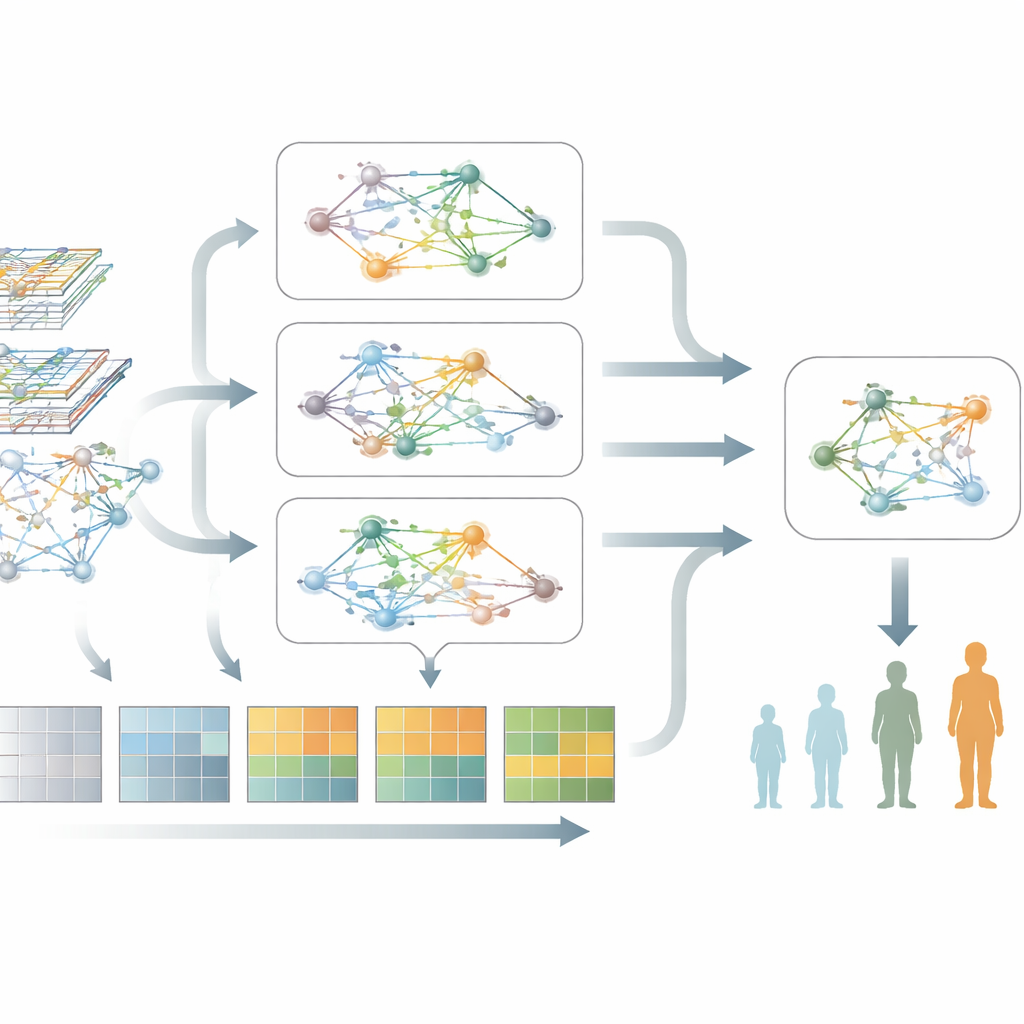
Ce que le modèle révèle sur la biologie de Parkinson
Au-delà de la prédiction, le modèle met en lumière des groupes de gènes et des voies biologiques fortement associés à l’aggravation de la maladie de Parkinson. Lorsque les auteurs ont examiné ces gènes, ils ont trouvé des signaux récurrents pointant vers une production et une gestion des protéines perturbées, une activation immunitaire chronique et des voies liées à la mort programmée des cellules et au stress cellulaire. De manière frappante, ces thèmes biologiques sont apparus dans deux groupes de patients indépendants, suggérant que le modèle capture une biologie robuste liée à la maladie plutôt que des motifs aléatoires. Cette vue au niveau du réseau aide à relier les marqueurs sanguins aux processus sous-jacents qui endommagent les neurones.
Du code complexe à des prévisions plus claires
En termes simples, ce travail montre qu’il est possible de transformer la complexité déroutante de l’activité génique sanguine en une empreinte compacte et lisible de la progression de la maladie de Parkinson. En examinant simultanément comment les gènes fluctuent dans le temps et comment ils interagissent au sein de réseaux changeants, le système M2DGAT peut estimer avec plus de précision à la fois le déclin moteur et cognitif que les outils existants. Bien que des validations supplémentaires soient nécessaires avant une utilisation clinique, l’approche ouvre la voie à un avenir où un test sanguin de routine, interprété par une IA sophistiquée basée sur les réseaux, pourrait aider les médecins à prévoir l’évolution de la maladie de Parkinson et à personnaliser les traitements bien avant l’apparition de symptômes sévères.
Citation: Wei, Z., Zeqi, X., Chenjun, W. et al. M\(\vphantom{0}^2\)DGAT: Multi-view multi-scale dynamic graph attention network(GAT) based prediction of Parkinson’s disease(PD) progression using whole-blood RNA sequencing data. Sci Rep 16, 11777 (2026). https://doi.org/10.1038/s41598-026-40636-x
Mots-clés: maladie de Parkinson, transcriptomique sanguine, réseaux neuronaux graphiques, progression de la maladie, médecine de précision