Clear Sky Science · pl
M $$\vphantom{0}^2$$ DGAT: wieloskalowa, wieloopcowa dynamiczna sieć uwagi grafowej (GAT) do przewidywania postępu choroby Parkinsona (PD) przy użyciu sekwencjonowania RNA z całej krwi
Dlaczego krew może pomóc śledzić choroby mózgu
Choroba Parkinsona jest najbardziej znana z drżeń i problemów z ruchem, ale zanim pojawią się te objawy, w mózgu zachodzą już przez lata ukryte uszkodzenia. Lekarze pilnie potrzebują sposobów przewidywania, jak szybko czyjaś choroba Parkinsona będzie się pogarszać, aby lepiej dostosować i zintensyfikować leczenie. To badanie pokazuje, że proste pobranie krwi, połączone z zaawansowanym systemem sztucznej inteligencji, może ujawnić subtelne sygnały molekularne przewidujące zarówno zmiany ruchowe, jak i poznawcze u osób z Parkinsonem.
Odczytywanie historii mózgu z krwi
Zamiast skanować mózg bezpośrednio, badacze skupili się na sekwencjonowaniu RNA z całej krwi, które mierzy, które geny są w komórkach krwi włączone lub wyciszone. Choć krew jest daleka od mózgu, wcześniejsze prace pokazały, że aktywność układu odpornościowego i inne procesy ogólnoustrojowe odzwierciedlają to, co dzieje się w układzie nerwowym. Wyzwanie polega na tym, że takie pomiary aktywności genów są niezwykle zaszumione: dziesiątki tysięcy genów zmieniają się w czasie, a istotne sygnały chorobowe łatwo mogą zostać zagłuszone. Zespół postawił sobie za cel zbudowanie modelu, który potrafi przesiać tę złożoność i śledzić, jak Parkinson rozwija się u poszczególnych pacjentów.
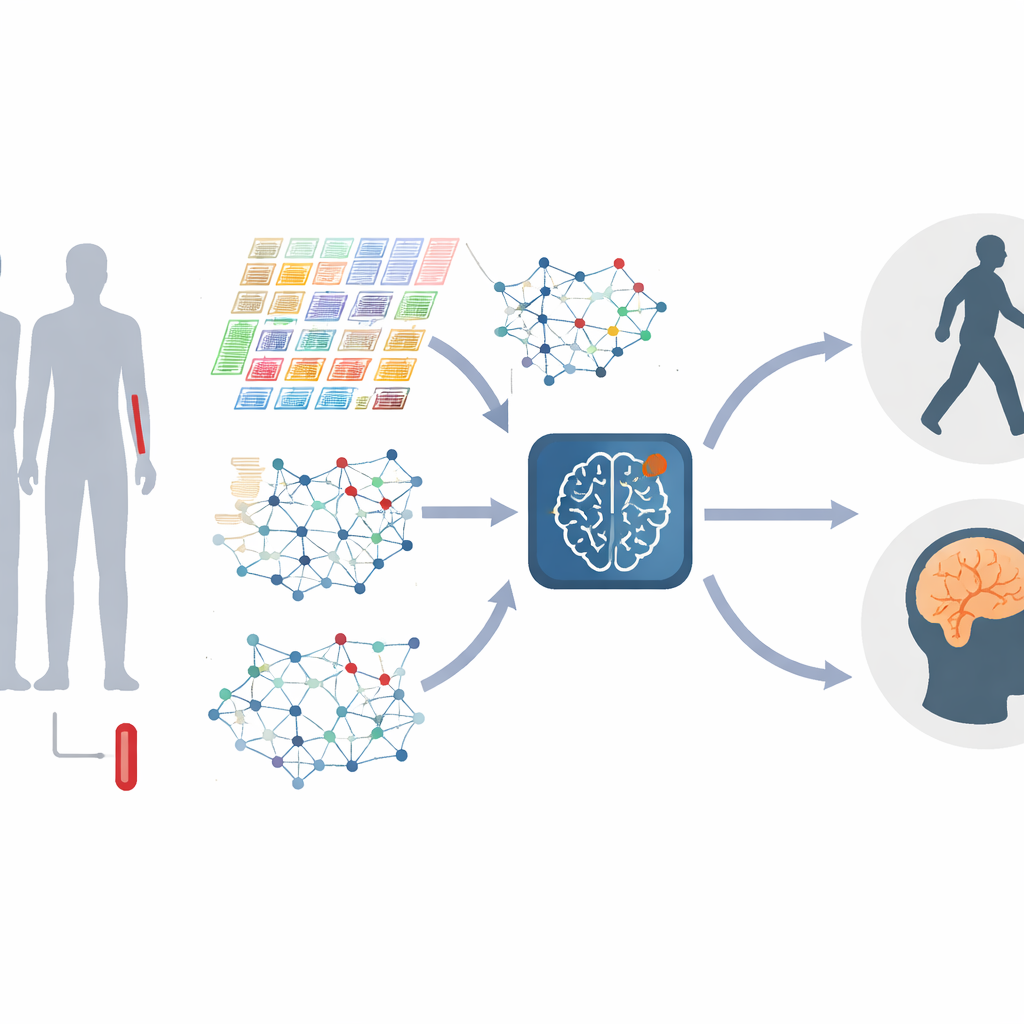
Przekształcanie genów w żywe sieci
Zamiast traktować każdy gen oddzielnie, autorzy przedstawiają geny jako sieć, w której geny o podobnym zachowaniu są ze sobą powiązane. Te sieci zmieniają się wraz z postępem choroby, a klastry genów — często związane z reakcjami odpornościowymi, obróbką białek czy śmiercią komórek — zyskują lub tracą na znaczeniu. Badanie buduje takie „grafy genów” zarówno na poziomie globalnym, obrazującym ogólną strukturę, jak i na poziomie lokalnym, koncentrującym się na ściśle powiązanych modułach genów. Łącząc informacje na wielu skalach, model potrafi wykrywać drobne zniekształcenia w interakcjach genów, które mogą oznaczać różne etapy lub typy Parkinsona.
Śledzenie choroby w czasie, a nie tylko na migawkach
Parkinson nie stoi w miejscu, więc model musi także rozumieć zmiany. Aby to osiągnąć, badacze wykorzystali powtarzane próbki krwi pobierane od tych samych osób podczas kilku wizyt w klinice, zamieniając dane każdego pacjenta w krótki film zamiast pojedynczego zdjęcia. Jedna część systemu koncentruje się na tym, jak poziomy aktywności genów rosną i maleją w czasie, ucząc się, które wzorce czasowe są najistotniejsze i odsiewając losowe fluktuacje. Inna część skupia się na tym, jak same sieci genów są przebudowywane w miarę postępu choroby. Specjalistyczny moduł „dynamicznej uwagi grafowej” uczy się, które połączenia w tych ewoluujących sieciach najlepiej rozróżniają poszczególne etapy choroby.
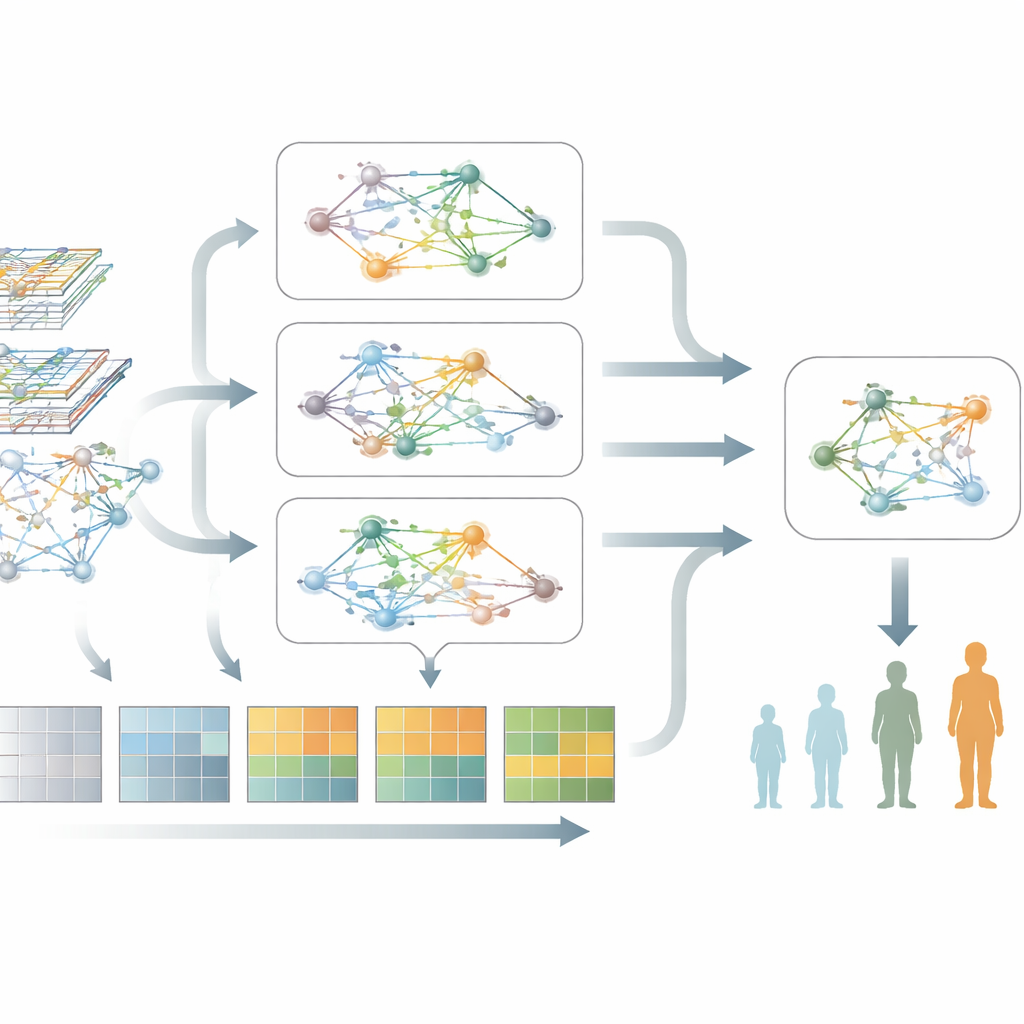
Łączenie dwóch perspektyw w jeden obraz
Rdzeniem nowej metody, nazwanej M2DGAT, jest połączenie tych dwóch perspektyw — zmian czasowych aktywności genów oraz przesunięć w strukturze sieci genów — w jedną wspólną reprezentację dla każdego pacjenta i punktu czasowego. Zamiast po prostu składać oba typy danych razem, model używa sprytnego zabiegu matematycznego do ich fuzji, wychwytując złożone interakcje między „kiedy” a „jak” geny działają nieprawidłowo. Powstałe sygnatury są następnie powiązane ze standardowymi miarami klinicznymi: skalą Hoehna i Yarha dla zaburzeń ruchowych oraz Montreal Cognitive Assessment dla funkcji poznawczych i pamięci. W dwóch dużych kohortach osób z Parkinsonem podejście to konsekwentnie przewyższało kilka wiodących metod głębokiego uczenia w klasyfikowaniu stadium choroby i przewidywaniu wyników poznawczych.
Co model ujawnia o biologii Parkinsona
Poza samą predykcją, model wskazuje grupy genów i szlaki molekularne najsilniej związane z pogarszaniem się Parkinsona. Gdy autorzy przeanalizowali te geny, znaleźli powtarzające się sygnały wskazujące na zaburzenia produkcji i obróbki białek, przewlekłą aktywację układu odpornościowego oraz szlaki związane z zaprogramowaną śmiercią komórkową i stresem komórkowym. Co istotne, te biologiczne motywy pojawiły się w dwóch niezależnych grupach pacjentów, co sugeruje, że model wychwytuje odporne, związane z chorobą procesy, a nie przypadkowe wzorce. Taki widok na poziomie sieci pomaga powiązać markery krwi z procesami prowadzącymi do uszkodzenia neuronów.
Od złożonego kodu do jaśniejszych prognoz
Mówiąc prosto, praca ta pokazuje, że można przekształcić przytłaczającą złożoność aktywności genów we krwi w zwarte, czytelne odciski palców postępu Parkinsona. Patrząc jednocześnie na to, jak geny fluktuują w czasie i jak wchodzą w interakcje w zmieniających się sieciach, system M2DGAT potrafi dokładniej ocenić zarówno pogorszenie ruchowe, jak i poznawcze niż istniejące narzędzia. Choć przed zastosowaniem w praktyce klinicznej potrzebna jest dalsza walidacja, podejście to wskazuje na przyszłość, w której rutynowy test krwi, zinterpretowany przez zaawansowaną, opartą na sieciach sztuczną inteligencję, mógłby pomóc lekarzom prognozować przebieg Parkinsona i dostosowywać leczenie na długo przed pojawieniem się ciężkich objawów.
Cytowanie: Wei, Z., Zeqi, X., Chenjun, W. et al. M\(\vphantom{0}^2\)DGAT: Multi-view multi-scale dynamic graph attention network(GAT) based prediction of Parkinson’s disease(PD) progression using whole-blood RNA sequencing data. Sci Rep 16, 11777 (2026). https://doi.org/10.1038/s41598-026-40636-x
Słowa kluczowe: choroba Parkinsona, transkryptomika krwi, grafowe sieci neuronowe, postęp choroby, medycyna precyzyjna