Clear Sky Science · es
M $$\vphantom{0}^2$$ DGAT: Red de atención de grafos dinámica multivista y multiescala basada en GAT para la predicción de la progresión de la enfermedad de Parkinson (EP) usando datos de secuenciación de ARN de sangre total
Por qué la sangre puede ayudar a seguir una enfermedad cerebral
La enfermedad de Parkinson es más conocida por sus temblores y problemas de movimiento, pero cuando estos síntomas aparecen ya han ocurrido años de daño oculto en el cerebro. Los médicos necesitan con urgencia formas de prever con qué rapidez empeorará la enfermedad en una persona para poder cronometrar y personalizar mejor los tratamientos. Este estudio muestra que una simple extracción de sangre, combinada con un sistema avanzado de inteligencia artificial, puede revelar señales moleculares sutiles que predicen tanto los cambios en el movimiento como en las funciones cognitivas en personas con Parkinson.
Leer la historia del cerebro a partir de la sangre
En lugar de escanear el cerebro directamente, los investigadores se centraron en la secuenciación de ARN de sangre total, que mide qué genes están activados o desactivados en las células sanguíneas. Aunque la sangre está lejos del cerebro, trabajos previos han mostrado que la actividad inmunitaria y otros procesos corporales reflejan lo que ocurre en el sistema nervioso. El reto es que estas lecturas de actividad génica son extremadamente ruidosas: decenas de miles de genes fluctúan con el tiempo y las señales relevantes de la enfermedad pueden quedar fácilmente sepultadas. El equipo se propuso construir un modelo capaz de cribar esta complejidad y seguir cómo se desarrolla el Parkinson en pacientes individuales.
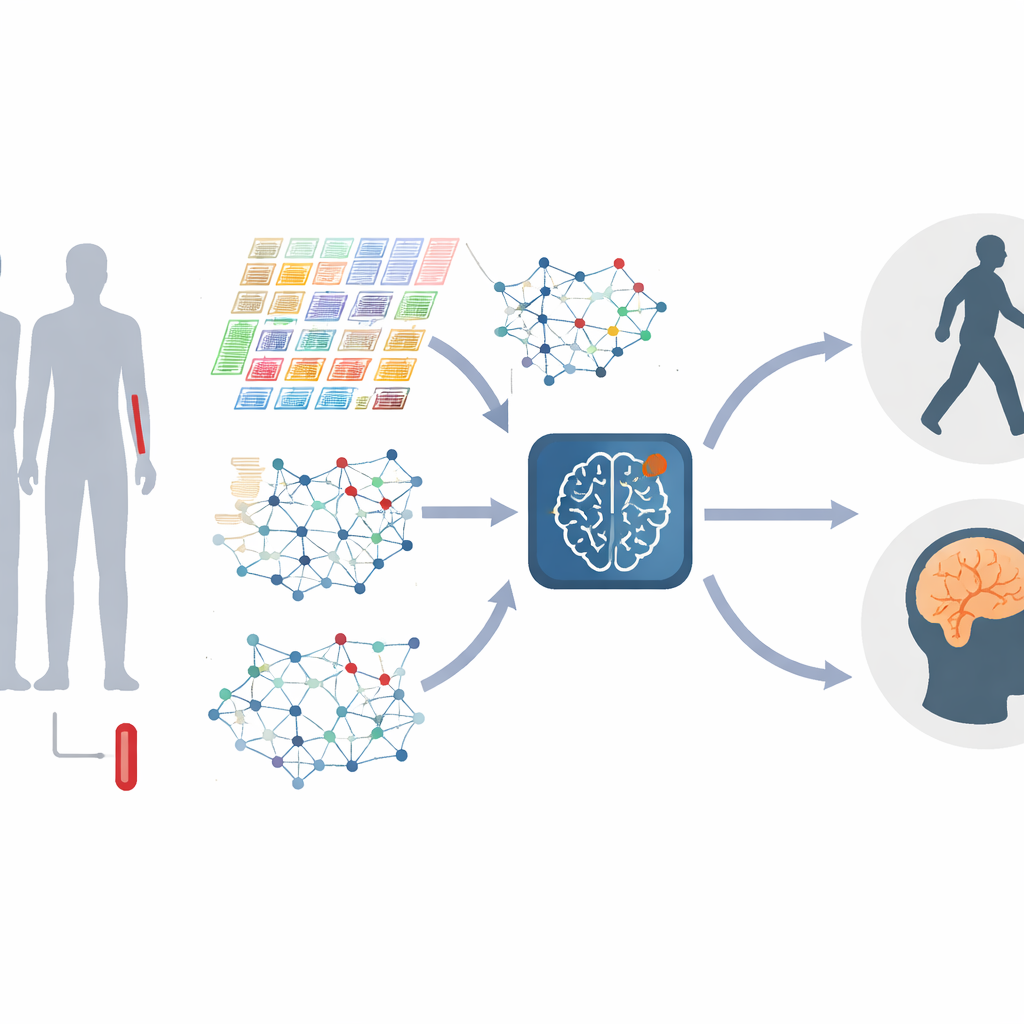
Convertir genes en redes vivas
En lugar de tratar cada gen por separado, los autores representan los genes como una red, donde genes con comportamientos similares están conectados entre sí. Estas redes cambian conforme progresa la enfermedad, con agrupaciones de genes—a menudo relacionadas con respuestas inmunitarias, manejo de proteínas o muerte celular—que aumentan o disminuyen de importancia. El estudio construye estos “grafos génicos” tanto a nivel global, capturando la estructura general, como a nivel local, enfocándose en módulos fuertemente conectados de genes relacionados. Al combinar información a través de muchas escalas, el modelo puede detectar distorsiones finas en cómo interactúan los genes, lo que puede señalar distintas etapas o tipos de Parkinson.
Seguir la enfermedad a lo largo del tiempo, no solo en instantáneas
El Parkinson no permanece estático, por lo que el modelo también necesita entender el cambio. Para ello, los investigadores usan muestras de sangre repetidas de las mismas personas en varias visitas clínicas, convirtiendo los datos de cada individuo en una pequeña película en lugar de una sola foto. Una parte de su sistema se centra en cómo los niveles de actividad génica suben y bajan con el tiempo, aprendiendo qué patrones temporales importan y filtrando fluctuaciones aleatorias. Otra parte se centra en cómo las propias redes génicas se reconfiguran a medida que avanza la enfermedad. Un motor especializado de “atención de grafos dinámica” aprende entonces qué conexiones en estas redes en evolución distinguen mejor una etapa de la enfermedad de otra.
Combinar dos perspectivas en una sola imagen
El núcleo del nuevo método, llamado M2DGAT, es que combina estas dos perspectivas—los cambios temporales en la actividad génica y la estructura cambiante de las redes génicas—en una representación conjunta para cada paciente y momento temporal. En lugar de simplemente apilar los dos tipos de datos, el modelo utiliza un ingenioso recurso matemático para fusionarlos, capturando interacciones complejas entre el “cuándo” y el “cómo” fallan los genes. Las firmas resultantes se vinculan luego con medidas clínicas estándar: la escala de Hoehn y Yahr para problemas de movimiento y el Montreal Cognitive Assessment para funciones cognitivas y memoria. En dos grandes cohortes de Parkinson, este enfoque superó de forma consistente a varios métodos de aprendizaje profundo líderes en la clasificación del estadio de la enfermedad y en la predicción de puntuaciones cognitivas.
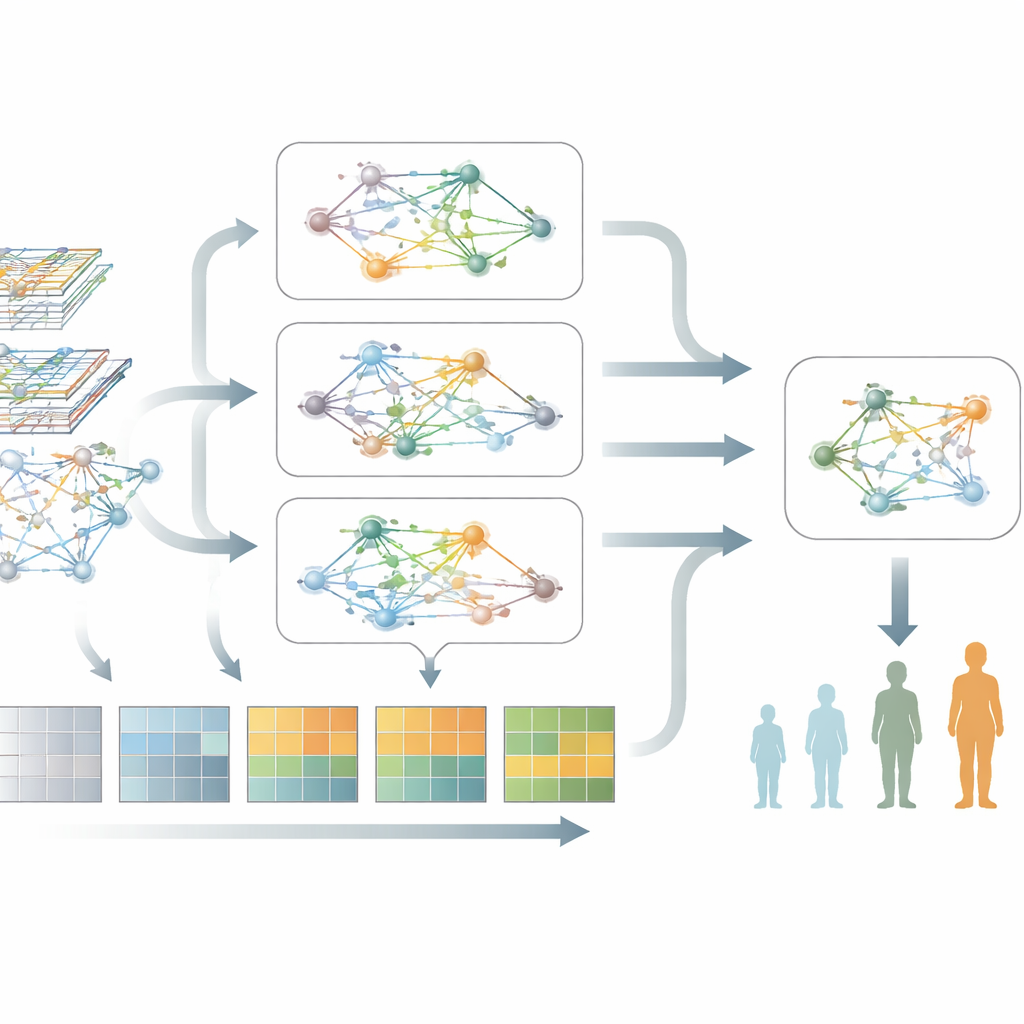
Lo que el modelo revela sobre la biología del Parkinson
Más allá de la predicción, el modelo destaca grupos de genes y vías que se asocian con el empeoramiento del Parkinson. Cuando los autores examinaron estos genes, hallaron señales repetidas que apuntan a una alteración en la producción y manejo de proteínas, activación inmunitaria crónica y rutas vinculadas a la muerte celular programada y al estrés celular. De forma destacada, estos temas biológicos aparecieron en dos grupos de pacientes independientes, lo que sugiere que el modelo captura biología relacionada con la enfermedad y robusta en lugar de patrones aleatorios. Esta visión a nivel de red ayuda a vincular los marcadores sanguíneos con los procesos subyacentes que dañan las neuronas.
Del código complejo a pronósticos más claros
En términos sencillos, este trabajo muestra que es posible convertir la desconcertante complejidad de la actividad génica sanguínea en una huella compacta y legible de la progresión del Parkinson. Al observar simultáneamente cómo los genes fluctúan con el tiempo y cómo interactúan en redes cambiantes, el sistema M2DGAT puede evaluar con mayor precisión tanto el deterioro motor como el cognitivo que las herramientas existentes. Aunque se necesita más validación antes de que pueda orientar la atención clínica, el enfoque apunta a un futuro en el que una prueba de sangre de rutina, interpretada mediante IA sofisticada basada en redes, podría ayudar a los médicos a prever el curso del Parkinson y personalizar tratamientos mucho antes de que aparezcan síntomas graves.
Cita: Wei, Z., Zeqi, X., Chenjun, W. et al. M\(\vphantom{0}^2\)DGAT: Multi-view multi-scale dynamic graph attention network(GAT) based prediction of Parkinson’s disease(PD) progression using whole-blood RNA sequencing data. Sci Rep 16, 11777 (2026). https://doi.org/10.1038/s41598-026-40636-x
Palabras clave: Enfermedad de Parkinson, transcriptómica sanguínea, redes neuronales de grafos, progresión de la enfermedad, medicina de precisión