Clear Sky Science · it
M $$\vphantom{0}^2$$ DGAT: rete di attenzione dinamica a grafo multi-visione multi-scala (GAT) per la predizione della progressione del morbo di Parkinson (PD) usando dati di sequenziamento dell'RNA del sangue intero
Perché il sangue può aiutare a tracciare le malattie cerebrali
Il morbo di Parkinson è più noto per i suoi tremori e i problemi di movimento, ma quando questi sintomi compaiono, anni di danni nascosti si sono già accumulati nel cervello. I medici hanno un bisogno urgente di strumenti per prevedere quanto velocemente la malattia progredirà in una persona, in modo da poter tempificare e personalizzare meglio i trattamenti. Questo studio dimostra che un semplice prelievo di sangue, combinato con un sistema di intelligenza artificiale avanzato, può rivelare segnali molecolari sottili che predicono sia i cambiamenti motori sia quelli cognitivi nelle persone con Parkinson.
Leggere la storia del cervello dal sangue
Invece di esaminare direttamente il cervello, i ricercatori si sono concentrati sul sequenziamento dell'RNA del sangue intero, che misura quali geni sono attivati o repressi nelle cellule del sangue. Sebbene il sangue sia lontano dal cervello, lavori precedenti hanno mostrato che l'attività immunitaria e altri processi sistemici rispecchiano ciò che avviene nel sistema nervoso. La sfida è che questi rilievi dell'attività genica sono estremamente rumorosi: decine di migliaia di geni fluttuano nel tempo e i segnali importanti della malattia possono facilmente essere sommersi. Il gruppo ha quindi costruito un modello in grado di setacciare questa complessità e tracciare come il Parkinson si sviluppa in singoli pazienti.
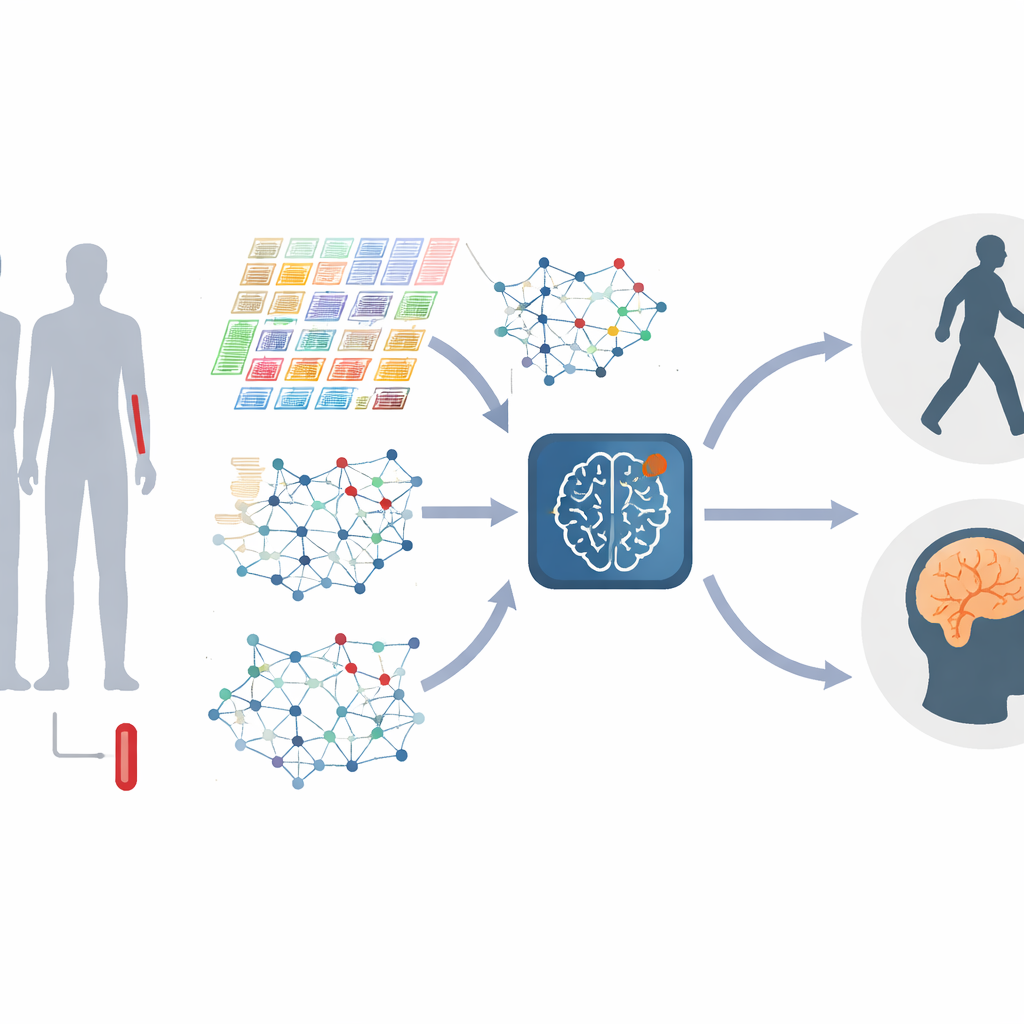
Trasformare i geni in reti viventi
Invece di trattare ogni gene separatamente, gli autori rappresentano i geni come una rete, dove i geni che si comportano in modo simile sono collegati tra loro. Queste reti cambiano con la progressione della malattia, con ammassi di geni — spesso legati a risposte immunitarie, gestione delle proteine o morte cellulare — che crescono o diminuiscono di importanza. Lo studio costruisce questi “grafi genici” sia a livello globale, catturando la struttura complessiva, sia a livello locale, concentrandosi su moduli ben connessi di geni correlati. Combinando informazioni su molte scale, il modello può rilevare distorsioni fini nelle interazioni geniche, che possono segnare differenti stadi o tipi di Parkinson.
Seguire la malattia nel tempo, non solo in istantanee
Il Parkinson non è statico, quindi il modello deve anche comprendere il cambiamento. Per farlo, i ricercatori immettono campioni di sangue ripetuti dalle stesse persone in più visite cliniche, trasformando i dati di ciascuna persona in un breve film invece che in una singola fotografia. Una parte del sistema si concentra su come i livelli di attività genica aumentano e diminuiscono nel tempo, imparando quali schemi temporali sono più rilevanti e filtrando le fluttuazioni casuali. Un'altra parte si concentra su come le reti geniche stesse si rimodellano con l'avanzare della malattia. Un motore specializzato di “attenzione a grafo dinamico” impara quindi quali connessioni in queste reti in evoluzione distinguono meglio uno stadio della malattia da un altro.
Fondere due prospettive in un'unica immagine
Il cuore del nuovo metodo, chiamato M2DGAT, è che combina queste due prospettive — i cambiamenti temporali nell'attività genica e la mutazione della struttura delle reti geniche — in un'unica rappresentazione congiunta per ogni paziente e punto temporale. Invece di limitarsi ad accatastare i due tipi di dati, il modello usa un trucco matematico intelligente per fonderli, catturando interazioni complesse tra il “quando” e il “come” i geni si comportano in modo anomalo. Le firme risultanti sono poi collegate a misure cliniche standard: la scala di Hoehn e Yahr per i problemi motori e il Montreal Cognitive Assessment per funzioni cognitive e memoria. In due grandi coorti di Parkinson, questo approccio ha costantemente superato diversi metodi di deep learning di riferimento nella classificazione dello stadio della malattia e nella predizione dei punteggi cognitivi.
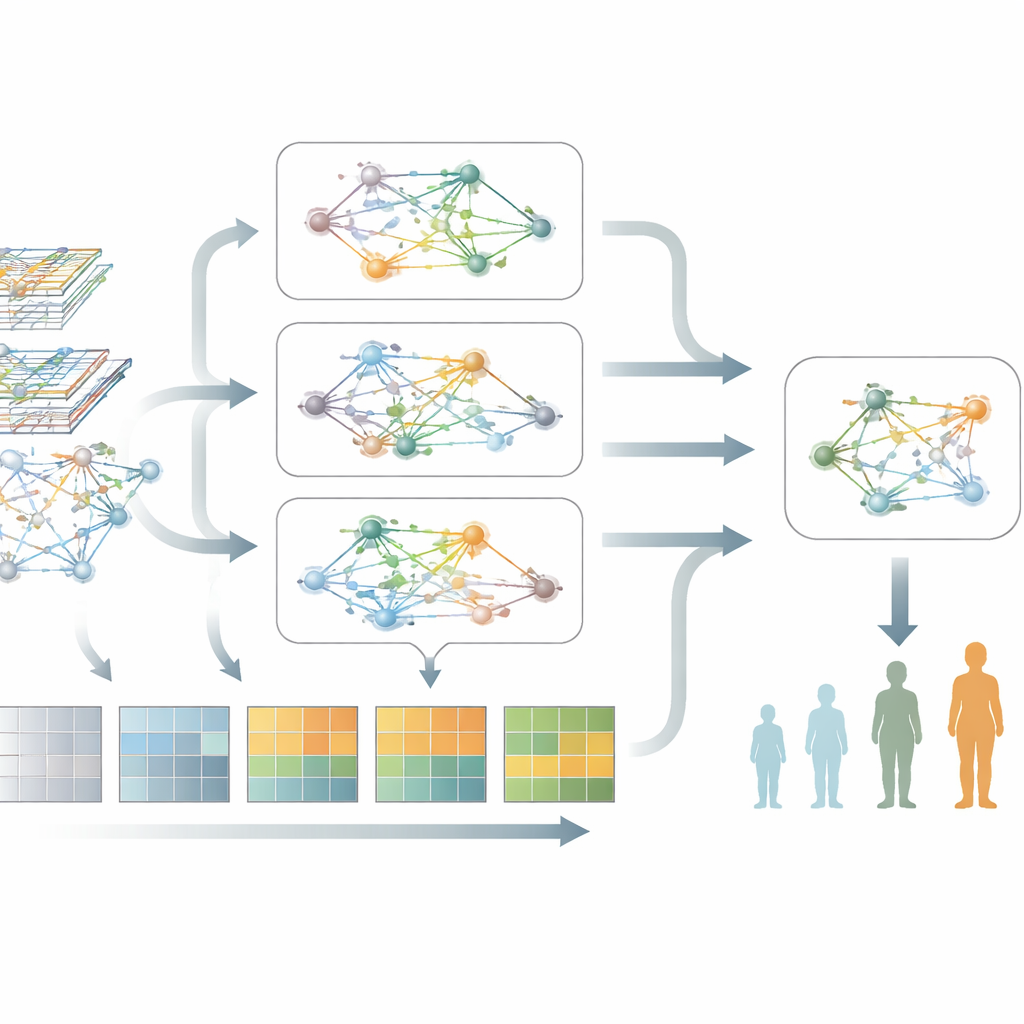
Cosa rivela il modello sulla biologia del Parkinson
Oltre alla previsione, il modello mette in evidenza gruppi di geni e vie biologiche fortemente associati al peggioramento del Parkinson. Quando gli autori hanno esaminato questi geni, hanno trovato segnali ricorrenti che indicano una produzione e gestione delle proteine alterata, un'attivazione immunitaria cronica e vie legate alla morte cellulare programmata e allo stress cellulare. In modo notevole, questi temi biologici sono comparsi in due gruppi di pazienti indipendenti, suggerendo che il modello cattura una biologia correlata alla malattia e robusta piuttosto che pattern casuali. Questo tipo di visione a livello di rete aiuta a ricollegare i marcatori del sangue ai processi sottostanti che danneggiano i neuroni.
Dal codice complesso a previsioni più chiare
In termini semplici, questo lavoro dimostra che è possibile trasformare l'intricata complessità dell'attività genica nel sangue in un'impronta compatta e interpretabile della progressione del Parkinson. Osservando simultaneamente come i geni fluttuano nel tempo e come interagiscono in reti in evoluzione, il sistema M2DGAT può valutare con maggiore accuratezza sia il declino motorio sia quello cognitivo rispetto agli strumenti esistenti. Pur richiedendo ulteriori validazioni prima di poter essere usato per guidare le cure, l'approccio indica un futuro in cui un normale esame del sangue, interpretato tramite un'IA sofisticata basata su reti, potrebbe aiutare i medici a prevedere l'andamento del Parkinson e a personalizzare i trattamenti molto prima che compaiano sintomi gravi.
Citazione: Wei, Z., Zeqi, X., Chenjun, W. et al. M\(\vphantom{0}^2\)DGAT: Multi-view multi-scale dynamic graph attention network(GAT) based prediction of Parkinson’s disease(PD) progression using whole-blood RNA sequencing data. Sci Rep 16, 11777 (2026). https://doi.org/10.1038/s41598-026-40636-x
Parole chiave: morbo di Parkinson, trascrittomica del sangue, reti neurali a grafo, progressione della malattia, medicina di precisione