Clear Sky Science · de
M $$\vphantom{0}^2$$ DGAT: Multi-View Multi-Skalen Dynamic Graph Attention Network (GAT)-basierte Vorhersage des Fortschreitens der Parkinson-Krankheit (PD) mithilfe von Whole-Blood-RNA-Sequenzierungsdaten
Warum Blut dabei helfen kann, Hirnerkrankungen zu verfolgen
Die Parkinson-Krankheit ist vor allem für Zittern und Bewegungsstörungen bekannt, doch zu dem Zeitpunkt, an dem diese Symptome sichtbar werden, hat das Gehirn bereits jahrelange verborgene Schäden erlitten. Ärztinnen und Ärzte benötigen dringend Methoden, um vorherzusagen, wie schnell die Krankheit eines Menschen voranschreitet, damit Behandlungen besser terminiert und individualisiert werden können. Diese Studie zeigt, dass eine einfache Blutabnahme, kombiniert mit einem fortgeschrittenen System der künstlichen Intelligenz, subtile molekulare Signale offenbaren kann, die Bewegungs- und Denkveränderungen bei Menschen mit Parkinson vorhersagen.
Die Geschichte des Gehirns im Blut lesen
Statt das Gehirn direkt zu scannen, konzentrierten sich die Forschenden auf Whole-Blood-RNA-Sequencing, das misst, welche Gene in Blutzellen hoch- oder runterreguliert sind. Obwohl Blut weit vom Gehirn entfernt ist, haben frühere Arbeiten gezeigt, dass Immunaktivität und andere körperweite Prozesse widerspiegeln, was im Nervensystem geschieht. Die Herausforderung besteht darin, dass diese Genaktivitätsmessungen extrem verrauscht sind: Zehntausende Gene schwanken über die Zeit, und wichtige krankheitsbezogene Signale können leicht untergehen. Das Team machte sich daran, ein Modell zu entwickeln, das diese Komplexität durchsiebt und verfolgt, wie sich Parkinson bei einzelnen Patienten entfaltet.
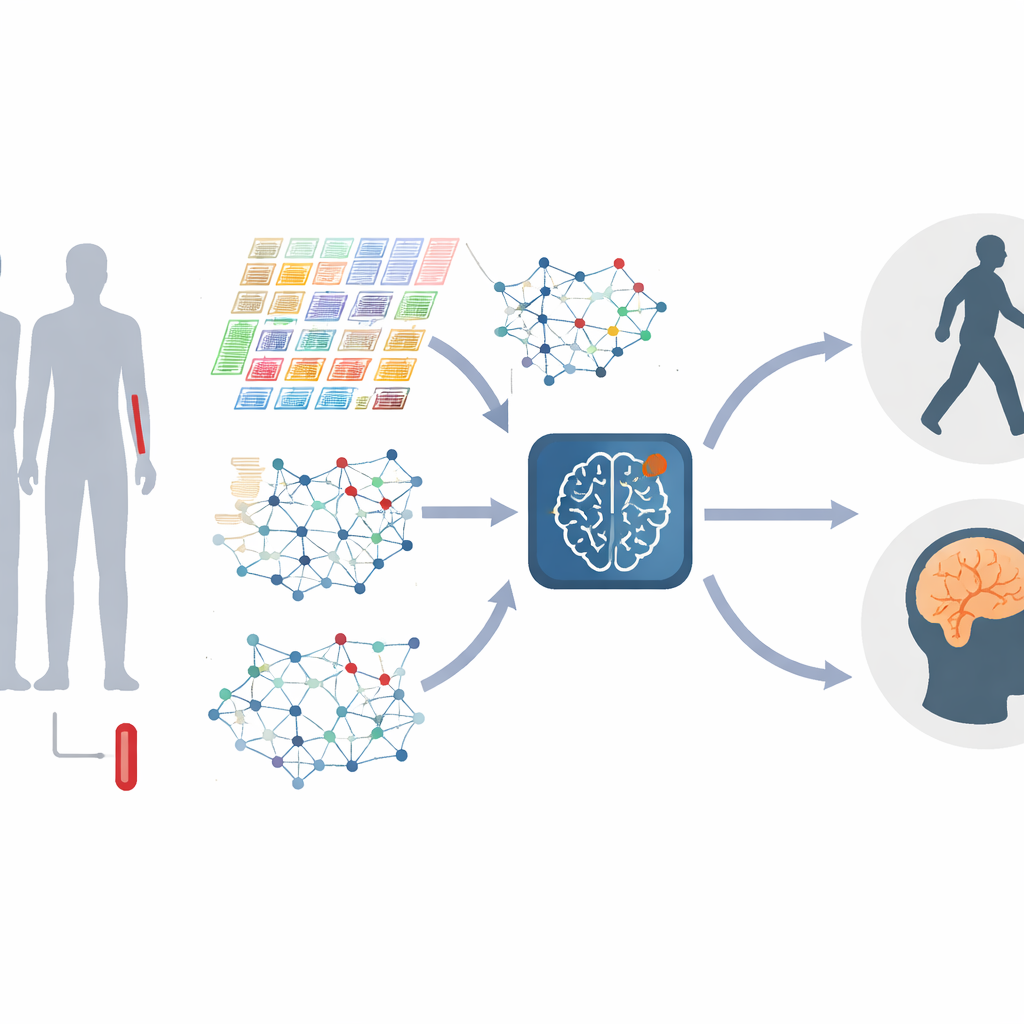
Gene in lebendige Netzwerke verwandeln
Anstatt jedes Gen einzeln zu betrachten, stellen die Autorinnen und Autoren Gene als Netzwerk dar, in dem ähnlich reagierende Gene miteinander verbunden sind. Diese Netzwerke verändern sich, wenn die Krankheit fortschreitet: Gencluster — häufig verbunden mit Immunantworten, Proteinverarbeitung oder Zelltod — gewinnen oder verlieren an Bedeutung. Die Studie konstruiert diese „Gen-Graphen“ sowohl auf globaler Ebene, um die Gesamtstruktur einzufangen, als auch auf lokaler Ebene, mit Fokus auf eng vernetzte Module verwandter Gene. Durch die Kombination von Informationen über viele Skalen kann das Modell feingliedrige Verzerrungen in den Geninteraktionen erkennen, die unterschiedliche Stadien oder Typen von Parkinson markieren können.
Die Krankheit über die Zeit verfolgen, nicht nur Momentaufnahmen
Parkinson bleibt nicht statisch, daher muss das Modell auch Veränderung verstehen. Dafür speisen die Forschenden wiederholte Blutproben derselben Personen von mehreren Klinikbesuchen ein und verwandeln die Daten jedes Menschen in einen Kurzfilm statt in ein einzelnes Foto. Ein Teil ihres Systems konzentriert sich darauf, wie Genaktivitätsniveaus im Zeitverlauf steigen und fallen, lernt, welche zeitlichen Muster am wichtigsten sind, und filtert zufällige Schwankungen heraus. Ein anderer Teil fokussiert darauf, wie sich die Genetzwerke selbst umbauen, während die Krankheit voranschreitet. Eine spezialisierte „dynamic graph attention“-Engine lernt dann, welche Verbindungen in diesen sich entwickelnden Netzwerken am besten ein Krankheitsstadium vom anderen unterscheiden.
Zwei Perspektiven zu einem Bild verschmelzen
Kernstück der neuen Methode, genannt M2DGAT, ist die Kombination dieser beiden Perspektiven — zeitliche Veränderungen der Genaktivität und die sich wandelnde Gen-Netzwerkstruktur — zu einer gemeinsamen Repräsentation für jeden Patienten und jeden Zeitpunkt. Anstatt die beiden Datentypen einfach nebeneinander zu stellen, nutzt das Modell einen ausgeklügelten mathematischen Ansatz, um sie zu verschmelzen und komplexe Wechselwirkungen zwischen dem „wann" und dem „wie" der fehlerhaften Genaktivität zu erfassen. Die resultierenden Signaturen werden dann mit gängigen klinischen Messgrößen verknüpft: der Hoehn-und-Yahr-Skala für Bewegungsstörungen und dem Montreal Cognitive Assessment für kognitive Fähigkeiten und Gedächtnis. In zwei großen Parkinson-Kohorten übertraf dieser Ansatz wiederholt mehrere führende Deep-Learning-Methoden bei der Stadieneinteilung und der Vorhersage kognitiver Scores.
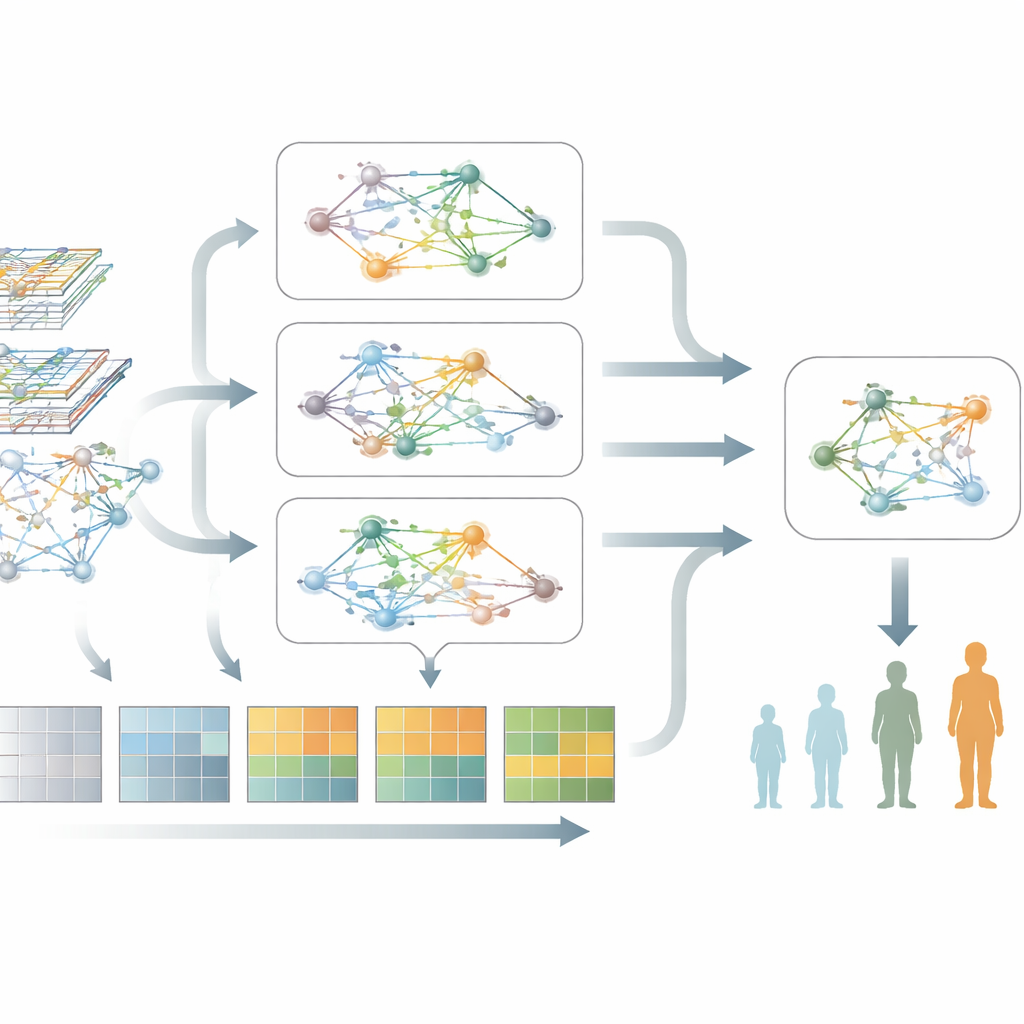
Was das Modell über die Biologie von Parkinson verrät
Über die reine Vorhersage hinaus hebt das Modell Gruppen von Genen und Signalwege hervor, die am stärksten mit einer Verschlechterung von Parkinson assoziiert sind. Bei der Untersuchung dieser Gene fanden die Autorinnen und Autoren wiederkehrende Hinweise auf gestörte Proteinsynthese und -verarbeitung, chronische Immunaktivierung sowie Wege, die mit programmiertem Zelltod und zellulärem Stress verknüpft sind. Auffällig ist, dass diese biologischen Themen in zwei unabhängigen Patientengruppen auftauchten, was darauf hindeutet, dass das Modell robuste, krankheitsbezogene Biologie erfasst und nicht nur zufällige Muster. Diese Netzwerk-Perspektive hilft, Blutmarker mit den zugrunde liegenden Prozessen zu verbinden, die Neurone schädigen.
Vom komplexen Code zu klareren Prognosen
Einfach gesagt zeigt diese Arbeit, dass es möglich ist, die überwältigende Komplexität der Genaktivität im Blut in einen kompakten, lesbaren Fingerabdruck des Parkinson-Fortschreitens zu verwandeln. Indem man gleichzeitig betrachtet, wie Gene über die Zeit schwanken und wie sie in sich wandelnden Netzwerken interagieren, kann das M2DGAT-System sowohl Bewegungs- als auch kognitiven Abbau genauer einschätzen als bestehende Werkzeuge. Zwar sind vor einer praktischen Anwendung weitere Validierungen erforderlich, doch der Ansatz deutet auf eine Zukunft hin, in der ein routinemäßiger Bluttest, interpretiert durch fortgeschrittene netzwerkbasierte KI, Ärzten helfen könnte, den Verlauf von Parkinson vorherzusagen und Therapien lange vor dem Auftreten schwerer Symptome individuell anzupassen.
Zitation: Wei, Z., Zeqi, X., Chenjun, W. et al. M\(\vphantom{0}^2\)DGAT: Multi-view multi-scale dynamic graph attention network(GAT) based prediction of Parkinson’s disease(PD) progression using whole-blood RNA sequencing data. Sci Rep 16, 11777 (2026). https://doi.org/10.1038/s41598-026-40636-x
Schlüsselwörter: Parkinson-Krankheit, Blut-Transkriptomik, Graph-Neuronale Netze, Krankheitsprogression, Präzisionsmedizin