Clear Sky Science · zh
硫化氢通过增强氧化磷酸化修复IFNγ/TNFα诱导的肠上皮屏障功能障碍
为什么肠道这层薄壁很重要
我们的肠道内壁仅有一层细胞,但它将肠腔内的外部环境与身体其余部分分隔开来。当这个屏障变得“渗漏”时,细菌和毒素可能穿透进入,助长不仅局限于消化道的炎症,还会影响肝脏、大脑和其他器官。本研究探讨了一种含硫小分子(能缓慢释放硫化氢气体)如何在炎症期间通过增强细胞的能量产生来保护这层脆弱的屏障。
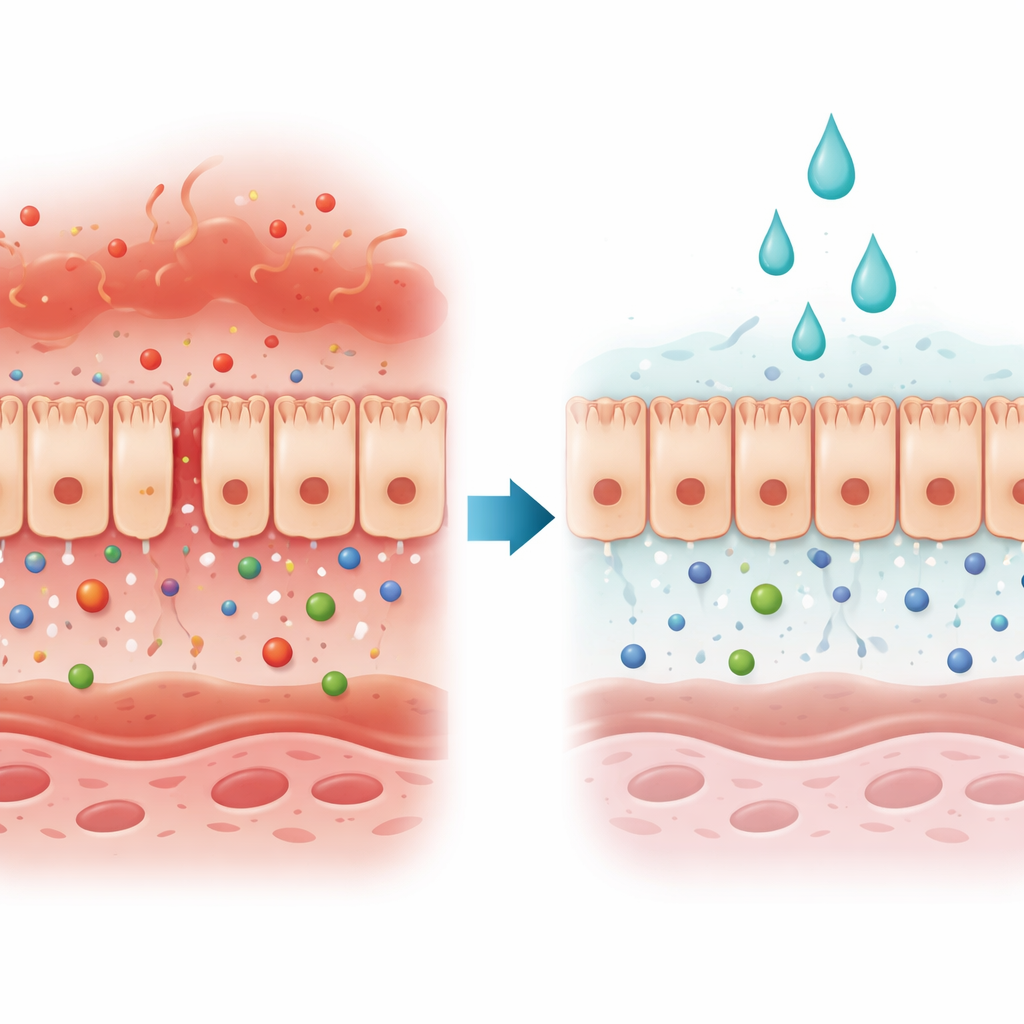
被攻击的身体守门人
肠上皮细胞形成一片连续的细胞层,像有选择性的门闸:阻挡有害入侵者,同时允许养分和水分通过。在许多肠病和肝病中,这道门闸失效,原因包括细胞间隙打开或细胞死亡。作者关注的是由两种免疫信号——干扰素γ和肿瘤坏死因子α——驱动的一类损伤,这些因子在炎性肠病中很常见。两者共同削弱了屏障,使肠道内的物质更容易到达血液循环。
具有双重特性的硫供体
研究者研究了4‑羟基硫苯甲酰胺(TBZ),这是一种可以释放硫化氢的化合物,而硫化氢在我们的细胞中也以低水平产生并具有保护作用。在体外培养的肠上皮细胞层和人类肠类器官中,TBZ表现出一种有趣且依赖情境的效应。单独使用时,它略微增加了细胞间的渗漏。但当屏障已被炎性信号损伤时,TBZ在很大程度上恢复了其功能。它减少了表征屏障破坏的电生理变化,并使荧光示踪分子的通透恢复到接近正常,尽管它并不能阻止细胞因细胞因子而发生的死亡。
为细胞的能量工厂提速
为揭示TBZ如何发挥这种保护作用,团队检查了处理后细胞的全基因表达。他们发现TBZ强烈激活了与氧化磷酸化相关的基因——这是线粒体(细胞的“发电厂”)生成大部分ATP能量的过程。线粒体复合体IV的关键成分及相关转运蛋白上调,提示TBZ在调节能量机械而非经典炎症通路方面发挥作用。后续实验证实了这一点:在炎症条件下,TBZ提高了线粒体ATP的产生而未改变糖酵解,表明是一种针对高效能量输出的特定提升。
当线粒体失常,屏障就会失守
作者随后检验了这种能量提升是否为屏障修复所必需。他们使用叠氮化钠,这是一种阻断线粒体复合体IV的化学物质。在不致细胞立即死亡的剂量下,叠氮化钠几乎关闭了氧化磷酸化,而使糖酵解在很大程度上保持。对接受TBZ处理的炎性细胞同时加入叠氮化钠后,TBZ的保护性屏障效应被抹去:电阻再次下降,荧光示踪物更容易渗漏。尽管细胞为代偿而在一定程度上转向糖酵解,但总ATP下降且屏障未能恢复,这将完整的线粒体呼吸直接与屏障完整性联系起来。
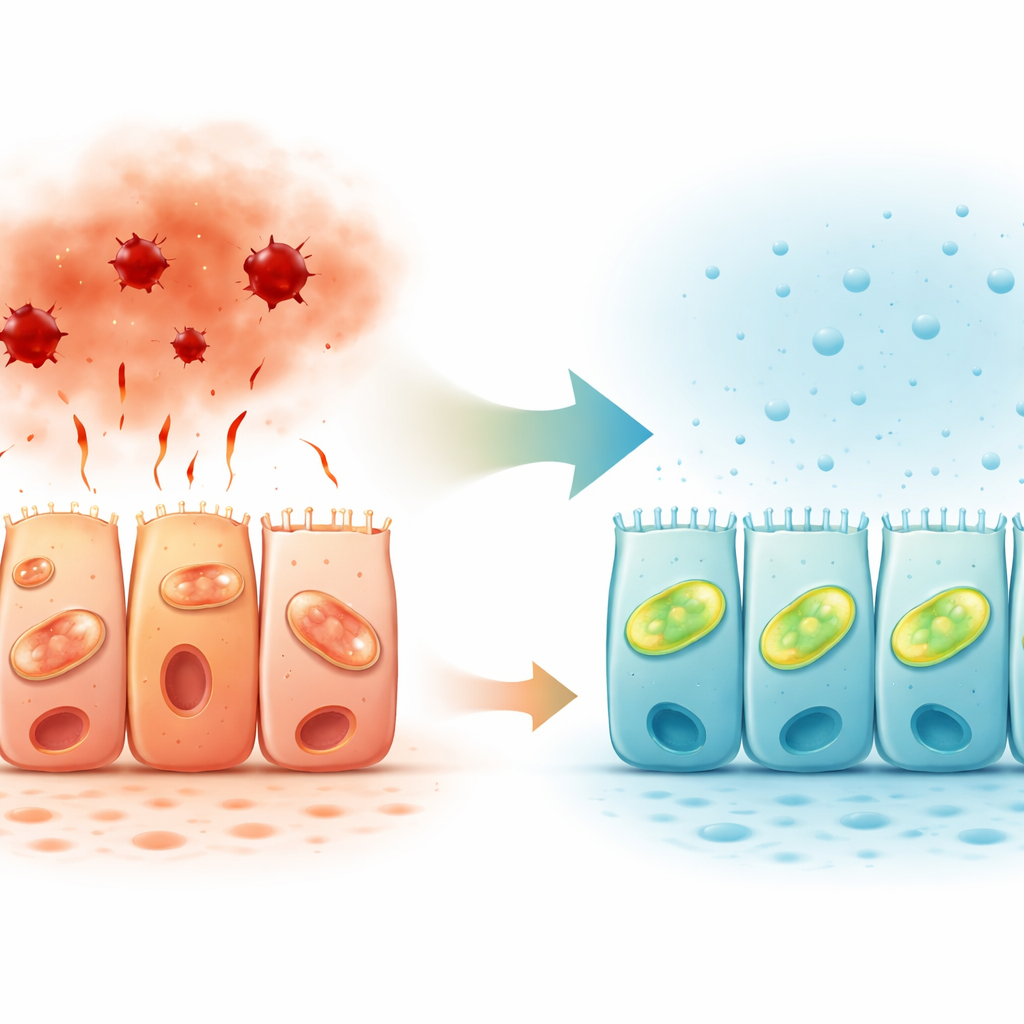
肠上皮中的天然气体信号
在观察人类结肠组织时,研究者还绘制了产生硫化氢的酶的位置分布。两种此类酶在上皮细胞朝向肠腔的一侧表达最强,尤其在升结肠更为明显。这种极化的表达模式支持了硫化氢在屏障与肠内容物接触的表面局部作用的观点,微调细胞对压力的响应。结合此前研究显示炎性肠病中硫化氢通路降低的结果,这些发现提示气体信号减弱可能促成了患者的屏障失效。
对未来治疗的意义
总体而言,这项研究显示,一种释放硫化氢的化合物能够通过提升线粒体的能量产生,特别是通过氧化磷酸化,来挽救被炎症损坏、渗漏的肠道屏障,尽管它本身并不阻止炎症导致的细胞死亡。对普通读者来说,信息是:维持肠道壁的紧密性可能在很大程度上依赖于“喂养”细胞的能量工厂,而不仅仅是抑制炎症。受TBZ启发的药物或靶向的硫化氢供体,有望在炎性肠病或肝病等病症中帮助稳定肠道屏障。然而,鉴于TBZ在无炎症情况下也可能增加渗漏,研究也强调了需将此类疗法与正确的情境和剂量相匹配的必要性。
引用: de Oliveira, J.P., van Sligtenhorst, M., Akkaya, C. et al. Hydrogen sulfide rescues IFNγ/TNFα-induced intestinal epithelial barrier dysfunction by enhancing oxidative phosphorylation. Sci Rep 16, 10208 (2026). https://doi.org/10.1038/s41598-026-40348-2
关键词: 肠道屏障, 硫化氢, 线粒体, 炎症, 上皮细胞