Clear Sky Science · it
Il solfuro di idrogeno ristabilisce la funzione di barriera epiteliale intestinale indotta da IFNγ/TNFα potenziando la fosforilazione ossidativa
Perché la parete sottile dell’intestino conta
L’epitelio intestinale è spesso spesso un singolo strato di cellule, eppure separa il mondo esterno presente nell’intestino dal resto dell’organismo. Quando questa barriera diventa «permeabile», batteri e tossine possono oltrepassarla, alimentando l’infiammazione non solo nel tratto digestivo ma anche nel fegato, nel cervello e in altri organi. Questo studio esplora come una piccola molecola contenente zolfo, che rilascia lentamente gas solfuro di idrogeno, possa proteggere questa fragile parete durante l’infiammazione aumentando la produzione di energia delle cellule.
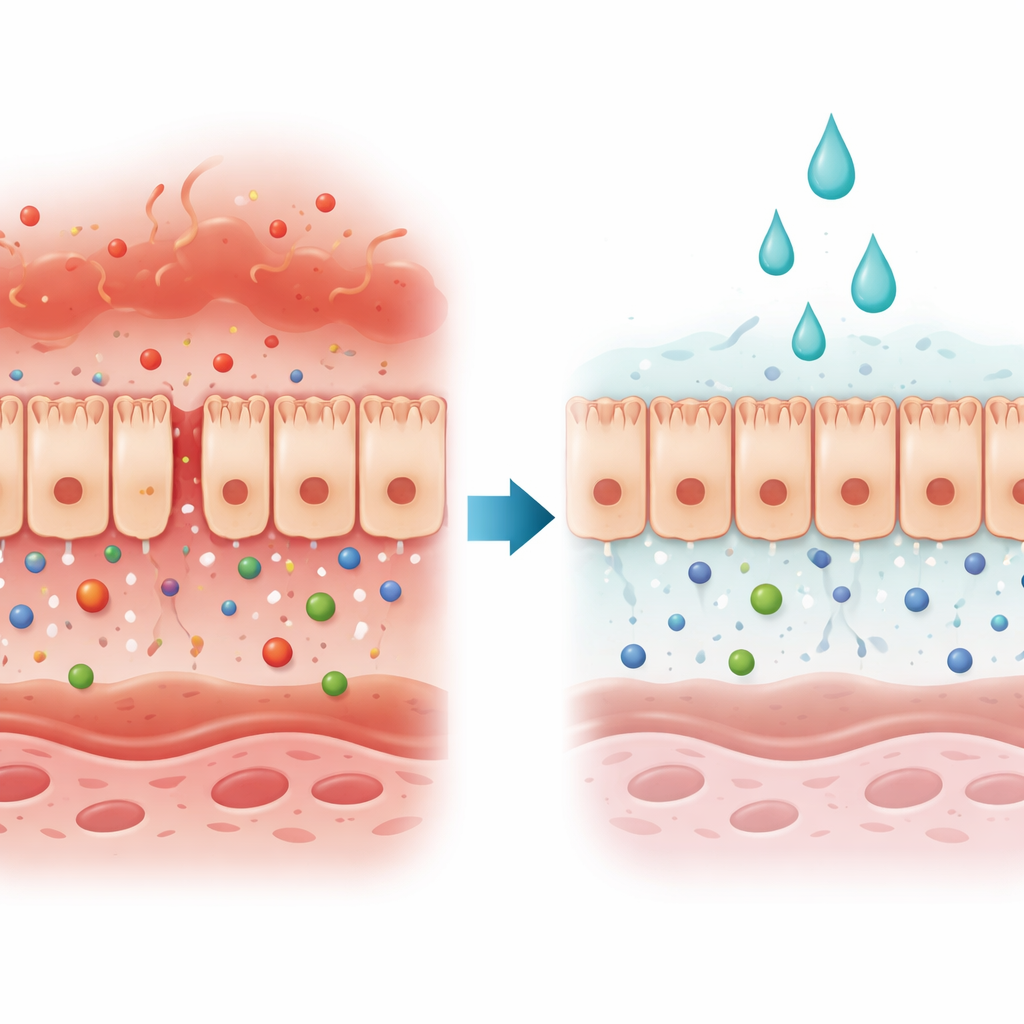
Il guardiano del corpo sotto attacco
Le cellule epiteliali intestinali formano un foglio continuo che funziona come un varco selettivo: blocca gli invasori nocivi lasciando passare nutrienti e acqua. In molte malattie intestinali e epatiche questo varco fallisce perché gli spazi tra le cellule si aprono o le cellule muoiono. Gli autori si sono concentrati su un tipo di danno guidato da due segnali immunitari, l’interferone‑gamma e il fattore di necrosi tumorale‑alpha, abbondanti nelle malattie infiammatorie intestinali. Questi segnali insieme indeboliscono la barriera e facilitano il passaggio di sostanze dall’intestino al flusso sanguigno.
Un donatore di zolfo con doppia personalità
I ricercatori hanno studiato la 4‑idrossitiobenzamide (TBZ), un composto capace di rilasciare solfuro di idrogeno, un gas che le nostre cellule producono a bassi livelli protettivi. In colture di strati cellulari intestinali e organoidi intestinali umani, la TBZ ha mostrato un effetto curioso e dipendente dal contesto. Da sola, aumentava leggermente la permeabilità fra le cellule. Ma quando la barriera era già danneggiata dai segnali infiammatori, la TBZ ne ristabiliva in larga parte la funzione. Riduceva i segni elettrici di rottura della barriera e riportava il passaggio di una molecola tracciante fluorescente verso valori più normali, pur non prevenendo la morte cellulare indotta dalle citochine.
Rifornire le centrali energetiche della cellula
Per capire come la TBZ esercitasse questa azione protettiva, il gruppo ha esaminato l’attività genica globale nelle cellule trattate. Hanno osservato che la TBZ attivava in modo marcato i geni collegati alla fosforilazione ossidativa — il processo mediante il quale i mitocondri, le «centrali elettriche» della cellula, producono la maggior parte dell’ATP. Componenti chiave del complesso mitocondriale IV e proteine di trasporto correlate risultavano sovraespressi, suggerendo che la TBZ modulasse la macchina energetica più che le vie infiammatorie classiche. Esperimenti successivi hanno confermato questo: in condizioni infiammatorie la TBZ aumentava la produzione mitocondriale di ATP senza modificare la glicolisi, indicando un incremento mirato della produzione di energia ad alta efficienza.
Quando i mitocondri vacillano, la barriera cede
Gli autori testarono poi se questo potenziamento energetico fosse necessario per la riparazione della barriera. Usarono l’azoturo di sodio, una sostanza che blocca il complesso IV nei mitocondri. A una dose che non uccideva le cellule, l’azoturo di sodio quasi azzerava la fosforilazione ossidativa lasciando in gran parte intatta la glicolisi. Nelle cellule infiammate trattate con TBZ, l’aggiunta di azoturo di sodio annullava l’effetto protettivo sulla barriera: la resistenza elettrica calava di nuovo e il tracciante fluorescente passava più facilmente. Anche se le cellule compensavano in parte spostandosi verso la glicolisi, l’ATP totale scese e la barriera non si riprese, collegando direttamente la respirazione mitocondriale intatta all’integrità della barriera.
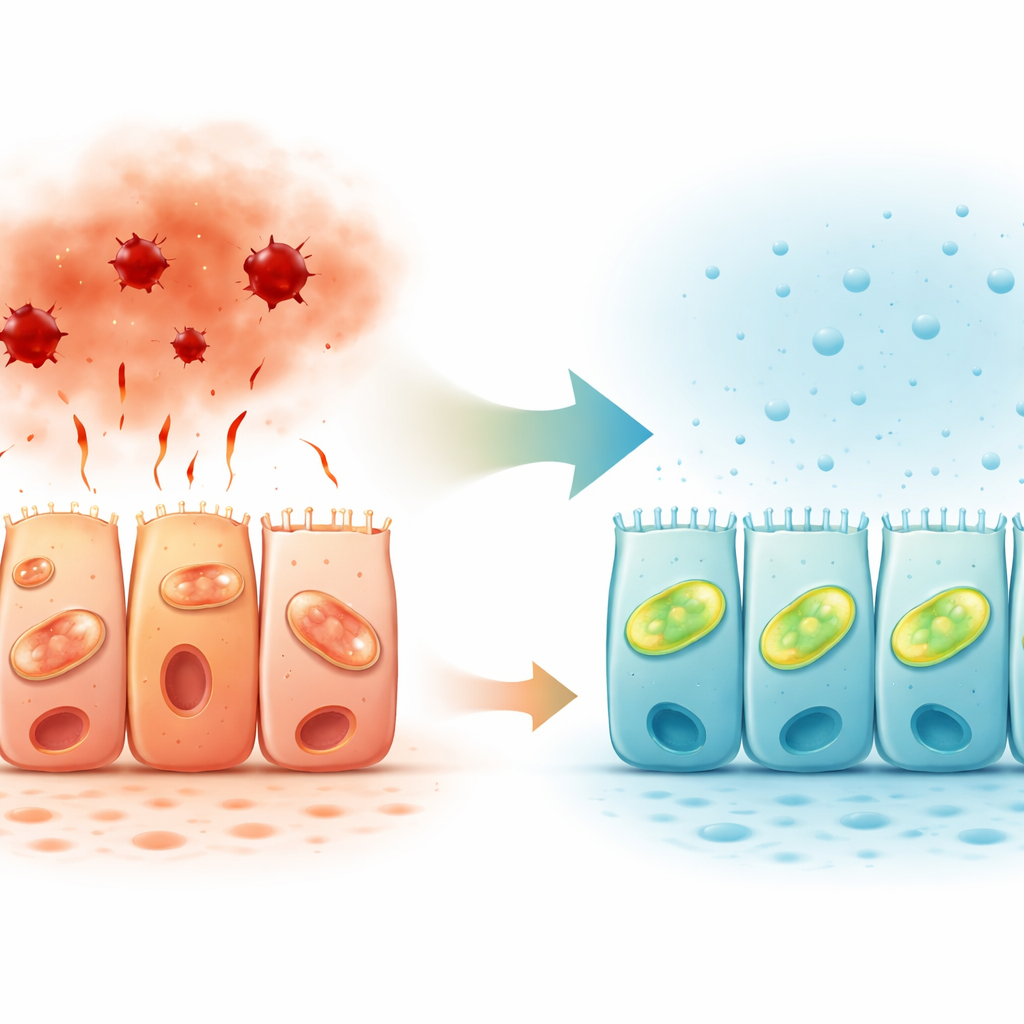
Segnali di gas naturali nel rivestimento intestinale
Analizzando tessuto colico umano, i ricercatori hanno anche mappato dove si trovano gli enzimi che producono solfuro di idrogeno. Due di questi enzimi risultavano espressi in modo più marcato nel lato apicale, rivolto verso il lume intestinale, delle cellule epiteliali, specialmente nel colon ascendente. Questo pattern polarizzato supporta l’idea che il solfuro di idrogeno agisca localmente in superficie, dove la barriera incontra il contenuto intestinale, modulando la risposta delle cellule allo stress. Unito a lavori precedenti che mostrano vie del solfuro di idrogeno ridotte nelle malattie infiammatorie intestinali, il risultato suggerisce che un segnalamento gassoso diminuito possa contribuire al fallimento della barriera nei pazienti.
Cosa significa per i trattamenti futuri
Complessivamente, lo studio dimostra che un composto che rilascia solfuro di idrogeno può rimediare a una barriera intestinale infiammata e permeabile aumentando la produzione di energia mitocondriale, specificamente attraverso la fosforilazione ossidativa, pur non prevenendo la morte cellulare infiammatoria. Per il pubblico non specialistico, il messaggio è che mantenere la tenuta della parete intestinale può dipendere tanto dal nutrire le «centrali» delle cellule quanto dal bloccare l’infiammazione. Farmaci ispirati alla TBZ, o donatori mirati di solfuro di idrogeno, potrebbero un giorno aiutare a stabilizzare la barriera intestinale in condizioni come le malattie infiammatorie intestinali o le patologie epatiche. Tuttavia, poiché la TBZ può anche aumentare la permeabilità in assenza di infiammazione, il lavoro sottolinea l’importanza di adattare tali terapie al contesto e al dosaggio appropriati.
Citazione: de Oliveira, J.P., van Sligtenhorst, M., Akkaya, C. et al. Hydrogen sulfide rescues IFNγ/TNFα-induced intestinal epithelial barrier dysfunction by enhancing oxidative phosphorylation. Sci Rep 16, 10208 (2026). https://doi.org/10.1038/s41598-026-40348-2
Parole chiave: barriera intestinale, solfuro di idrogeno, mitocondri, infiammazione, cellule epiteliali