Clear Sky Science · pt
O sulfeto de hidrogênio resgata a disfunção da barreira epitelial intestinal induzida por IFNγ/TNFα ao aumentar a fosforilação oxidativa
Por que a parede fina do intestino importa
O revestimento dos nossos intestinos tem apenas uma célula de espessura, ainda que separe o mundo externo presente no intestino do restante do corpo. Quando essa barreira se torna “permeável”, bactérias e toxinas podem atravessar, alimentando a inflamação não apenas no trato digestivo, mas também no fígado, no cérebro e em outros órgãos. Este estudo investiga como uma pequena molécula contendo enxofre, que libera lentamente gás sulfeto de hidrogênio, pode proteger essa parede frágil durante a inflamação ao aumentar a produção de energia das células.
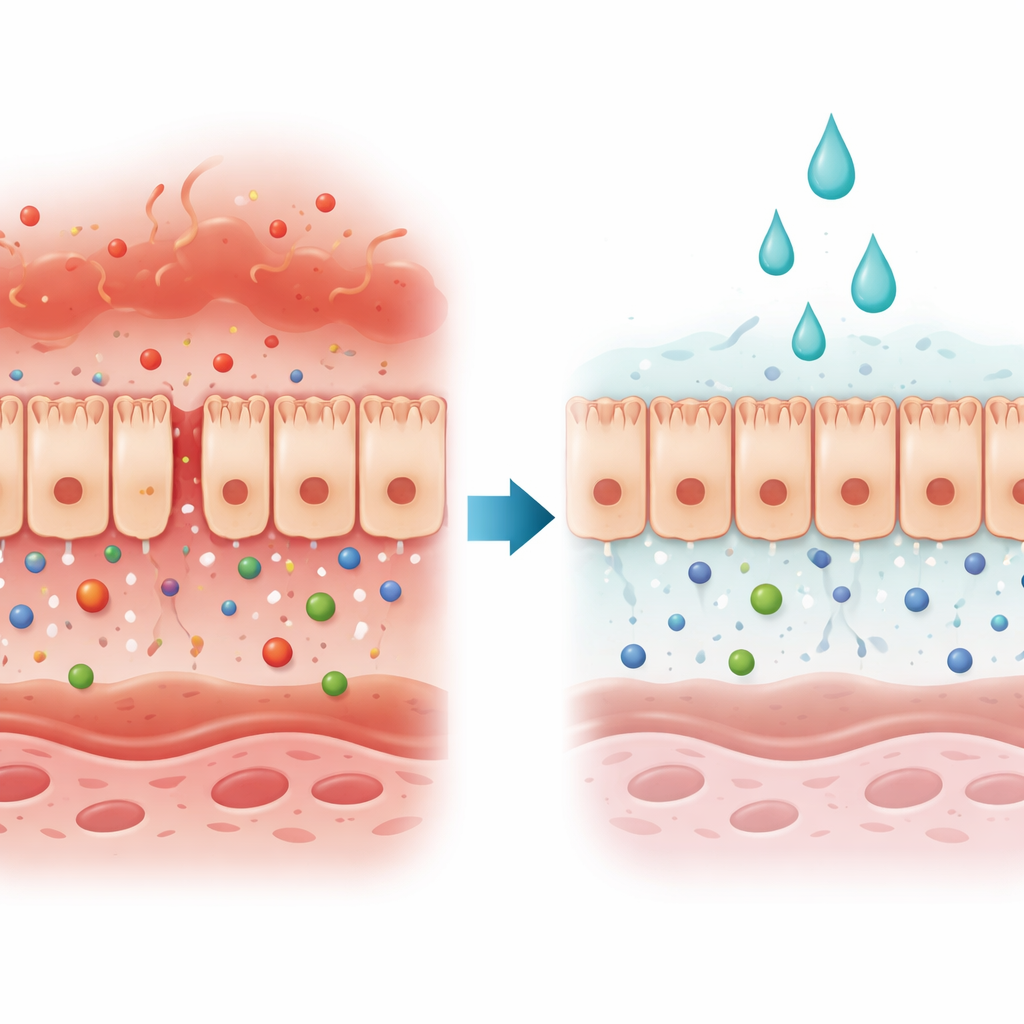
O guardião do corpo sob ataque
As células epiteliais intestinais formam uma camada contínua que funciona como um portão seletivo: bloqueia invasores nocivos enquanto permite a passagem de nutrientes e água. Em muitas doenças do intestino e do fígado, esse portão falha porque os espaços entre as células se abrem ou as células morrem. Os autores focaram em um tipo de lesão impulsionada por dois sinais imunes, interferon‑gama e fator de necrose tumoral‑alfa, abundantes na doença inflamatória intestinal. Juntos, esses sinais enfraquecem a barreira e facilitam que substâncias do intestino alcancem a corrente sanguínea.
Um doador de enxofre com dupla personalidade
Os pesquisadores estudaram 4‑hidroxitiobenzamida (TBZ), um composto que pode liberar sulfeto de hidrogênio, um gás que nossas próprias células também produzem em níveis baixos e protetores. Em camadas de células intestinais cultivadas em laboratório e em organoides intestinais humanos, o TBZ teve um efeito curioso e dependente do contexto. Por si só, aumentou ligeiramente a permeabilidade entre as células. Mas quando a barreira já estava danificada pelos sinais inflamatórios, o TBZ restaurou em grande parte sua função. Ele reduziu sinais elétricos de ruptura da barreira e aproximou a passagem de uma molécula traçadora fluorescente ao normal, mesmo sem impedir a morte celular desencadeada pelas citocinas.
Reforçando as usinas de energia das células
Para descobrir como o TBZ exerce essa ação protetora, a equipe examinou a atividade gênica global nas células tratadas. Eles descobriram que o TBZ ativou fortemente genes ligados à fosforilação oxidativa — o processo pelo qual as mitocôndrias, as “usinas” das células, produzem a maior parte do ATP. Componentes-chave do complexo IV mitocondrial e proteínas de transporte relacionadas foram regulados para cima, sugerindo que o TBZ ajustava a maquinaria energética em vez de atuar nas vias clássicas de inflamação. Experimentos complementares confirmaram isso: sob condições inflamatórias, o TBZ aumentou a produção mitocondrial de ATP sem alterar a glicólise, indicando um aumento direcionado na produção de energia de alta eficiência.
Quando as mitocôndrias falham, a barreira cede
Os autores então testaram se esse aumento de energia era necessário para a reparação da barreira. Eles usaram azida de sódio, um químico que bloqueia o complexo IV nas mitocôndrias. Em uma dose que não matou as células diretamente, a azida de sódio praticamente interrompeu a fosforilação oxidativa enquanto deixou a glicólise em grande parte intacta. Em células inflamadas tratadas com TBZ, a adição de azida de sódio apagou o efeito protetor na barreira: a resistência elétrica caiu novamente e o traçador fluorescente vazou com mais facilidade. Embora as células tenham deslocado parte do metabolismo para a glicólise em compensação, o ATP total diminuiu e a barreira não se recuperou, vinculando diretamente a respiração mitocondrial intacta à integridade da barreira.
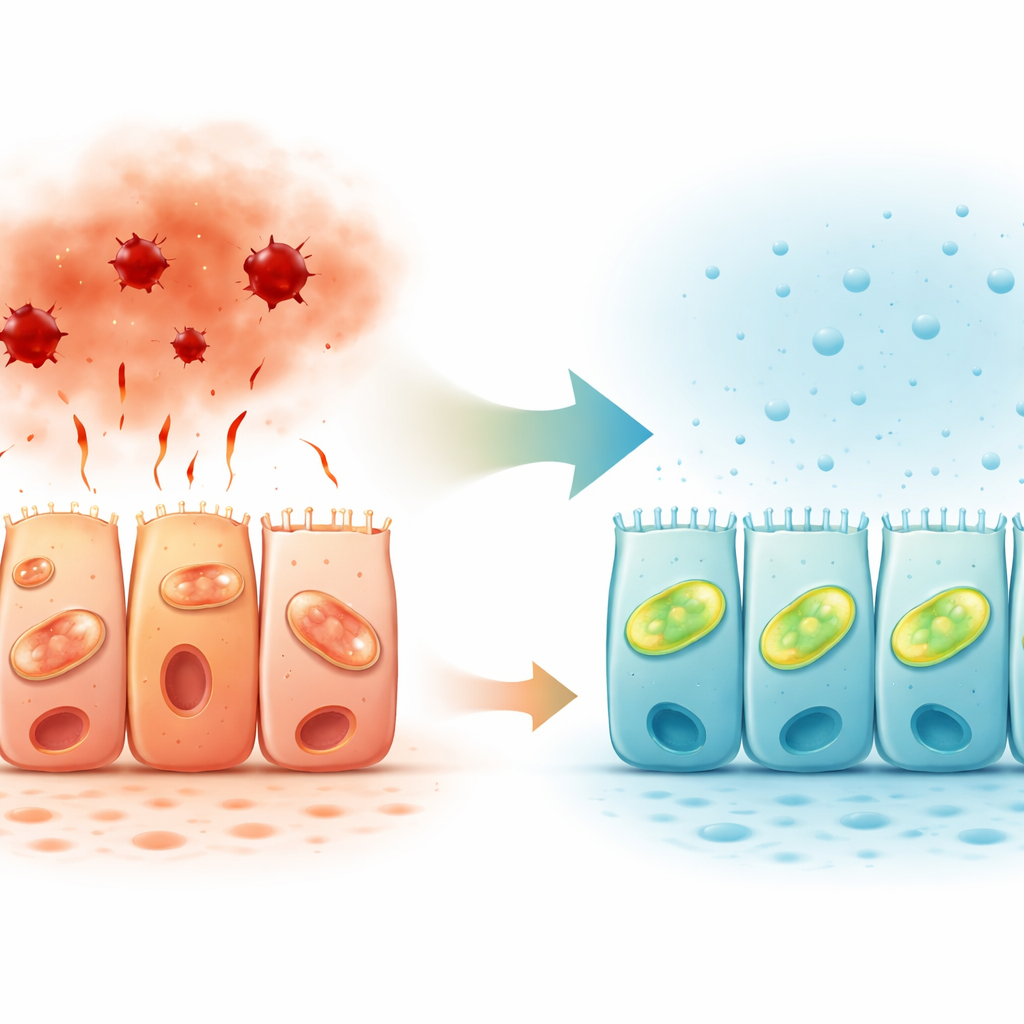
Sinais de gás natural no revestimento intestinal
Ao analisar tecido de cólon humano, os pesquisadores também mapearam onde as enzimas produtoras de sulfeto de hidrogênio são encontradas. Duas dessas enzimas foram mais fortemente expressas no lado superior, voltado para o lúmen intestinal, das células epiteliais, especialmente no cólon ascendente. Esse padrão polarizado apoia a ideia de que o sulfeto de hidrogênio atua localmente na superfície onde a barreira encontra o conteúdo intestinal, afinando como as células respondem ao estresse. Em conjunto com trabalhos anteriores que mostraram vias de sulfeto de hidrogênio reduzidas na doença inflamatória intestinal, os achados sugerem que a sinalização gasosa diminuída pode contribuir para a falha da barreira em pacientes.
O que isso significa para tratamentos futuros
No conjunto, o estudo mostra que um composto liberador de sulfeto de hidrogênio pode resgatar uma barreira intestinal inflamada e permeável ao aumentar a produção de energia mitocondrial, especificamente por meio da fosforilação oxidativa, embora não impeça a morte celular inflamatória em si. Para um leitor leigo, a mensagem é que manter a parede intestinal impermeável pode depender tanto de alimentar as usinas de energia das células quanto de bloquear a inflamação. Drogas inspiradas no TBZ, ou doadores direcionados de sulfeto de hidrogênio, podem um dia ajudar a estabilizar a barreira intestinal em condições como doença inflamatória intestinal ou doença hepática. Entretanto, porque o TBZ também pode aumentar a permeabilidade quando a inflamação está ausente, o trabalho ressalta a necessidade de ajustar cuidadosamente essas terapias ao contexto e à dose adequados.
Citação: de Oliveira, J.P., van Sligtenhorst, M., Akkaya, C. et al. Hydrogen sulfide rescues IFNγ/TNFα-induced intestinal epithelial barrier dysfunction by enhancing oxidative phosphorylation. Sci Rep 16, 10208 (2026). https://doi.org/10.1038/s41598-026-40348-2
Palavras-chave: barreira intestinal, sulfeto de hidrogênio, mitocôndrias, inflamação, células epiteliais