Clear Sky Science · he
גופרית מימית מצילה את תפקוד מחסום אפיתל המעי שנפגע על‑ידי IFNγ/TNFα על ידי הגברת הפוספורילציה החמצונית
מדוע דפנות המעי הדקות חשובות
השכבה שמצפה את המעי שלנו היא בעובי של תּא אחד בלבד, אך היא מפרידה בין העולם החיצון שבמעי לבין שאר הגוף. כאשר מחסום זה נעשה "דליף", חיידקים ורעלנים עלולים לחדור, ולהסעיף דלקת לא רק במערכת העיכול אלא גם בכבד, במוח ובאיברים אחרים. המחקר הזה בוחן כיצד מולקולה קטנה המכילה גופרית, שמשחררת באיטיות גז גופרית מימית, יכולה לעזור להגן על הקיר השברירי הזה בזמן דלקת על‑ידי חיזוק ייצור האנרגיה של התאים.
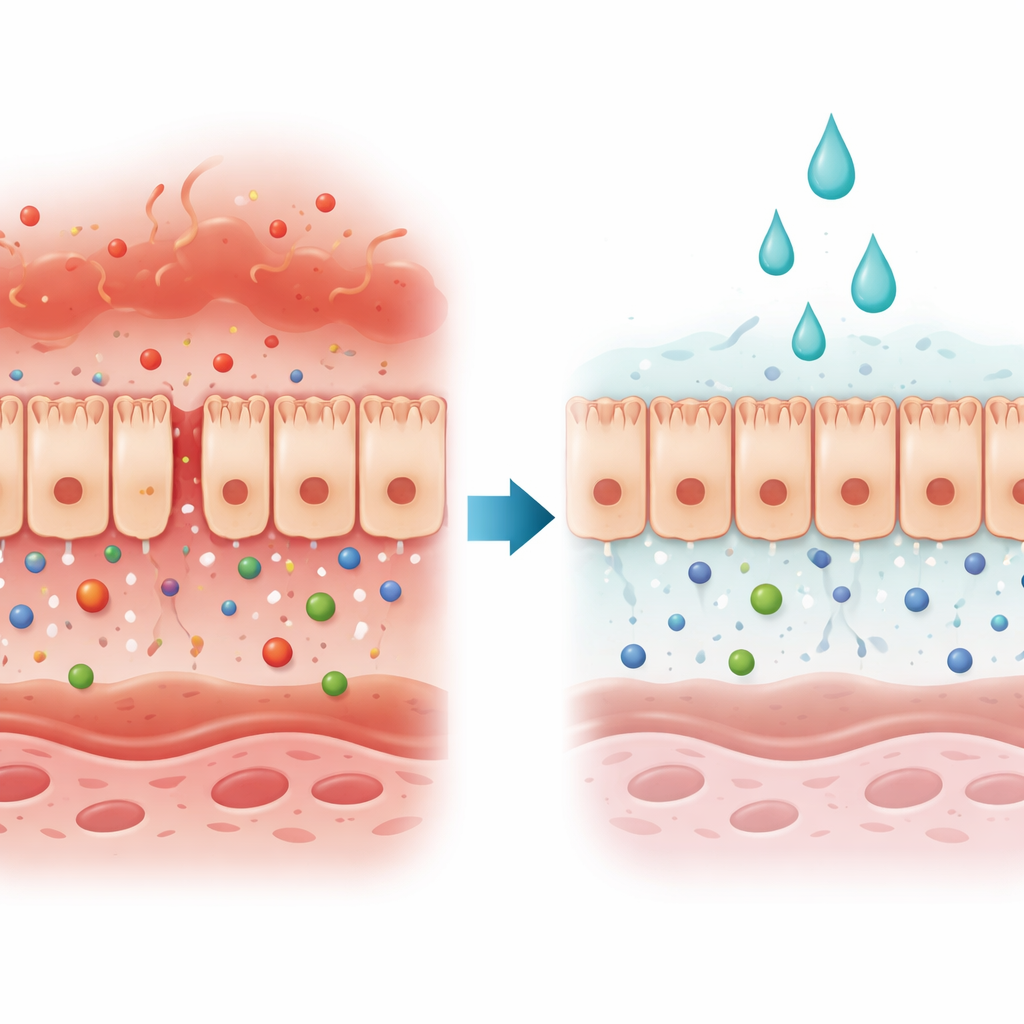
שומר השער של הגוף תחת מתקפה
תאי האפיתל של המעי יוצרים גיליון רציף הפועל כשער ברירתי: הוא חוסם פולשים מזיקים ובאותו זמן מאפשר מעבר של נוטריינטים ומים. במחלות רבות של המעי והכבד השער הזה נכשל בגלל שהמרווחים בין תאים נפתחים או שהתאים נמקים. החוקרים התמקדו בסוג של פגיעה המונעת על‑ידי שני אותות חיסוניים, אינטרפרון‑גמא וטומור נקרוזיס‑אלפא, שנמצאים בשפע במחלת מעי דלקתית. יחד, אותות אלה מחלישים את המחסום ומקלים על חומרים במעי להגיע למחזור הדם.
תורם גופרית עם אישיות כפולה
החוקרים בחנו את 4‑הידרוקסיתיובנזאמיד (TBZ), תרכובת שיכולה לשחרר גופרית מימית — גז שהגוף מייצר בקצבים נמוכים והגנתיים. במצעי תאים של שכבות אפיתל מעיים ובעוברי מעי אנושיים, ל‑TBZ היה אפקט מעניין התלוי בהקשר. כשהוא נמצא לבדו, הוא הגביר במעט את החדירות בין התאים. אך כאשר המחסום כבר נפגע על‑ידי אותות דלקתיים, TBZ החזיר במידה רבה את תפקודו. הוא צמצם סימנים חשמליים של קריסת המחסום והחזיר את מעבר מולקולת מעקב פלואורסצנטית לכיוון הנורמה, אף שלא מנע את מוות התאים שהעירויים גרמו לו.
הספקת תחנות הכוח של התא
כדי לגלות כיצד TBZ מפעיל את האפקט המגן הזה, הצוות בדק פעילות גנים גלובלית בתאים מטופלים. הם מצאו כי TBZ מדליק בעוצמה גנים הקשורים לפוספורילציה חמצונית — התהליך שבו המיטוכונדריה, "תחנות הכוח" של התא, מייצרות את רוב מולקולות ה‑ATP. רכיבים מרכזיים של קומפלקס IV המיטוכונדריאלי וחלבוני הובלה קשורים הועלו בביטוי, מה שמרמז ש‑TBZ מכוונן את מכונת האנרגיה ולא את מסלולי הדלקת הקלאסיים. ניסויים נוספים איששו זאת: בתנאי דלקת, TBZ הגביר ייצור ATP מיטוכונדריאלי ללא שינוי בגליקוליזה, מה שמצביע על עלייה ממוקדת בתפוקת אנרגיה בעלת יעילות גבוהה.
כשמיטוכונדריה נחלשות, המחסום נכשל
החוקרים בחנו האם הגברה זו של האנרגיה נחוצה לתיקון המחסום. הם השתמשו באזיד הנתרן, כימיקל החוסם את קומפלקס IV במיטוכונדריה. במינון שלא הרג את התאים באופן ישיר, אזיד הנתרן כמעט ועצר את הפוספורילציה החמצונית בעוד שהגליקוליזה נשארה ברובה שלמה. בתאים מדוללים שטופלו ב‑TBZ, הוספת אזיד הנתרן ביטלה את אפקט ההגנה על המחסום: ההתנגדות החשמלית ירדה שוב והמולקולת הפלואורסצנטית דלפה ביתר קלות. אף שהתאים הזיזו חלקית את מטבוליזםם לכיוון גליקוליזה כפיצוי, ה‑ATP הכולל ירד והמחסום לא התאושש, מה שמקשר בצורה ישירה נשימה מיטוכונדריאלית תקינה לשלמות המחסום.
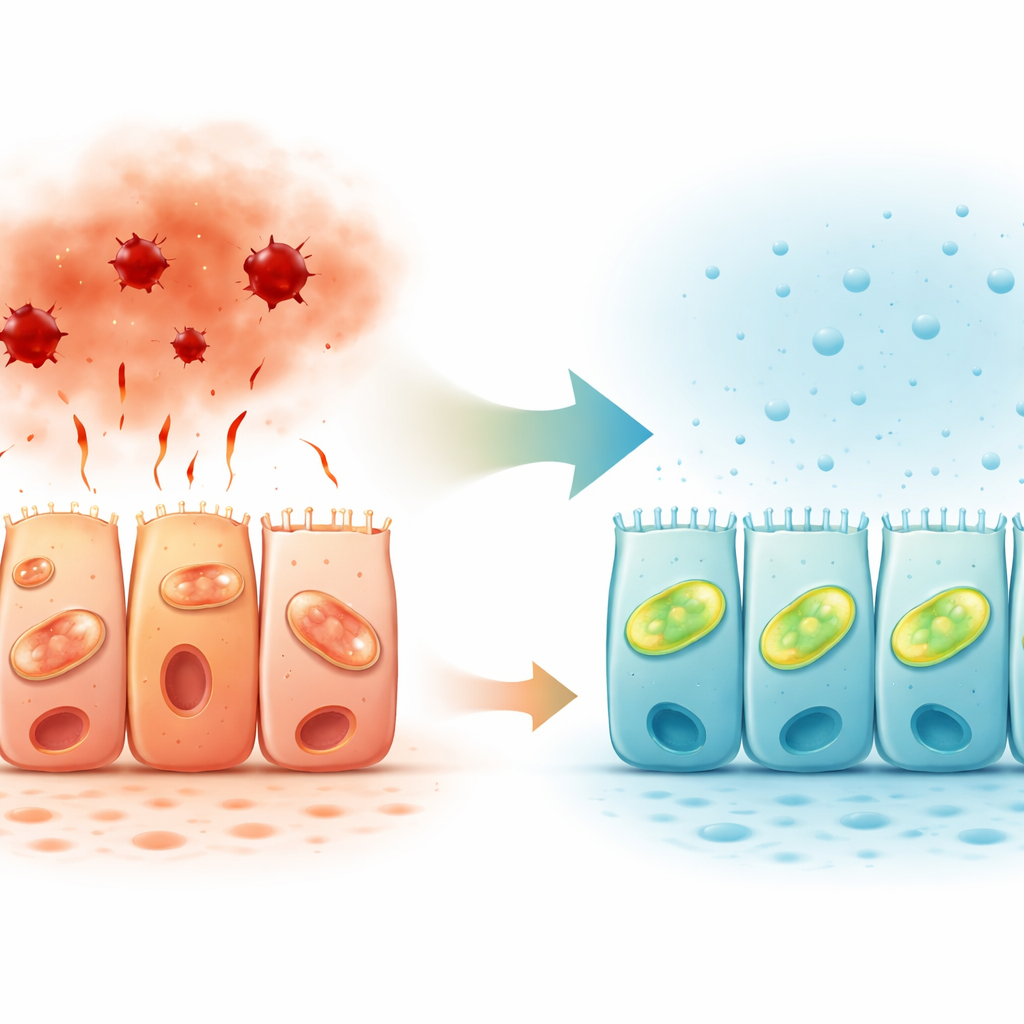
אותות גז טבעיים בציפוי המעי
בהסתכלות על רקמת קולון אנושית, החוקרים גם מיפו היכן נמצאים האנזימים המייצרים גופרית מימית. שני אנזימים כאלה הובעו בעוצמה רבה יותר בצד העליון הפונה למעי של התאים האפיתליים, במיוחד בקולון העולה. תבנית מקוטבת זו תומכת ברעיון שגופרית מימית פועלת מקומית על המשטח שבו המחסום נפגש עם תוכן המעי, ומכווננת את תגובת התאים ללחץ. בשילוב עם עבודות קודמות שהראו ירידה בדרכי גופרית מימית במחלת מעי דלקתית, הממצאים מציעים כי אותות גז מוחלשים עשויים לתרום לכשל המחסום בחולים.
מה המשמעות לטיפולים עתידיים
לסיכום, המחקר מראה כי תרכובת המשחררת גופרית מימית יכולה להציל מחסום מעי מדולל ונזוק על‑ידי הגברת ייצור האנרגיה המיטוכונדריאלי, במיוחד דרך הפוספורילציה החמצונית, אף שאינה עוצרת את מוות התאים הדלקתי עצמו. עבור הקורא הכללי, המסר הוא ששימור הדוק של דפנות המעי עשוי להיות תלוי לא פחות בהזנת תחנות הכוח של התאים מאשר בחסימת הדלקת. תרופות בהשראת TBZ, או תורמי גופרית מימית ממוקדים, עשויות יום אחד לסייע לייצב את מחסום המעי במצבים כמו מחלת מעי דלקתית או מחלות כבד. יחד עם זאת, כיוון ש‑TBZ יכול גם להגביר חדירות כשהדלקת אינה נוכחת, העבודה מדגישה גם את הצורך להתאים טיפולים אלה בקפידה להקשר ולמינון הנכונים.
ציטוט: de Oliveira, J.P., van Sligtenhorst, M., Akkaya, C. et al. Hydrogen sulfide rescues IFNγ/TNFα-induced intestinal epithelial barrier dysfunction by enhancing oxidative phosphorylation. Sci Rep 16, 10208 (2026). https://doi.org/10.1038/s41598-026-40348-2
מילות מפתח: מחסום מעי, גופרית מימית, מיטוכונדריה, דלקת, תאי אפיתל