Clear Sky Science · fr
Le sulfure d’hydrogène rétablit la dysfonction de la barrière épithéliale intestinale induite par IFNγ/TNFα en renforçant la phosphorylation oxydative
Pourquoi la fine paroi de l’intestin compte
L’épithélium intestinal ne fait qu’une cellule d’épaisseur, et pourtant il sépare le monde extérieur présent dans l’intestin du reste de l’organisme. Lorsque cette barrière devient « perméable », des bactéries et des toxines peuvent passer, alimentant l’inflammation non seulement dans le tube digestif mais aussi dans le foie, le cerveau et d’autres organes. Cette étude examine comment une petite molécule contenant du soufre, qui libère lentement du sulfure d’hydrogène gazeux, peut aider à protéger cette paroi fragile pendant l’inflammation en stimulant la production d’énergie des cellules.
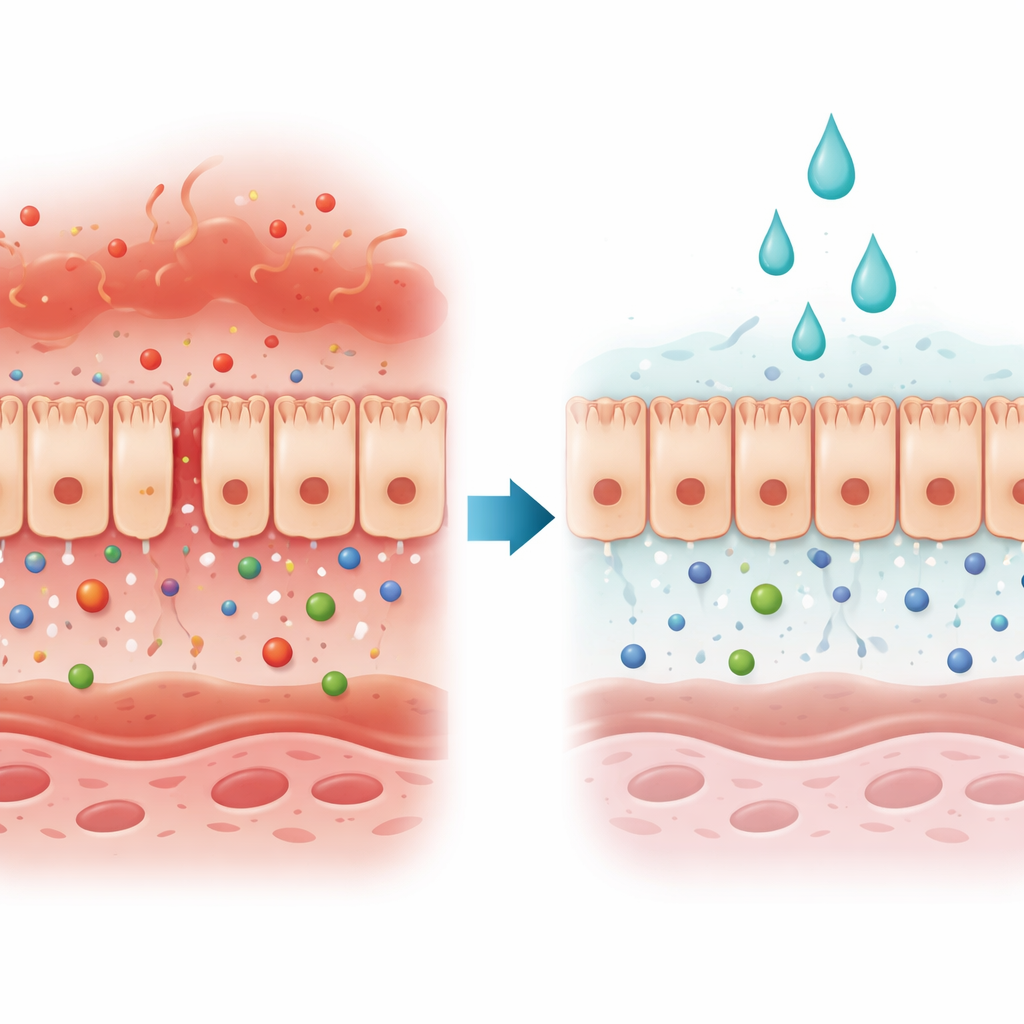
Le gardien du corps sous attaque
Les cellules épithéliales intestinales forment une nappe continue qui fonctionne comme une porte sélective : elle bloque les envahisseurs nocifs tout en laissant passer les nutriments et l’eau. Dans de nombreuses maladies intestinales et hépatiques, cette porte cède car les espaces entre les cellules s’ouvrent ou les cellules meurent. Les auteurs se sont concentrés sur un type de lésion induite par deux signaux immunitaires, l’interféron‑gamma et le facteur de nécrose tumorale alpha, abondants dans la maladie inflammatoire de l’intestin. Ensemble, ces signaux affaiblissent la barrière et facilitent le passage de substances de l’intestin vers le sang.
Un donneur de soufre à double visage
Les chercheurs ont étudié la 4‑hydroxithiobenzamide (TBZ), un composé capable de libérer du sulfure d’hydrogène, un gaz que nos propres cellules produisent aussi à faibles niveaux protecteurs. Dans des couches cellulaires intestinales cultivées en laboratoire et dans des organoïdes intestinaux humains, la TBZ a eu un effet curieux et dépendant du contexte. À elle seule, elle augmentait légèrement la perméabilité entre les cellules. Mais lorsque la barrière avait déjà été endommagée par des signaux inflammatoires, la TBZ en a rétabli la fonction en grande partie. Elle a réduit les signes électriques de rupture de la barrière et a ramené le passage d’un traceur fluorescent vers la normale, même si elle n’a pas empêché la mort cellulaire déclenchée par les cytokines.
Renforcer les centrales énergétiques cellulaires
Pour comprendre comment la TBZ exerce cette action protectrice, l’équipe a examiné l’expression génique globale dans les cellules traitées. Ils ont constaté que la TBZ activait fortement des gènes liés à la phosphorylation oxydative — le processus par lequel les mitochondries, les « centrales » de la cellule, produisent la majeure partie de l’ATP. Des composants clés du complexe IV mitochondrial et des protéines de transport associées étaient surexprimés, ce qui suggère que la TBZ réglait la machinerie énergétique plutôt que les voies inflammatoires classiques. Des expériences de suivi l’ont confirmé : en conditions inflammatoires, la TBZ augmentait la production mitochondriale d’ATP sans modifier la glycolyse, indiquant une hausse ciblée de la production d’énergie à haute efficacité.
Quand les mitochondries faiblissent, la barrière cède
Les auteurs ont ensuite testé si ce gain énergétique était nécessaire à la réparation de la barrière. Ils ont utilisé de l’azoture de sodium, un produit chimique qui bloque le complexe IV des mitochondries. À une dose qui ne tuait pas immédiatement les cellules, l’azoture a presque arrêté la phosphorylation oxydative tout en laissant la glycolyse pour l’essentiel intacte. Dans les cellules enflammées traitées par la TBZ, l’ajout d’azoture a annulé l’effet protecteur sur la barrière : la résistance électrique est retombée et le traceur fluorescent a de nouveau fuité plus facilement. Même si les cellules ont partiellement compensé par une bascule vers la glycolyse, l’ATP total a diminué et la barrière ne s’est pas rétablie, reliant directement la respiration mitochondriale intacte à l’intégrité de la barrière.
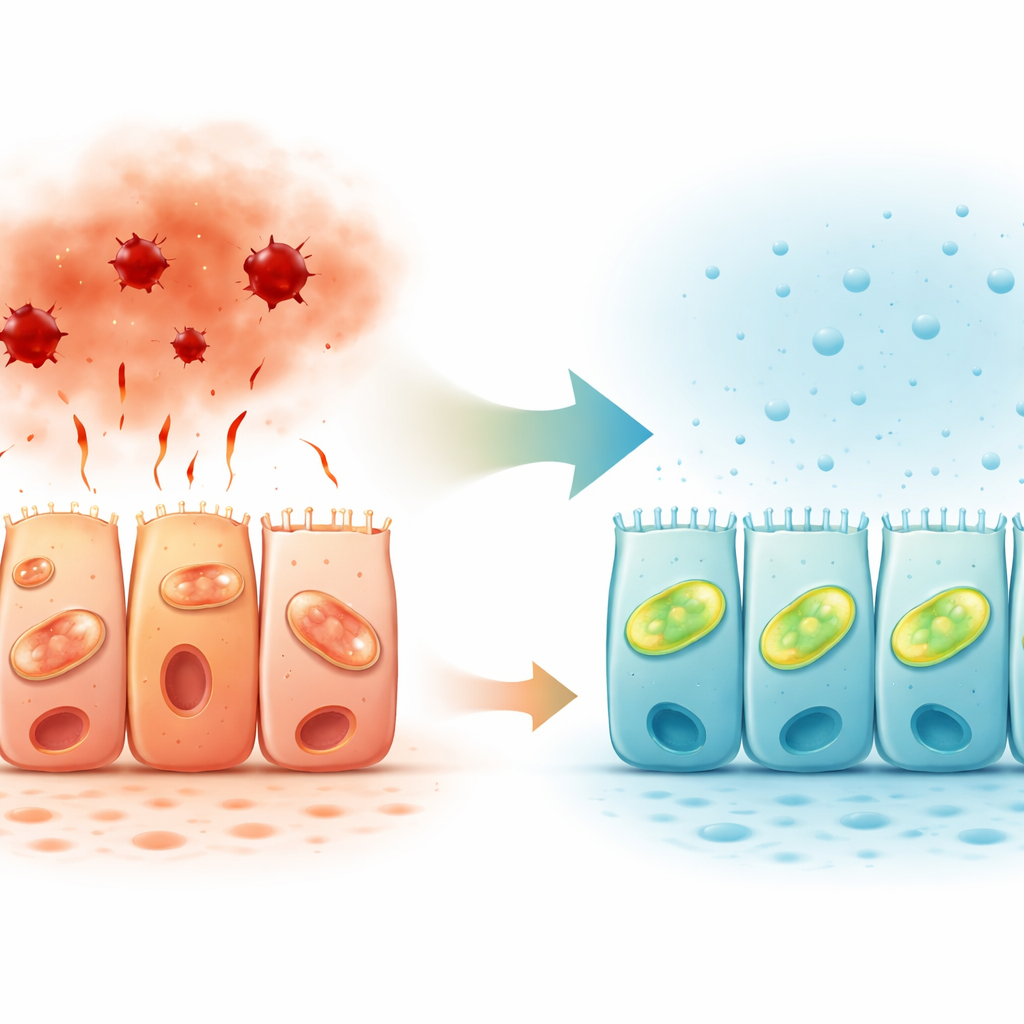
Des signaux gazeux naturels dans la muqueuse intestinale
En examinant des tissus du côlon humain, les chercheurs ont aussi cartographié où se trouvent les enzymes productrices de sulfure d’hydrogène. Deux de ces enzymes s’exprimaient le plus fortement du côté apical des cellules épithéliales, en contact avec la lumière intestinale, en particulier dans le côlon ascendant. Ce schéma polarisé soutient l’idée que le sulfure d’hydrogène agit localement à la surface où la barrière rencontre le contenu intestinal, réglant finement la réponse des cellules au stress. Associées à des travaux antérieurs montrant une baisse des voies du sulfure d’hydrogène dans la maladie inflammatoire de l’intestin, ces observations suggèrent qu’une signalisation gazeuse diminuée peut contribuer à la défaillance de la barrière chez les patients.
Ce que cela signifie pour les traitements futurs
Au total, l’étude montre qu’un composé libérant du sulfure d’hydrogène peut sauver une barrière intestinale enflammée et perméable en augmentant la production d’énergie mitochondriale, spécifiquement via la phosphorylation oxydative, même s’il n’empêche pas la mort cellulaire inflammatoire elle‑même. Pour un lecteur non spécialiste, le message est que le maintien de l’étanchéité de la paroi intestinale dépend peut‑être autant d’un bon approvisionnement des « centrales » cellulaires que du blocage de l’inflammation. Des médicaments inspirés par la TBZ, ou des donneurs de sulfure d’hydrogène ciblés, pourraient un jour aider à stabiliser la barrière intestinale dans des affections comme la maladie inflammatoire de l’intestin ou les maladies hépatiques. Toutefois, parce que la TBZ peut aussi augmenter la perméabilité en l’absence d’inflammation, le travail souligne aussi la nécessité d’adapter ces thérapies au bon contexte et à la bonne dose.
Citation: de Oliveira, J.P., van Sligtenhorst, M., Akkaya, C. et al. Hydrogen sulfide rescues IFNγ/TNFα-induced intestinal epithelial barrier dysfunction by enhancing oxidative phosphorylation. Sci Rep 16, 10208 (2026). https://doi.org/10.1038/s41598-026-40348-2
Mots-clés: barrière intestinale, sulfure d’hydrogène, mitochondries, inflammation, cellules épithéliales