Clear Sky Science · tr
Hidrojen sülfür, oksidatif fosforilasyonu artırarak IFNγ/TNFα kaynaklı bağırsak epitelyal bariyer disfonksiyonunu kurtarıyor
Bağırsağın İnce Duvarının Neden Önemi Var
Bağırsaklarımızın örtüsü yalnızca bir hücre kalınlığındadır, ancak bağırsaktaki dış dünyayı vücudun geri kalanından ayırır. Bu bariyer "sızdığında", bakteri ve toksinler geçiş yaparak sadece sindirim sisteminde değil karaciğer, beyin ve diğer organlarda da inflamasyonu tetikleyebilir. Bu çalışma, yavaşça hidrojen sülfür gazı salabilen küçük bir kükürt içeren molekülün, hücrelerin enerji üretimini artırarak inflamasyon sırasında bu hassas duvarı nasıl koruyabildiğini inceliyor.
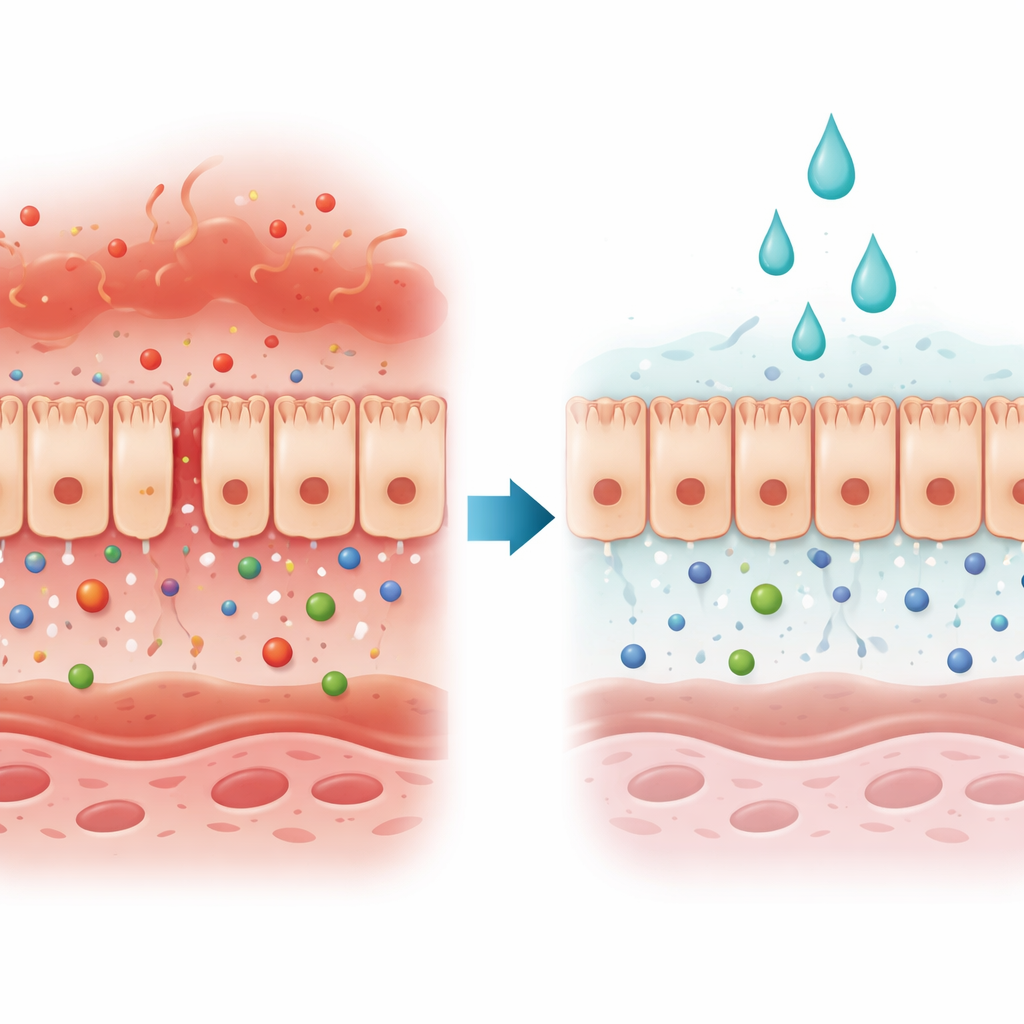
Vücudun Kapı Bekçisi Saldırı Altında
Bağırsak epitelyal hücreleri, zararlı istilacıları engellerken besin ve suyun geçmesine izin veren seçici bir kapı gibi kesintisiz bir tabaka oluşturur. Birçok bağırsak ve karaciğer hastalığında bu kapı, hücreler arasındaki boşluklar açıldığında veya hücreler öldüğünde işlevini yitirir. Yazarlar, inflamatuar bağırsak hastalığında bol bulunan iki bağışıklık sinyali, interferon‑gamma ve tümör nekroz faktör‑alfa tarafından yönlendirilen bir yaralanma türüne odaklandı. Bu sinyaller birlikte bariyeri zayıflatarak bağırsaktaki maddelerin kana ulaşmasını kolaylaştırır.
İki Yüzlü Bir Kükürt Verici
Araştırmacılar, hidrojen sülfür salabilen 4‑hidroksitiobenzamid (TBZ) bileşiğini incelediler; bu gazı bizim hücrelerimiz de düşük, koruyucu düzeylerde üretir. Laboratuvarda yetiştirilen bağırsak hücre katmanları ve insan bağırsak organoidlerinde TBZ ilginç ve bağlama bağlı bir etki gösterdi. Tek başına, hücreler arasındaki sızmayı hafifçe artırdı. Ancak bariyer zaten inflamatuar sinyallerle zarar görmüşse TBZ işlevi büyük ölçüde geri getirdi. Elektriksel bariyer bozulması işaretlerini azalttı ve floresan izleyici molekülün geçişini normale yaklaştırdı; buna rağmen sitokinlerin tetiklediği hücre ölümünü engellemedi.
Hücrenin Enerji Santrallerini Güçlendirmek
TBZ’nin bu koruyucu etkiyi nasıl gösterdiğini ortaya çıkarmak için ekip, tedavi edilmiş hücrelerde küresel gen aktivitesini inceledi. TBZ’nin oksidatif fosforilasyonla ilişkili genleri güçlü şekilde açtığını buldular — mitokondrilerin, hücrenin ATP enerjisinin çoğunu ürettiği süreç. Mitokondriyal kompleks IV’ün ana bileşenleri ve ilişkili taşıyıcı proteinler yukarı düzenlendi; bu da TBZ’nin klasik inflamasyon yollarından çok enerji mekanizmasını ayarladığını düşündürüyor. İzleme deneyleri bunu doğruladı: inflamatuar koşullar altında TBZ, glikolizi değiştirmeden mitokondrial ATP üretimini artırdı; bu da yüksek verimli enerji çıktısında hedefli bir artışı işaret ediyor.
Mitokondriler Arızalandığında Bariyer Çöküyor
Yazarlar sonra bu enerji artışının bariyer onarımı için gerekli olup olmadığını test ettiler. Mitokondrilerde kompleks IV’ü engelleyen sodyum azid adlı bir kimyasal kullandılar. Hücreleri doğrudan öldürmeyen bir dozda, sodyum azid oksidatif fosforilasyonu neredeyse kapatırken glikolizi büyük ölçüde korudu. İnflamasyonlu hücrelerde TBZ ile birlikte sodyum azid eklenmesi, koruyucu bariyer etkisini ortadan kaldırdı: elektriksel direnç tekrar düştü ve floresan izleyici daha kolay sızdı. Hücreler telafi amacıyla bir ölçüde glikolize kaymış olsa da toplam ATP düştü ve bariyer toparlanmadı; bu, sağlam mitokondriyal solunumu bariyer bütünlüğüne doğrudan bağladı.
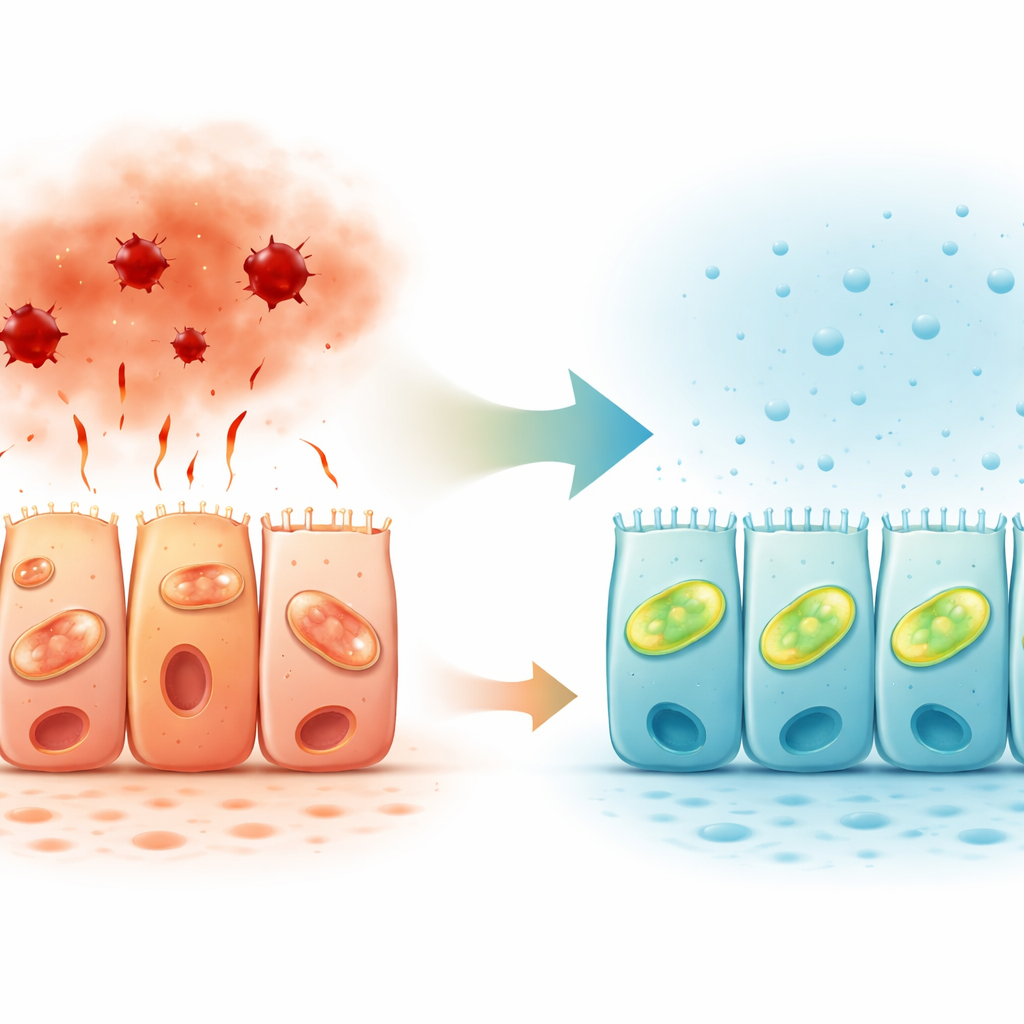
Bağırsak Örtüsünde Doğal Gaz Sinyalleri
İnsan kolon dokusuna bakıldığında araştırmacılar ayrıca hidrojen sülfür üreten enzimlerin nerede bulunduğunu haritaladılar. Bu enzimlerden ikisi, özellikle çıkan kolonda, epitelyal hücrelerin üstteki, bağırsak boşluğuna bakan tarafında en güçlü şekilde eksprese ediliyordu. Bu kutuplaşmış desen, hidrojen sülfürün bariyerin bağırsak içeriğiyle buluştuğu yüzeyde yerel olarak hareket ettiğini ve hücrelerin strese yanıtını ince ayarladığını destekliyor. Önceki çalışmaların inflamatuar bağırsak hastalığında hidrojen sülfür yollarının azaldığını göstermesiyle birlikte, bulgular gaz sinyallemesinin azalmasının hastalarda bariyer çöküşüne katkıda bulunabileceğini öne sürüyor.
Gelecek Tedaviler İçin Ne Anlama Geliyor
Toplamda çalışma, hidrojen sülfür salan bir bileşiğin inflamasyonla sızan bağırsak bariyerini oksidatif fosforilasyon yoluyla mitokondriyal enerji üretimini artırarak kurtarabileceğini gösteriyor; buna rağmen inflamatuar kaynaklı hücre ölümünü durdurmuyor. Halk için mesaj şudur: bağırsağın sıkı kalması, hücrelerin enerji santrallerine besin sağlamaya en az inflamasyonu engellemek kadar bağlı olabilir. TBZ’den esinlenen ilaçlar veya hedeflenmiş hidrojen sülfür bağışçıları bir gün inflamatuar bağırsak hastalığı veya karaciğer hastalığı gibi durumlarda bağırsak bariyerini stabil hale getirmeye yardımcı olabilir. Ancak TBZ’nin inflamasyon yokken de sızmayı artırabilmesi nedeniyle, bu tür tedavilerin doğru bağlama ve doza dikkatle eşleştirilmesi gerektiğini vurguluyor.
Atıf: de Oliveira, J.P., van Sligtenhorst, M., Akkaya, C. et al. Hydrogen sulfide rescues IFNγ/TNFα-induced intestinal epithelial barrier dysfunction by enhancing oxidative phosphorylation. Sci Rep 16, 10208 (2026). https://doi.org/10.1038/s41598-026-40348-2
Anahtar kelimeler: bağırsak bariyeri, hidrojen sülfür, mitokondri, inflamasyon, epitelyal hücreler