Clear Sky Science · es
El sulfuro de hidrógeno restaura la disfunción de la barrera epitelial intestinal inducida por IFNγ/TNFα al potenciar la fosforilación oxidativa
Por qué importa la delgada pared intestinal
El revestimiento de nuestros intestinos tiene apenas un solo estrato celular, y sin embargo separa el mundo exterior presente en el intestino del resto del cuerpo. Cuando esta barrera se vuelve “permeable”, bacterias y toxinas pueden filtrarse, alimentando la inflamación no solo en el tracto digestivo sino también en el hígado, el cerebro y otros órganos. Este estudio explora cómo una pequeña molécula que contiene azufre, y que libera lentamente gas sulfuro de hidrógeno, puede ayudar a proteger esa pared frágil durante la inflamación al aumentar la producción de energía de las células.
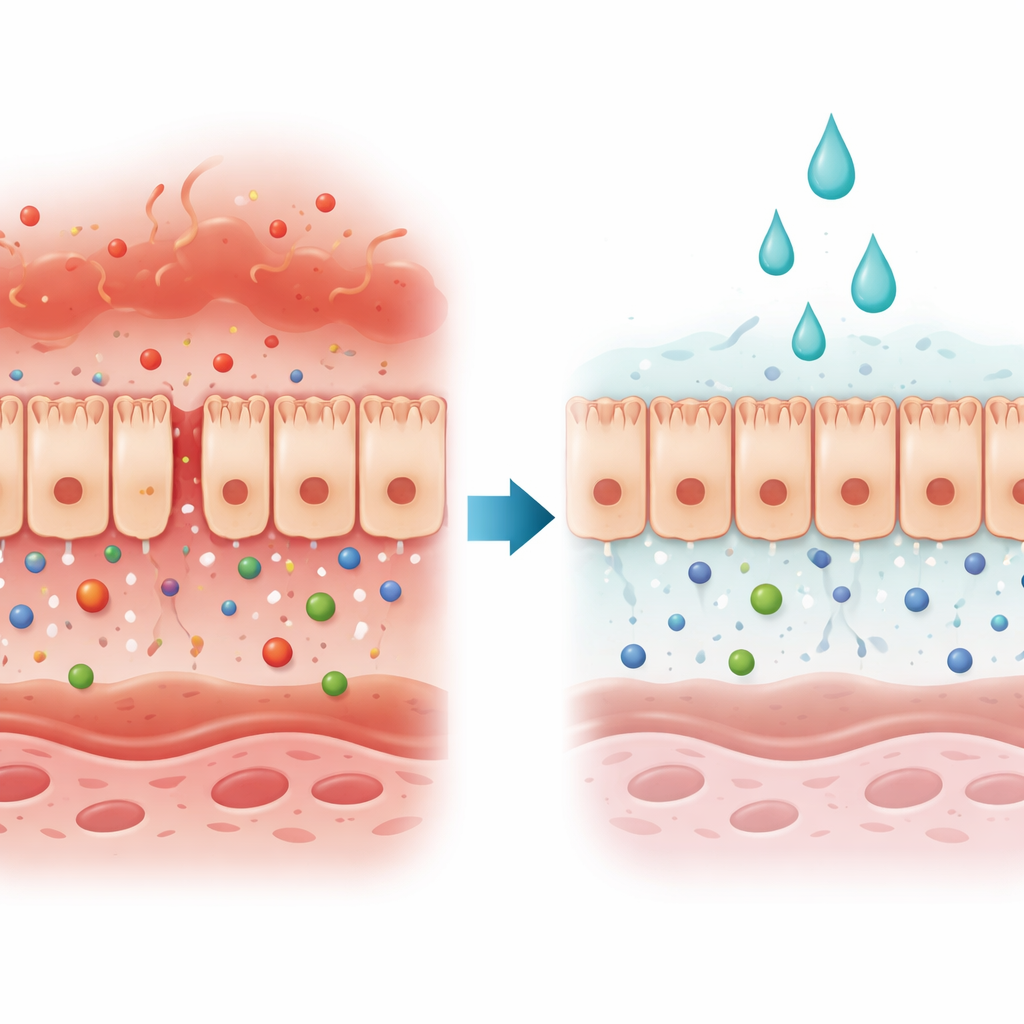
El guardián del cuerpo bajo ataque
Las células epiteliales intestinales forman una lámina continua que actúa como una puerta selectiva: bloquea invasores dañinos mientras permite el paso de nutrientes y agua. En muchas enfermedades intestinales y hepáticas, esta puerta falla porque se abren los espacios entre las células o porque las células mueren. Los autores se centraron en un tipo de daño impulsado por dos señales inmunes, interferón‑gamma y factor de necrosis tumoral‑alfa, que abundan en la enfermedad inflamatoria intestinal. En conjunto, estas señales debilitan la barrera y facilitan que sustancias del intestino lleguen al torrente sanguíneo.
Un donante de azufre con doble cara
Los investigadores estudiaron 4‑hidroxitiobenzamida (TBZ), un compuesto que puede liberar sulfuro de hidrógeno, un gas que nuestras propias células también generan a niveles bajos y protectores. En capas de células intestinales cultivadas en laboratorio y en organoides intestinales humanos, TBZ presentó un efecto curioso y dependiente del contexto. Por sí solo, aumentó ligeramente la permeabilidad entre células. Pero cuando la barrera ya había sido dañada por señales inflamatorias, TBZ restauró en gran medida su función. Redujo las señales eléctricas de ruptura de barrera y devolvió el paso de una molécula trazadora fluorescente hacia valores cercanos a lo normal, aunque no evitó la muerte celular desencadenada por las citoquinas.
Poniendo en marcha las centrales energéticas celulares
Para descubrir cómo ejerce TBZ esta acción protectora, el equipo examinó la actividad génica global en las células tratadas. Encontraron que TBZ activó fuertemente genes vinculados a la fosforilación oxidativa —el proceso por el cual las mitocondrias, las “centrales energéticas” de la célula, producen la mayor parte del ATP. Se reguló al alza componentes clave del complejo mitocondrial IV y proteínas de transporte relacionadas, lo que sugiere que TBZ modulaba la maquinaria energética más que las vías clásicas de inflamación. Experimentos de seguimiento confirmaron esto: en condiciones inflamatorias, TBZ aumentó la producción mitocondrial de ATP sin cambiar la glucólisis, indicando un incremento específico en la producción de energía de alta eficiencia.
Cuando las mitocondrias fallan, la barrera cede
Los autores probaron entonces si este impulso energético era necesario para la reparación de la barrera. Usaron azida de sodio, un químico que bloquea el complejo IV mitocondrial. A una dosis que no mató las células de manera inmediata, la azida de sodio casi extinguió la fosforilación oxidativa mientras dejaba la glucólisis en gran medida intacta. En células inflamadas tratadas con TBZ, la adición de azida de sodio eliminó el efecto protector sobre la barrera: la resistencia eléctrica volvió a caer y el trazador fluorescente se filtró con mayor facilidad. Aunque las células compensaron en parte con un aumento de la glucólisis, el ATP total descendió y la barrera no se recuperó, vinculando directamente la respiración mitocondrial intacta con la integridad de la barrera.
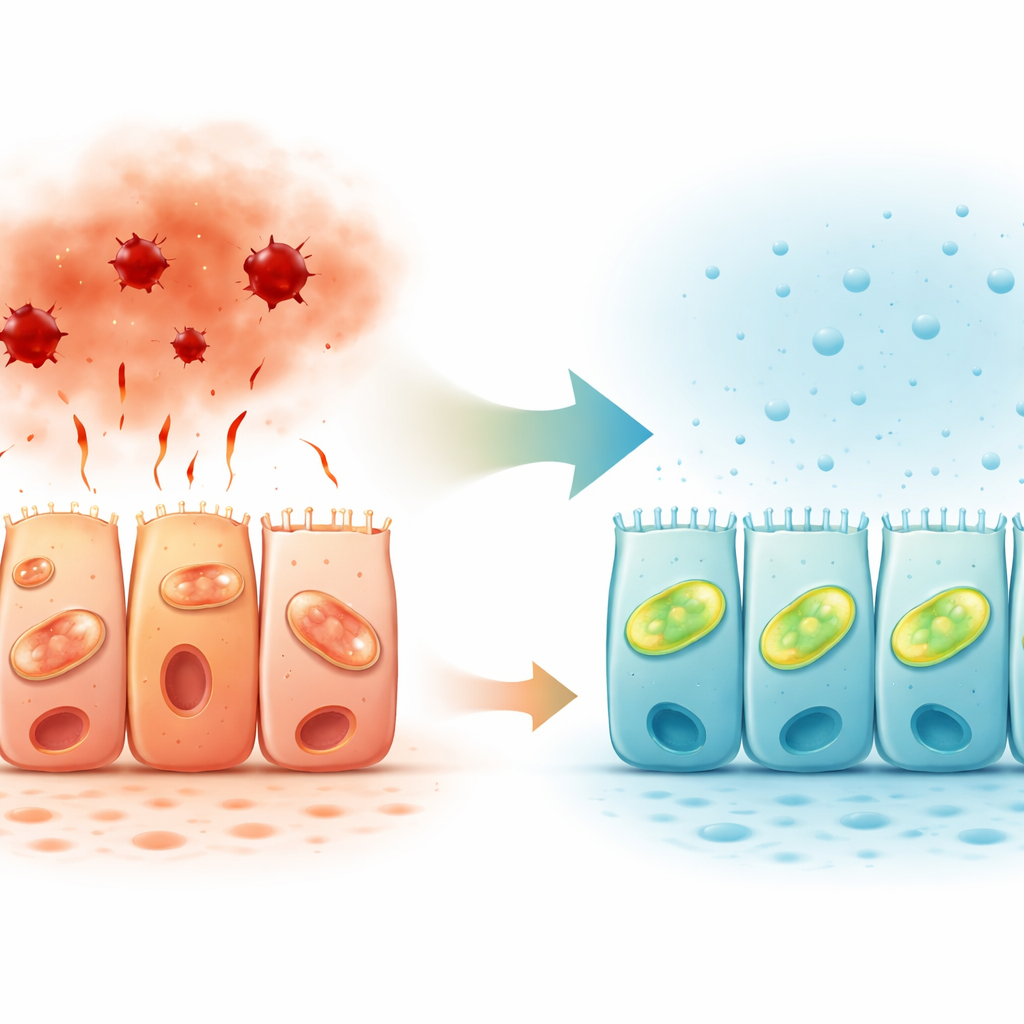
Señales de gas natural en el revestimiento intestinal
Al analizar tejido de colon humano, los investigadores también cartografiaron dónde se localizan las enzimas que producen sulfuro de hidrógeno. Dos de esas enzimas se expresaron con mayor intensidad en el lado superior de las células epiteliales, el que da al lumen intestinal, especialmente en el colon ascendente. Este patrón polarizado respalda la idea de que el sulfuro de hidrógeno actúa localmente en la superficie donde la barrera se encuentra con el contenido intestinal, afinando la respuesta celular al estrés. Combinado con trabajos previos que muestran vías de sulfuro de hidrógeno reducidas en la enfermedad inflamatoria intestinal, los hallazgos sugieren que una señalización gaseosa disminuida puede contribuir a la falla de la barrera en los pacientes.
Qué significa esto para tratamientos futuros
En conjunto, el estudio muestra que un compuesto liberador de sulfuro de hidrógeno puede rescatar una barrera intestinal inflamada y permeable al aumentar la producción mitocondrial de energía, específicamente mediante la fosforilación oxidativa, aun cuando no detiene la muerte celular inflamatoria en sí. Para el público general, el mensaje es que mantener la hermeticidad de la pared intestinal puede depender tanto de alimentar a las centrales energéticas celulares como de bloquear la inflamación. Medicamentos inspirados en TBZ, o donantes de sulfuro de hidrógeno dirigidos, podrían algún día ayudar a estabilizar la barrera intestinal en condiciones como la enfermedad inflamatoria intestinal o la enfermedad hepática. Sin embargo, dado que TBZ también puede aumentar la permeabilidad cuando no hay inflamación, el trabajo subraya la necesidad de ajustar cuidadosamente estas terapias al contexto y la dosis apropiados.
Cita: de Oliveira, J.P., van Sligtenhorst, M., Akkaya, C. et al. Hydrogen sulfide rescues IFNγ/TNFα-induced intestinal epithelial barrier dysfunction by enhancing oxidative phosphorylation. Sci Rep 16, 10208 (2026). https://doi.org/10.1038/s41598-026-40348-2
Palabras clave: barrera intestinal, sulfuro de hidrógeno, mitocondrias, inflamación, células epiteliales