Clear Sky Science · nl
Waterstofsulfide herstelt IFNγ/TNFα-geïnduceerde disfunctie van de intestinale epitheellaag door oxidatieve fosforylering te versterken
Waarom de dunne wand van de darm ertoe doet
De bekleding van onze darmen bestaat uit slechts één cellaag, en toch scheidt zij de buitenwereld in onze darm van de rest van het lichaam. Als deze barrière “lekkend” wordt, kunnen bacteriën en toxines binnendringen en ontstekingen aanwakkeren, niet alleen in het spijsverteringskanaal maar ook in de lever, de hersenen en andere organen. Deze studie onderzoekt hoe een kleine zwavelhoudende verbinding, die langzaam waterstofsulfidegas afgeeft, deze kwetsbare wand tijdens ontsteking kan beschermen door de energieproductie van de cellen te versterken.
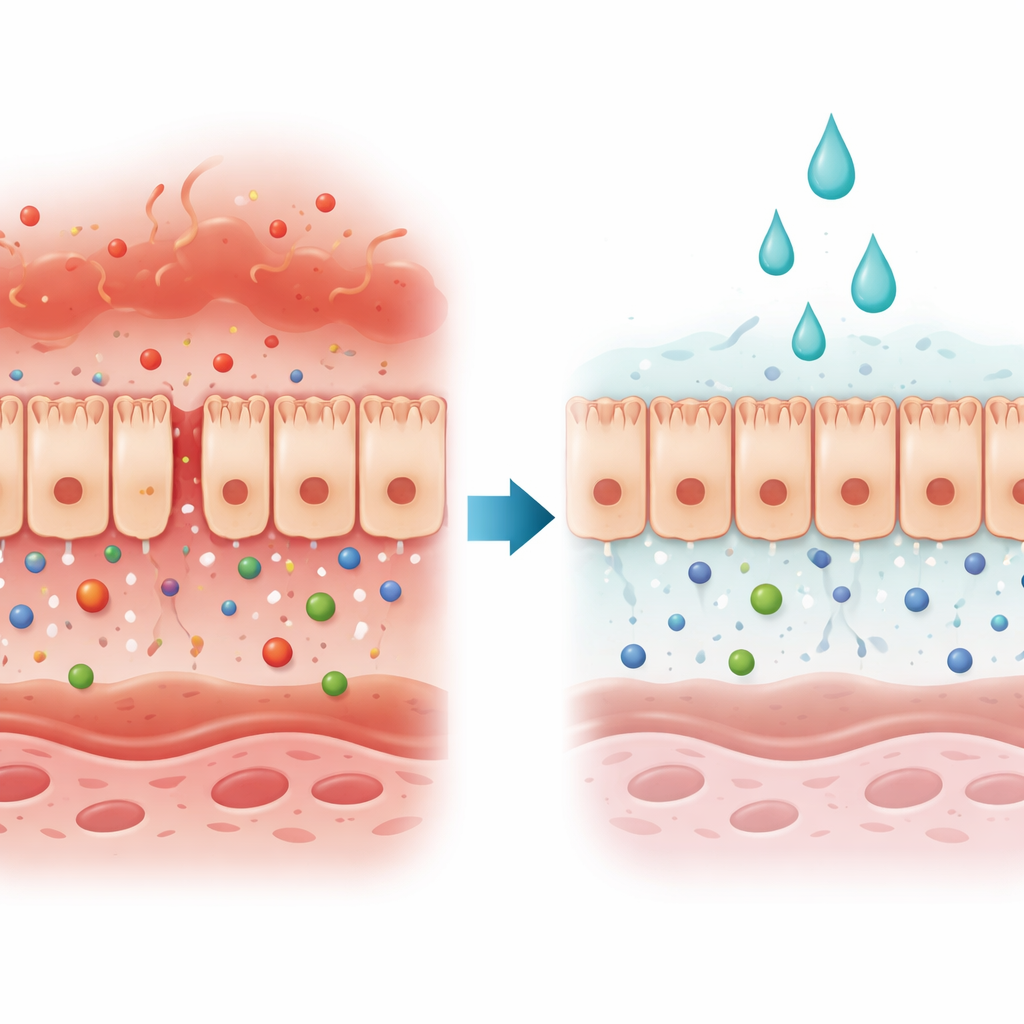
De poortwachter van het lichaam onder aanval
Intestinale epitheelcellen vormen een onafgebroken laag die als een selectieve poort functioneert: ze houdt schadelijke indringers tegen en laat voedingsstoffen en water passeren. In veel darmaandoeningen en leverziekten faalt deze poort omdat de ruimtes tussen de cellen wijder worden of omdat cellen afsterven. De auteurs richtten zich op een type schade dat wordt aangedreven door twee immuunsignalen, interferon‑gamma en tumor necrose factor‑alpha, die overvloedig aanwezig zijn bij inflammatoire darmziekte. Gezamenlijk verzwakken deze signalen de barrière en maken ze het makkelijker voor stoffen in de darm om de bloedbaan te bereiken.
Een zwaveldonor met een tweeslachtig karakter
De onderzoekers bestudeerden 4‑hydroxithiobenzamide (TBZ), een verbinding die waterstofsulfide kan afgeven, een gas dat onze eigen cellen ook in lage, beschermende concentraties produceren. In in het laboratorium gekweekte intestinale cellagen en humane intestinale organoïden had TBZ een opmerkelijk contextafhankelijk effect. Op zichzelf vergrootte het de doorlaatbaarheid tussen de cellen licht. Maar wanneer de barrière al was beschadigd door ontstekingssignalen, herstelde TBZ grotendeels de functie. Het verminderde elektrische tekenen van barrièrefalen en bracht de doorgang van een fluorescerende tracermolecule weer dichter bij normaal, ook al voorkwam het niet het celdood die door de cytokinen werd veroorzaakt.
De energiecentrales van de cel opschalen
Om te achterhalen hoe TBZ deze beschermende werking tot stand brengt, bekeek het team de globale genactiviteit in behandelde cellen. Ze vonden dat TBZ sterk genen activeerde die gekoppeld zijn aan oxidatieve fosforylering — het proces waarbij mitochondriën, de “energiecentrales” van de cel, het merendeel van ATP produceren. Belangrijke componenten van mitochondriaal complex IV en gerelateerde transporteiwitten waren hoger tot expressie gebracht, wat suggereert dat TBZ de energiemachines afstemt in plaats van klassieke ontstekingsroutes. Vervolgexperimenten bevestigden dit: onder ontstekingscondities verhoogde TBZ de mitochondriale ATP-productie zonder glycolyse te veranderen, wat wijst op een gerichte stijging van energie met hoge efficiëntie.
Als mitochondriën falen, faalt de barrière
De auteurs testten vervolgens of deze energieboost nodig was voor het herstel van de barrière. Ze gebruikten natriumazide, een chemische stof die complex IV in mitochondriën blokkeert. Bij een dosis die de cellen niet meteen doodde, zette natriumazide bijna alle oxidatieve fosforylering uit terwijl glycolyse grotendeels intact bleef. In ontstoken cellen die met TBZ waren behandeld, maakte toevoeging van natriumazide de beschermende barrièrewerking ongedaan: de elektrische weerstand daalde opnieuw en de fluorescerende tracer lekte gemakkelijker door. Hoewel de cellen enigszins naar glycolyse verschoven als compensatie, daalde de totale ATP en herstelde de barrière niet, waarmee intacte mitochondriale respiratie rechtstreeks aan barrière-integriteit werd gekoppeld.
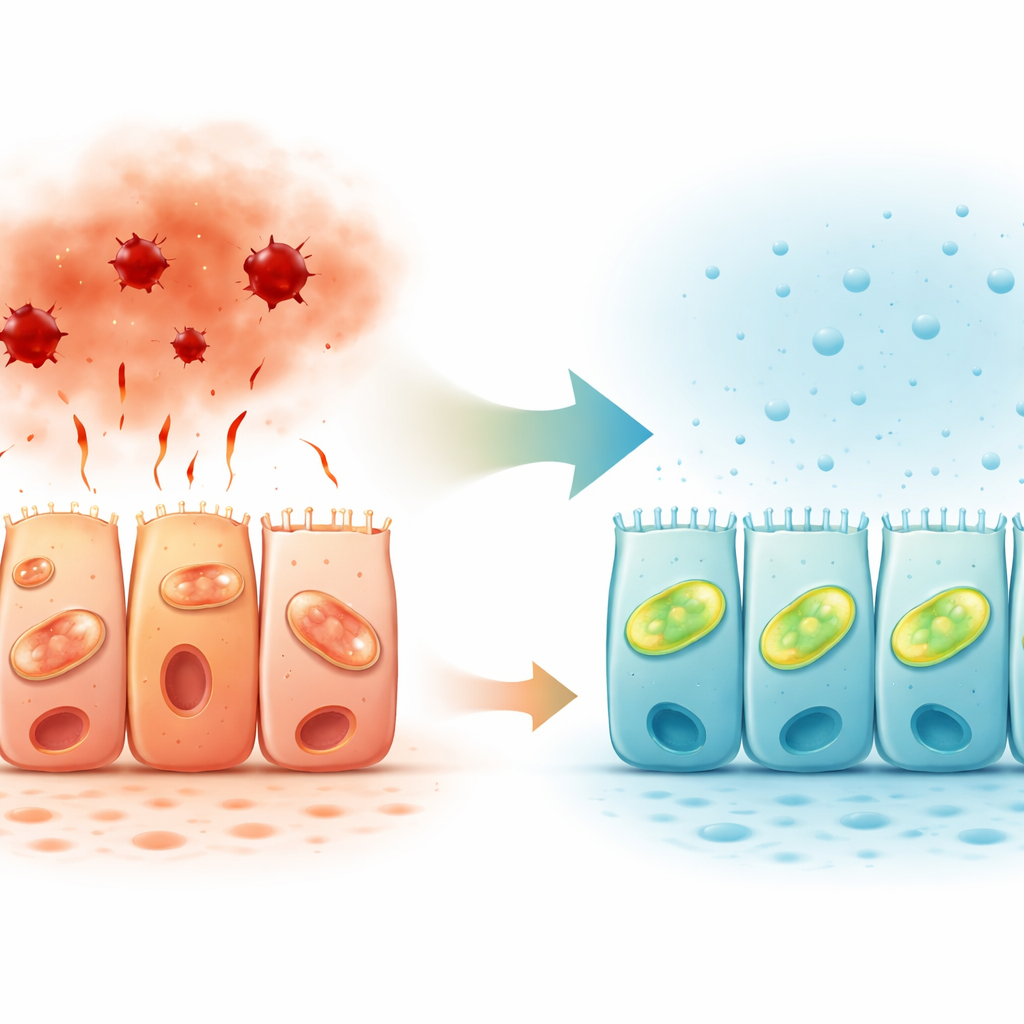
Endogene gassignalen in de darmslijmvlies
Bij onderzoek van menselijk colonweefsel brachten de onderzoekers ook in kaart waar enzymen die waterstofsulfide produceren zich bevinden. Twee van deze enzymen kwamen het sterkst tot expressie aan de bovenkant van de epitheelcellen, de zijde die naar de darmholte gericht is, met name in het opgaande colon. Dit gepolariseerde patroon ondersteunt het idee dat waterstofsulfide lokaal werkt aan het oppervlak waar de barrière in contact staat met de darminhoud en fijn regelt hoe cellen op stress reageren. Gecombineerd met eerder werk dat verminderde waterstofsulfide‑routes bij inflammatoire darmziekte liet zien, suggereren de bevindingen dat verminderde gassignalisatie kan bijdragen aan barrièrefalen bij patiënten.
Wat dit betekent voor toekomstige behandelingen
Samengevat toont de studie aan dat een waterstofsulfide‑afgevende verbinding een ontstoken, lekkende intestinale barrière kan herstellen door de mitochondriale energieproductie op te voeren, specifiek via oxidatieve fosforylering, hoewel zij de ontstekingsgeïnduceerde celdood zelf niet voorkomt. Voor een leek is de boodschap dat het strak houden van de darmwand evenzeer kan afhangen van het voeden van de energiecentrales van cellen als van het remmen van ontsteking. Geneesmiddelen gebaseerd op TBZ, of gerichte waterstofsulfide‑donoren, zouden op termijn kunnen helpen de darmbarrière te stabiliseren bij aandoeningen zoals inflammatoire darmziekte of leverziekte. Omdat TBZ echter ook de doorlaatbaarheid kan verhogen wanneer er geen ontsteking is, benadrukt het werk bovendien de noodzaak om dergelijke therapieën zorgvuldig af te stemmen op de juiste context en dosering.
Bronvermelding: de Oliveira, J.P., van Sligtenhorst, M., Akkaya, C. et al. Hydrogen sulfide rescues IFNγ/TNFα-induced intestinal epithelial barrier dysfunction by enhancing oxidative phosphorylation. Sci Rep 16, 10208 (2026). https://doi.org/10.1038/s41598-026-40348-2
Trefwoorden: intestinale barrière, waterstofsulfide, mitochondriën, ontsteking, epitheelcellen