Clear Sky Science · ar
يُنقِذ كبريتيد الهيدروجين خلل حاجز الظهارة المعوية الناجم عن IFNγ/TNFα عبر تعزيز الفسفرة التأكسدية
لماذا يهم جدار الأمعاء الرقيق
بطانة أمعائنا تتألف من طبقة خلوية واحدة فقط، ومع ذلك تفصل العالم الخارجي داخل القناة الهضمية عن بقية الجسم. عندما يصبح هذا الحاجز «مسربًا»، يمكن أن تتسلل البكتيريا والسموم، مما يغذي الالتهاب ليس فقط في الجهاز الهضمي بل أيضًا في الكبد والدماغ وأعضاء أخرى. تستكشف هذه الدراسة كيف يمكن لجزيء صغير يحتوي على الكبريت، يُطلق ببطء غاز كبريتيد الهيدروجين، أن يساعد في حماية هذا الجدار الهش أثناء الالتهاب عن طريق تعزيز إنتاج الطاقة في الخلايا.
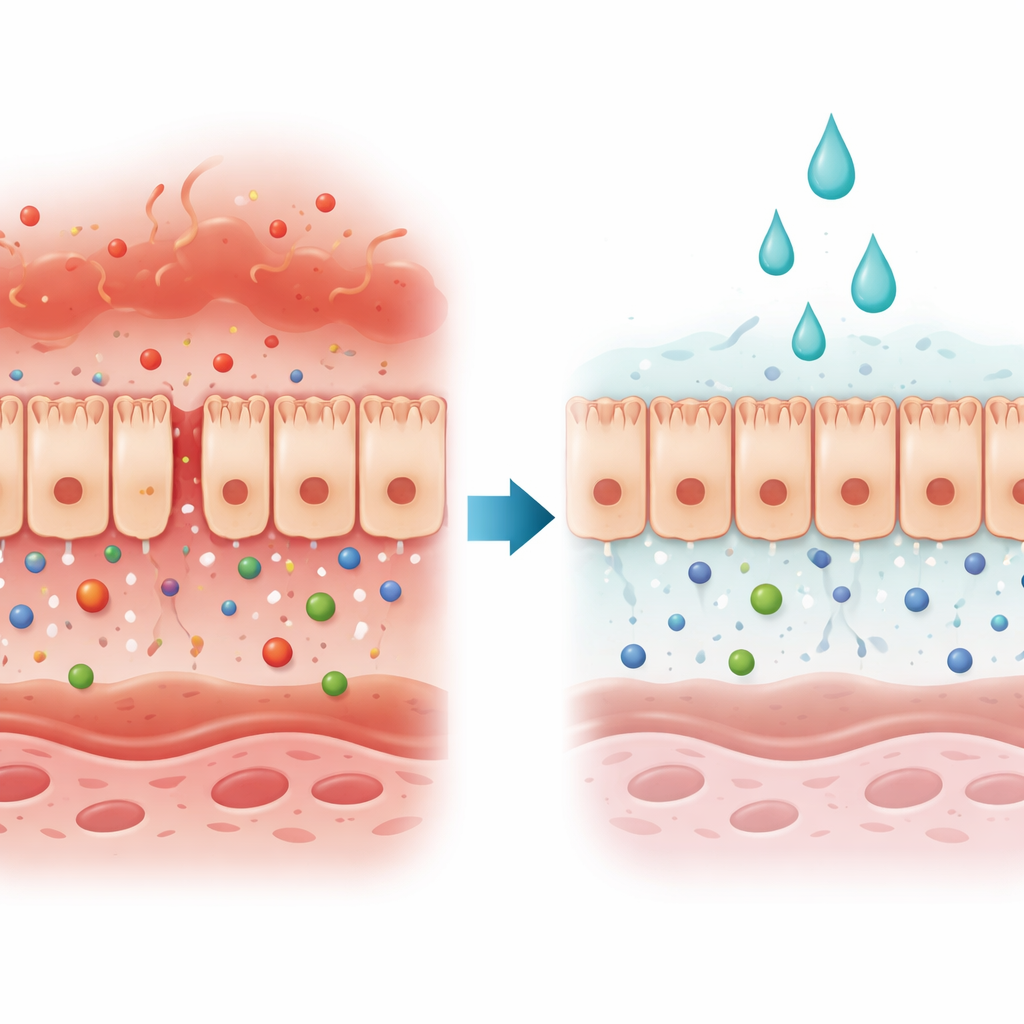
حارس الجسم تحت الهجوم
تشكل الخلايا الطلائية المعوية سطحًا مستمرًا يعمل كبوابة انتقائية: يمنع الغزاة الضارين بينما يسمح بمرور المغذيات والماء. في العديد من أمراض الأمعاء والكبد، تفشل هذه البوابة لأن الفراغات بين الخلايا تتسع أو تموت الخلايا. ركز الباحثون على نوع من الإصابة يقودها إشارتان مناعيتان، إنترفيرون‑غاما وعامل نخر الورم‑ألفا، واللتان تتوافران بكثرة في مرض الأمعاء الالتهابي. معًا، تضعف هاتان الإشارتان الحاجز وتجعل من الأسهل للمواد في الأمعاء الوصول إلى مجرى الدم.
مانح كبريت له وجهان
درس الباحثون مركبًا يُدعى 4‑هيدروكسي ثيوبنزاميد (TBZ)، وهو مركب قادر على إطلاق كبريتيد الهيدروجين، الغاز الذي تنتجه خلايانا أيضًا بمستويات منخفضة ووقائية. في طبقات الخلايا المعوية المزروعة مخبريًا وفي العضويات المعوية البشرية، أظهر TBZ تأثيرًا غريبًا يعتمد على السياق. بمفرده، زاد قليلًا من التسرب بين الخلايا. ولكن عندما كان الحاجز قد تضرر بالفعل بإشارات التهابية، استعاد TBZ وظيفته إلى حد كبير. خفّض علامات كهربائية لانهيار الحاجز وأعاد مرور جزيء متتبع فلوري نحو الطبيعي، على الرغم من أنه لم يمنع موت الخلايا الذي تحفزه السيتوكينات.
تشغيل محطات طاقة الخلايا
لكشف كيف يمارس TBZ هذا التأثير الوقائي، فحص الفريق نشاط الجينات الشامل في الخلايا المعالجة. وجدوا أن TBZ فعّل بقوة جينات مرتبطة بالفسفرة التأكسدية — وهي العملية التي تصنع بها الميتوكوندريا، «محطات طاقة» الخلية، معظم طاقة ATP. تم تنظيم مكونات رئيسية من المركب الميتوكوندري الرابع وبروتينات النقل المرتبطة صعودًا، ما يشير إلى أن TBZ كان يضبط آلية الطاقة بدلًا من مسارات الالتهاب التقليدية. أكدت تجارب متابعة ذلك: تحت ظروف التهابية، عزز TBZ إنتاج ATP الميتوكوندري دون تغيير اللاهواء (التحلل السكري)، مما يدل على ارتفاع مستهدف في إنتاج الطاقة عالي الكفاءة.
عندما تتعطل الميتوكوندريا، يفشل الحاجز
ثم اختبر المؤلفون ما إذا كان هذا التعزيز للطاقة ضروريًا لإصلاح الحاجز. استخدموا الأزوت الصوديومي، مركب كيميائي يعيق المركب الرابع في الميتوكوندريا. بجرعة لم تقتل الخلايا فورًا، عطّل الأزوت الصوديومي تقريبًا الفسفرة التأكسدية في حين ترك التحلل السكري سليمًا إلى حد بعيد. في الخلايا الملتهبة المعالجة بـTBZ، ألغى إضافة الأزوت الصوديومي التأثير الوقائي على الحاجز: انخفضت المقاومة الكهربائية مرة أخرى وتسرب المتتبع الفلوري ازداد. على الرغم من أن الخلايا تحولت إلى حد ما نحو التحلل السكري كتعويض، فإن إجمالي ATP انخفض ولم يتعافَ الحاجز، مما يربط التنفس الميتوكوندري السليم مباشرةً بسلامة الحاجز.
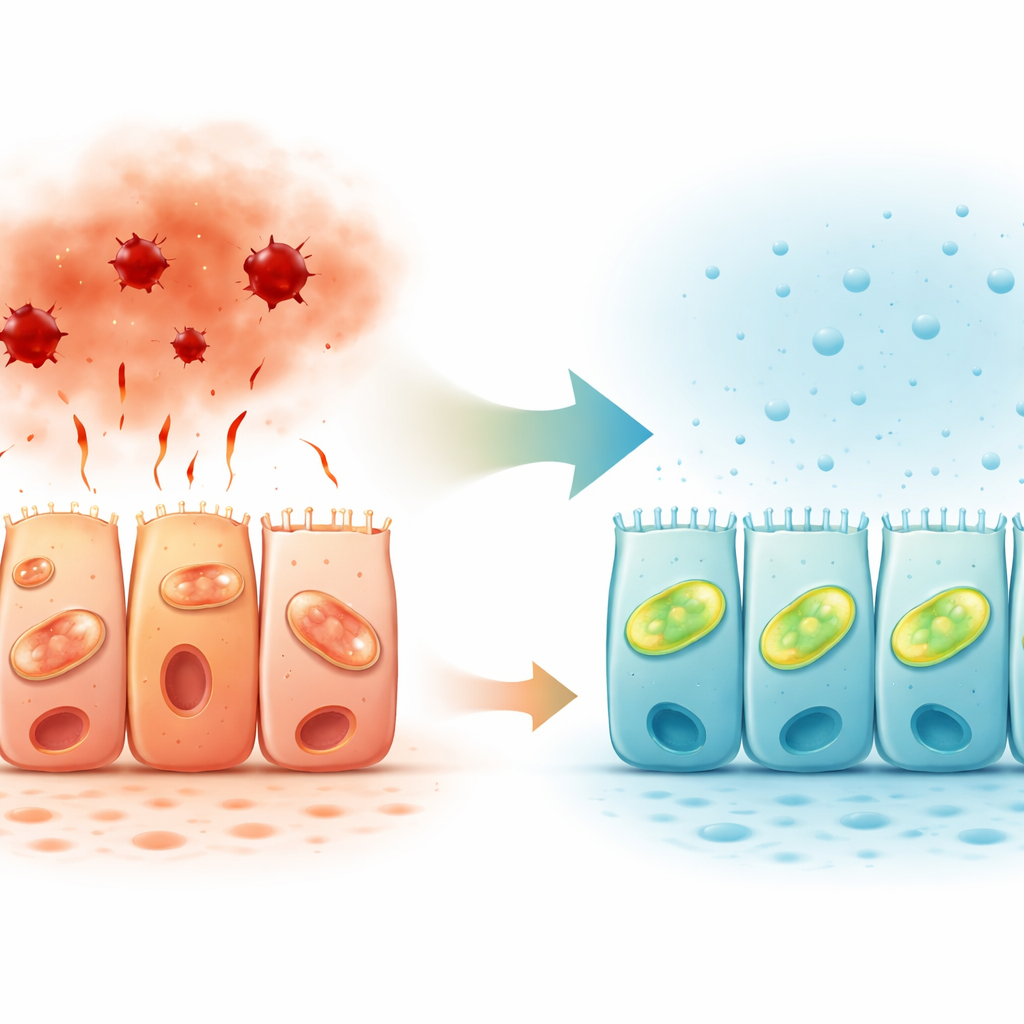
إشارات الغاز الطبيعي في بطانة الأمعاء
بالنظر إلى نسيج القولون البشري، رسم الباحثون أيضًا خريطة مواقع إنزيمات إنتاج كبريتيد الهيدروجين. كان تعبير اثنين من هذه الإنزيمات أقوى في الجانب العلوي المواجه للأمعاء من الخلايا الطلائية، خصوصًا في القولون الصاعد. يدعم هذا النمط المستقطب فكرة أن كبريتيد الهيدروجين يعمل محليًا عند السطح حيث يلتقي الحاجز بمحتويات الأمعاء، مضبطًا استجابة الخلايا للضغط. مجتمعةً مع أعمال سابقة أظهرت مسارات كبريتيد هيدروجين منخفضة في مرض الأمعاء الالتهابي، تشير النتائج إلى أن ضعف إشارات الغاز قد يساهم في فشل الحاجز لدى المرضى.
ماذا يعني هذا للعلاجات المستقبلية
باجمال، تُظهر الدراسة أن مركبًا مطلقًا لكبريتيد الهيدروجين يمكنه إنقاذ حاجز معوي ملتهب ومسرب عبر رفع إنتاج الطاقة الميتوكوندرية، وبالأخص عبر الفسفرة التأكسدية، بالرغم من أنه لا يوقف موت الخلايا الالتهابي بحد ذاته. للقراء غير المتخصصين، الرسالة هي أن الحفاظ على إحكام جدار الأمعاء قد يعتمد بقدر ما على تغذية محطات طاقة الخلايا كما يعتمد على كبح الالتهاب. قد تساعد أدوية مستوحاة من TBZ، أو مانحات كبريتيد هيدروجين مستهدفة، يومًا ما في تثبيت الحاجز المعوي في حالات مثل مرض الأمعاء الالتهابي أو أمراض الكبد. ومع ذلك، لأن TBZ يمكن أن يزيد أيضًا من التسرب عندما لا يوجد التهاب، تبرز الحاجة إلى مواءمة هذه العلاجات بعناية مع السياق والجرعة المناسبين.
الاستشهاد: de Oliveira, J.P., van Sligtenhorst, M., Akkaya, C. et al. Hydrogen sulfide rescues IFNγ/TNFα-induced intestinal epithelial barrier dysfunction by enhancing oxidative phosphorylation. Sci Rep 16, 10208 (2026). https://doi.org/10.1038/s41598-026-40348-2
الكلمات المفتاحية: الحاجز المعوي, كبريتيد الهيدروجين, الميتوكوندريا, الالتهاب, الخلايا الطلائية