Clear Sky Science · ru
Сероводород спасает барьер кишечного эпителия, индуцированный IFNγ/TNFα, усиливая окислительное фосфорилирование
Почему важна тонкая стенка кишечника
Слой клеток, выстилающий наши кишечники, состоит всего из одного ряда, но он отделяет среду в просвете кишечника от остального организма. Когда этот барьер становится «проницаемым», бактерии и токсины могут просачиваться, подпитывая воспаление не только в пищеварительном тракте, но и в печени, мозге и других органах. В этом исследовании изучается, как небольшая содержащая серу молекула, медленно выделяющая газ сероводород, может защищать эту хрупкую стенку при воспалении, повышая производство энергии в клетках.
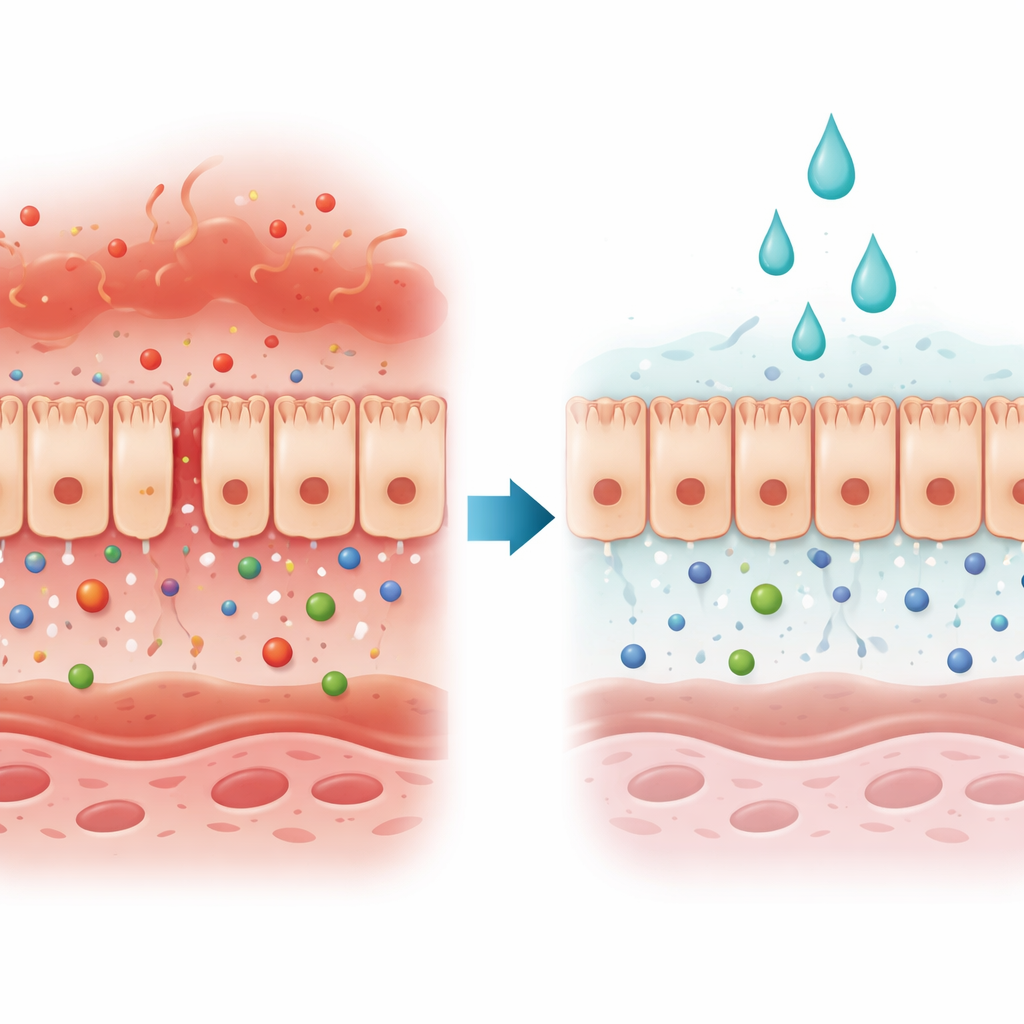
Режим работы «сторожа» организма под ударом
Эпителиальные клетки кишечника образуют непрерывный слой, функционирующий как выборочный «ворота»: он препятствует вредным чужеродным агентам и одновременно пропускает питательные вещества и воду. При многих заболеваниях кишечника и печени эти ворота нарушаются — межклеточные контакты размыкаются или клетки погибают. Авторы сосредоточились на типе повреждения, вызванном двумя иммунными сигналами — интерфероном‑гамма и фактором некроза опухоли‑альфа, которые повышены при воспалительных заболеваниях кишечника. Вместе эти сигналы ослабляют барьер и упрощают перемещение содержимого кишечника в кровоток.
Донор серы с двойным характером
Исследователи изучали 4‑гидрокситиобензиамид (TBZ) — соединение, способное выделять сероводород, газ, который наши клетки также вырабатывают в малых, защитных количествах. В культурах эпителиальных слоев кишечника и в человеческих кишечных органоидах TBZ проявлял любопытный эффект, зависящий от контекста. Сам по себе он слегка увеличивал проницаемость между клетками. Но когда барьер уже был повреждён воспалительными сигналами, TBZ в значительной мере восстанавливал его функцию. Он снижал электрические признаки нарушения барьера и возвращал прохождение флуоресцентного трейсера ближе к норме, хотя не предотвращал гибель клеток, вызванную цитокинами.
«Заводики энергии» клеток получают источник питания
Чтобы выяснить, как TBZ обеспечивает эту защиту, команда проанализировала глобальную активность генов в обработанных клетках. Они обнаружили, что TBZ сильно активирует гены, связанные с окислительным фосфорилированием — процессом, с помощью которого митохондрии, «энергетические станции» клетки, производят большую часть ATP. Были повышены ключевые компоненты комплекса IV митохондрий и связанные транспортные белки, что указывает на то, что TBZ настраивает энергетический аппарат, а не классические воспалительные пути. Последующие эксперименты это подтвердили: в условиях воспаления TBZ усиливал митохондриальное производство ATP, не изменяя гликолиза, что свидетельствует о целенаправленном повышении энергоэффективности.
Когда митохондрии дают сбой, барьер рушится
Затем авторы проверили, требуется ли это энергетическое повышение для восстановления барьера. Они использовали азид натрия — химическое вещество, блокирующее комплекс IV митохондрий. При дозе, не приводящей к мгновенной гибели клеток, азид натрия почти полностью выключал окислительное фосфорилирование, оставляя гликолиз в большей степени нетронутым. В инфицированных воспалением клетках, обработанных TBZ, добавление азида натрия стирало защитный эффект: электрическое сопротивление снова падало, а флуоресцентный трекер проходил легче. Несмотря на частичный переход клеток на гликолиз как компенсацию, общий уровень ATP снижался, и барьер не восстанавливался, что напрямую связывает целостное митохондриальное дыхание с сохранением барьера.
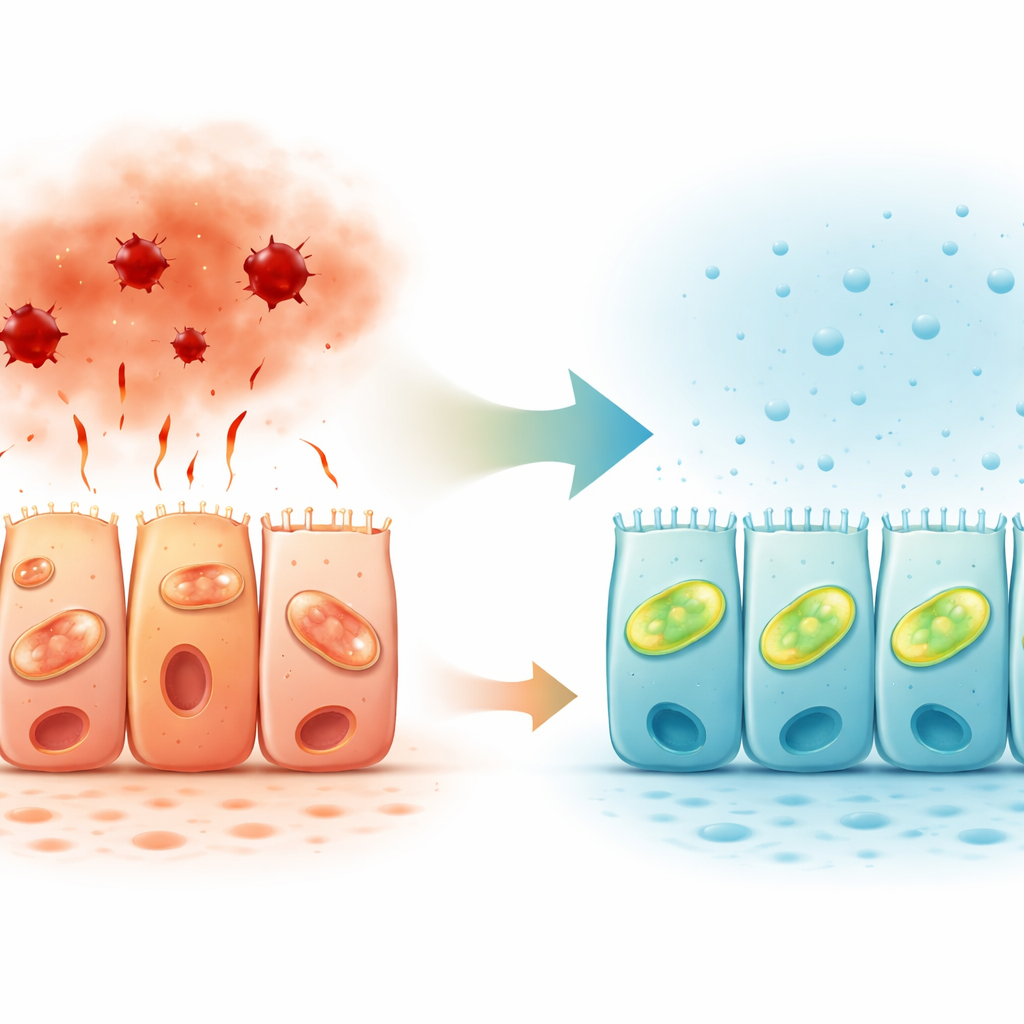
Сигналы «природного газа» в слизистой кишечника
Изучая ткани толстой кишки человека, исследователи также локализовали ферменты, производящие сероводород. Два таких фермента наиболее сильно экспрессировались на верхней, обращённой к просвету стороне эпителиальных клеток, особенно в восходящей ободочной кишке. Эта полярная картина поддерживает идею о том, что сероводород действует локально на поверхности, где барьер сталкивается с содержимым кишечника, тонко регулируя реакцию клеток на стресс. В сочетании с прежними работами, показывающими снижение путей сероводорода при воспалительных заболеваниях кишечника, эти результаты предполагают, что ослабление газовой сигнализации может способствовать нарушению барьера у пациентов.
Что это значит для будущих терапий
В целом исследование показывает, что соединение, выделяющее сероводород, может восстановить воспалённый, проницаемый кишечный барьер, усилив митохондриальное производство энергии, в частности через окислительное фосфорилирование, хотя оно и не останавливает саму воспалительную гибель клеток. Для неспециалиста вывод таков: поддержание плотности кишечной стенки может зависеть не только от подавления воспаления, но и от подпитки «энергетических станций» клеток. Препараты, созданные по образцу TBZ, или целевые доноры сероводорода могли бы в будущем помочь стабилизировать кишечный барьер при таких состояниях, как воспалительные заболевания кишечника или болезни печени. Однако поскольку TBZ при отсутствии воспаления также может повышать проницаемость, работа подчёркивает необходимость тщательно подбирать контекст и дозу подобных терапий.
Цитирование: de Oliveira, J.P., van Sligtenhorst, M., Akkaya, C. et al. Hydrogen sulfide rescues IFNγ/TNFα-induced intestinal epithelial barrier dysfunction by enhancing oxidative phosphorylation. Sci Rep 16, 10208 (2026). https://doi.org/10.1038/s41598-026-40348-2
Ключевые слова: кишечный барьер, сероводород, митохондрии, воспаление, эпителиальные клетки