Clear Sky Science · zh
来自野生型猴子和Tau-P301L转基因猴子多种组织的单核RNA测序数据集
这项猴子研究为何重要
阿尔茨海默病以夺走记忆著称,但它也会改变运动、平衡以及多类脑细胞的健康状况。要设计更有效的治疗方法,科学家需要尽可能模拟人类病情的动物模型。本研究提供了来自一种经基因工程改造并出现类阿尔茨海默改变的猴子的一份详细细胞图谱,为理解不同脑与脊髓细胞在疾病进展中如何反应,提供了一个强有力的新视角。
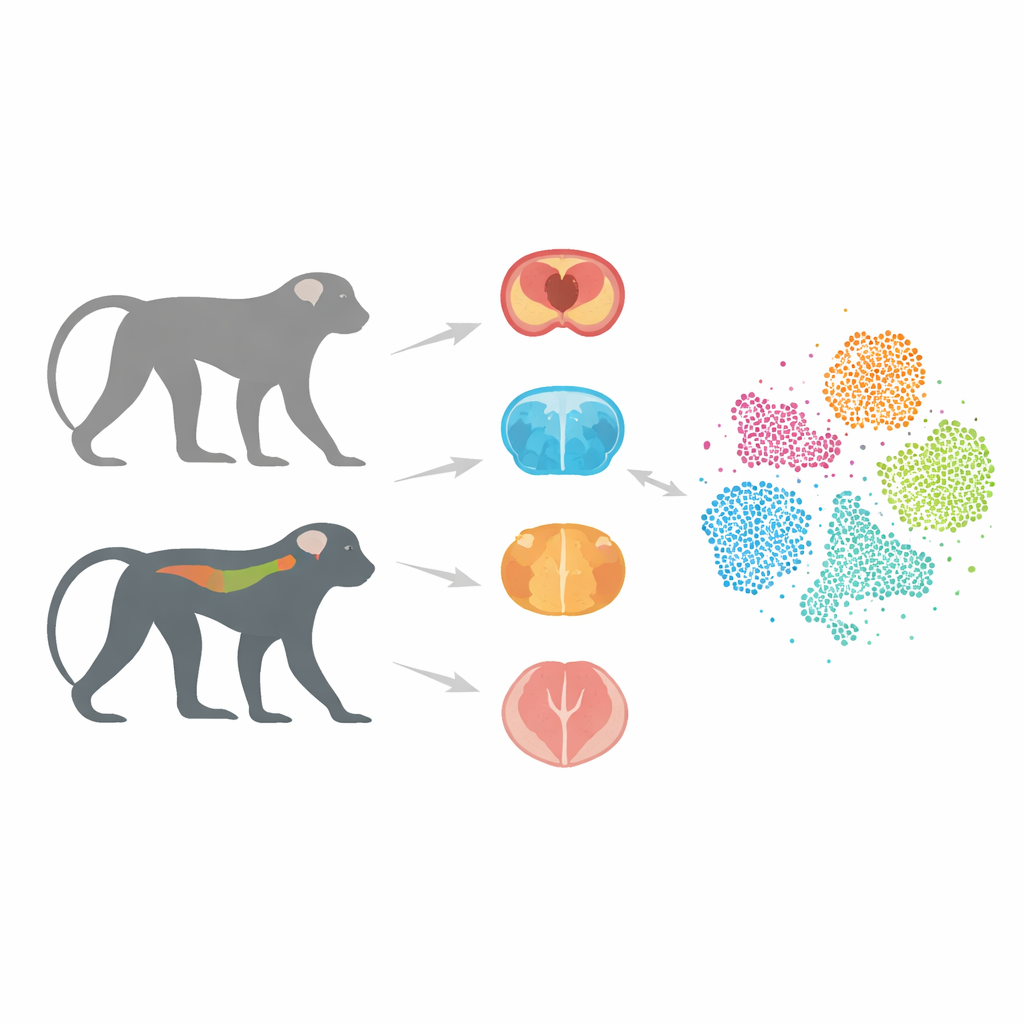
比人类更贴近的动物替代模型
大多数阿尔茨海默研究依赖携带与该病相关人类基因的小鼠模型。这些模型教会了研究者许多知识,但它们常常无法预测潜在药物在人类中的疗效。一个主要原因是小鼠的大脑和免疫系统与人类存在显著差异。相比之下,猴子在大脑结构和基因组成上与人类更为相似。在早期工作中,研究者构建了携带人类型tau蛋白(称为Tau-P301L)的短尾猕猴,这种tau在多种痴呆中异常聚集。这些猴子逐渐出现神经细胞损伤和运动障碍,类似人类tau驱动疾病的关键特征。
读取成千上万细胞内部的信息
在本项目中,团队聚焦于三个关键区域:参与记忆的海马体、与运动和动机相关的纹状体,以及有助于控制姿势和步态且日益被认为与阿尔茨海默有关的脊髓。研究人员从转基因和健康猴子的这些组织中分离出单个细胞核,并采用单核RNA测序技术。该技术能够读取每个细胞中活跃的基因,从而以极高精度区分细胞类型和状态。经过仔细的质量控制以去除受损细胞和技术误差后,他们汇编出包含36,623个高质量细胞的图谱。
猴子神经系统的细胞图谱
通过将具有相似基因活性模式的细胞分组,团队识别出13种主要细胞类型,包括神经元、若干类支持细胞(如星形胶质细胞和少突胶质细胞)、免疫样小胶质细胞,以及稀有群体如T细胞和室管膜带细胞。他们使用已知标志基因验证了每一组,并证明这些簇是清晰且一致的。比较病变与健康猴子时,他们发现某些小胶质细胞——一种脑内免疫细胞——在Tau-P301L动物中增多。这些小胶质细胞表达的基因此前与损伤感知和在人类阿尔茨海默大脑蛋白沉积周围看到的炎症反应相关,这暗示该猴模型捕捉到了许多小鼠研究中缺失或较弱的重要免疫反应。
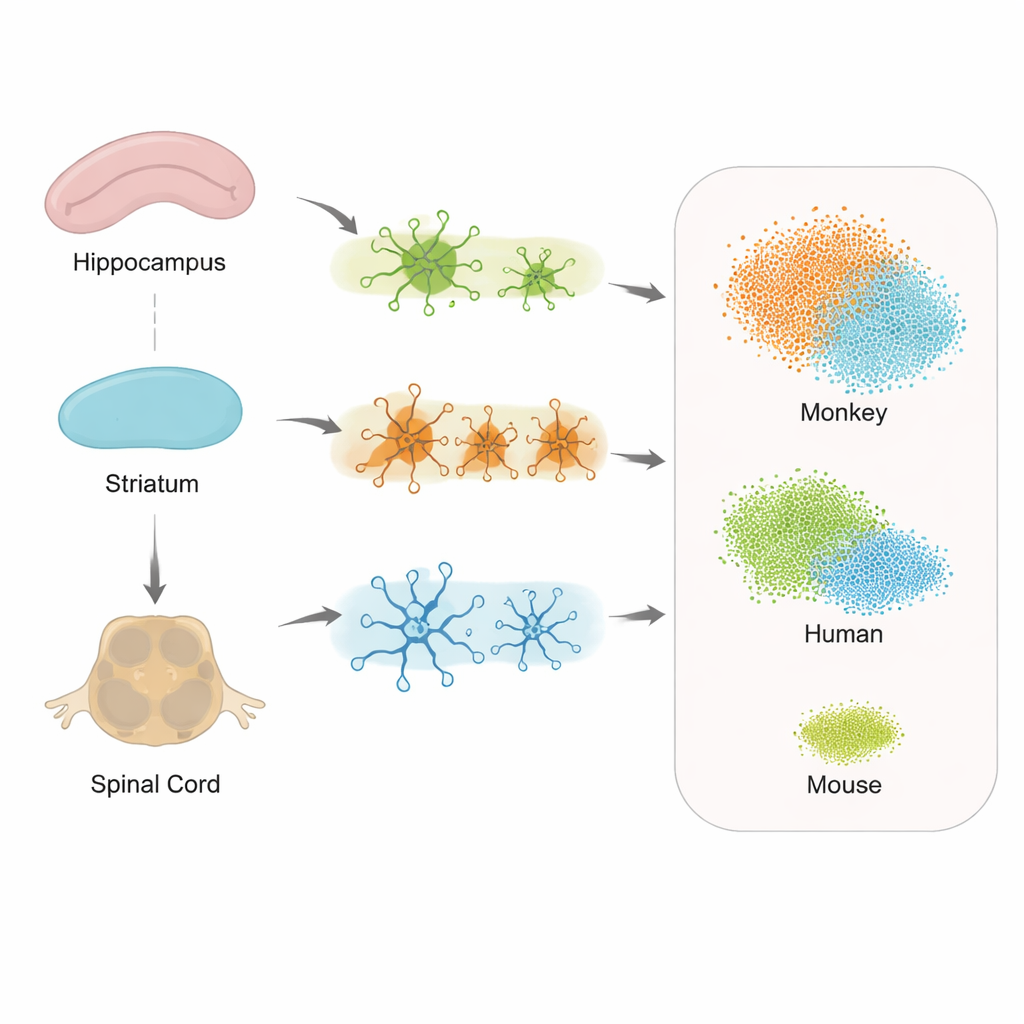
不同区域,不同的细胞反应
当研究者检查海马、纹状体和脊髓中支持细胞的基因变化时,他们既观察到共同的反应,也看到区域特异性的反应。星形胶质细胞、小胶质细胞和少突胶质细胞都显示出活性改变,但具体的基因组合因部位而异。这表明神经系统的每个部分都会发起其特有的应激反应,这或许能解释为何某些症状(如行走困难)可能在明显记忆丧失之前出现。重要的是,脊髓显示出强烈的参与,支持了阿尔茨海默不仅是脑部疾病,而是更广泛中枢神经系统疾病的观点。
与人类高度相似的猴子数据
为测试猴子模型与人类疾病的相似度,团队将其海马数据与已有的人类早发性阿尔茨海默数据集和另一个tau突变小鼠模型的数据进行了比较。他们重点比较了小胶质细胞以及在人体患者中已描述的一种“疾病相关”细胞状态。猴子小胶质细胞的基因活性模式与人类大脑的重叠远多于小鼠模式,包括许多在小鼠中几乎没有改变的关键免疫和应激相关基因。这表明Tau-P301L猴子在单细胞水平上比现有啮齿动物模型更好地再现了人类样的疾病特征。
这对未来阿尔茨海默研究的意义
对非专业读者来说,主要信息是:这项研究提供了一份丰富且公开可用的逐细胞图谱,展示了人源化tau蛋白如何在比小鼠更接近我们的物种中扰乱脑与脊髓细胞。该图谱突出了受影响最严重的细胞类型和区域,并显示猴子模型比常规小鼠模型更忠实地再现了人类免疫细胞的变化。因此,这些数据为研究阿尔茨海默起始与传播的假说提供了有价值的试验场,并可能帮助研究者设计在进入人体临床时更有可能奏效的治疗策略。
引用: Han, B., Chen, Y., Ouyang, W. et al. Single-nucleus RNA sequencing dataset of diverse tissues from wild-type monkey and Tau-P301L transgenic monkey. Sci Data 13, 497 (2026). https://doi.org/10.1038/s41597-026-06882-4
关键词: 阿尔茨海默病, tau蛋白, 非人灵长类模型, 单细胞RNA测序, 小胶质细胞