Clear Sky Science · es
Conjunto de datos de ARN de núcleo único de tejidos diversos de mono silvestre y mono transgénico Tau-P301L
Por qué importa este estudio en monos
La enfermedad de Alzheimer es más conocida por robar la memoria, pero también altera el movimiento, el equilibrio y la salud de muchos tipos de células cerebrales. Para diseñar tratamientos mejores, los científicos necesitan modelos animales que imiten la condición humana lo más fielmente posible. Este estudio presenta un mapa celular detallado de un mono especialmente diseñado que desarrolla cambios similares a los del Alzheimer, ofreciendo una nueva y potente ventana para entender cómo responden distintas células del cerebro y la médula espinal a medida que la enfermedad progresa.
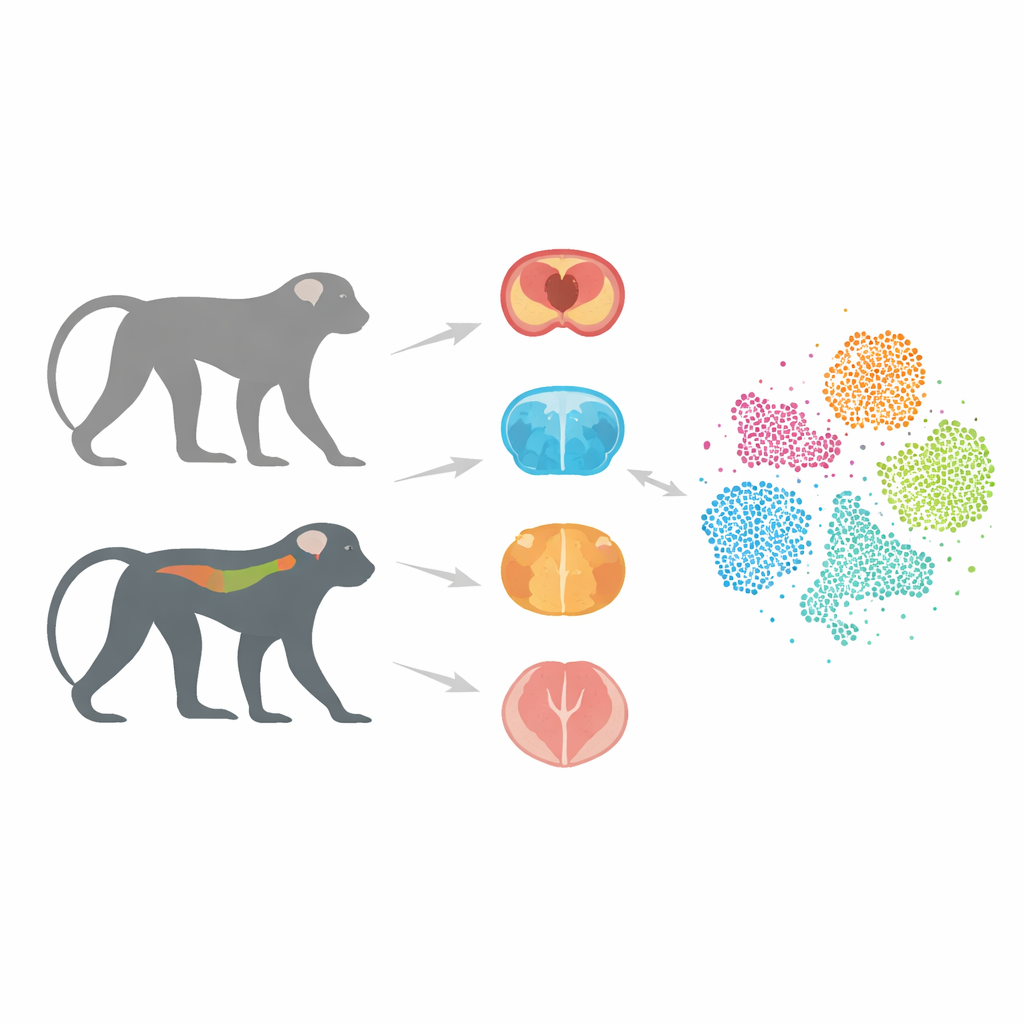
Un sustituto animal más cercano a las personas
La mayoría de la investigación sobre Alzheimer se ha basado en ratones que portan genes humanos vinculados a la enfermedad. Estos modelos han enseñado mucho, pero a menudo no logran predecir si un fármaco potencial funcionará en personas. Una gran razón es que los cerebros y los sistemas inmunitarios de los ratones difieren notablemente de los nuestros. Los monos, en contraste, comparten una estructura cerebral y un repertorio genético mucho más parecido al humano. En trabajos previos, los autores generaron monos cínomolgus que portan una versión humana de la proteína tau, llamada Tau-P301L, que forma agregados anómalos en varias demencias. Estos monos desarrollan de forma gradual daño neuronal y problemas de movimiento, semejando rasgos clave de la enfermedad humana impulsada por tau.
Leer los mensajes dentro de miles de células
En este proyecto, el equipo se centró en tres regiones clave: el hipocampo, importante para la memoria; el estriado, implicado en el movimiento y la motivación; y la médula espinal, que contribuye al control de la postura y la marcha y que cada vez se reconoce más como parte del cuadro del Alzheimer. A partir de monos transgénicos y sanos, los investigadores aislaron núcleos individuales de las células de estos tejidos y usaron secuenciación de ARN de núcleo único. Esta técnica determina qué genes están activos en cada célula, permitiendo a los científicos distinguir tipos y estados celulares con gran precisión. Tras controles de calidad cuidadosos para eliminar células dañadas y errores técnicos, compilaron un atlas de 36.623 células de alta calidad.
Un mapa celular del sistema nervioso del mono
Al agrupar células con patrones de actividad génica similares, el equipo identificó 13 tipos celulares principales, incluidos neuronas, varios tipos de células de soporte como astrocitos y oligodendrocitos, microglía con función inmunitaria y poblaciones raras como células T y células de la zona ventricular. Verificaron cada grupo usando genes marcadores conocidos y mostraron que los clústeres eran limpios y consistentes. Al comparar monos enfermos y sanos, hallaron que ciertos microglía —un tipo de célula inmune cerebral— se expandían en los animales Tau-P301L. Estas microglías expresaban genes vinculados previamente a la detección de daño y respuestas inflamatorias observadas alrededor de depósitos proteicos en cerebros humanos con Alzheimer, lo que sugiere que el modelo de mono captura una reacción inmune importante que falta o está atenuada en muchos estudios con ratones.
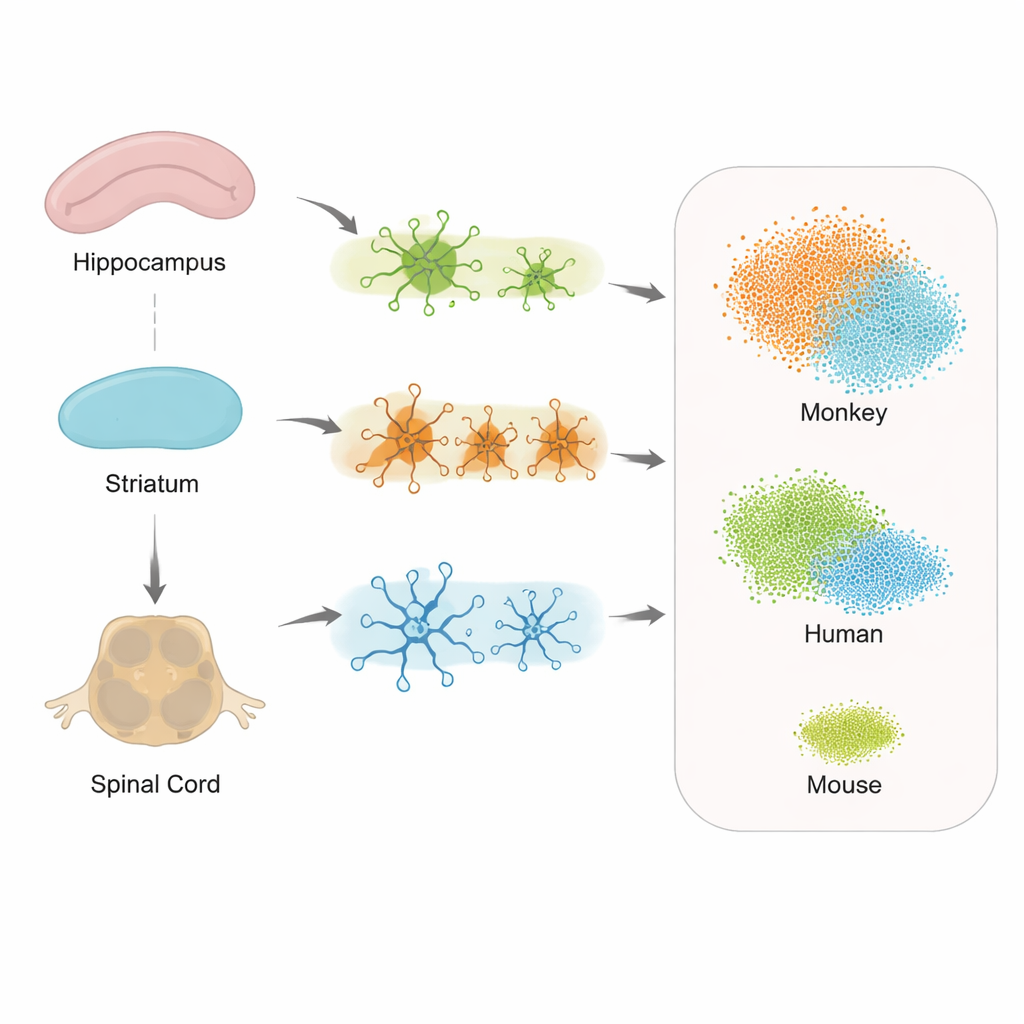
Diferentes regiones, distintas respuestas celulares
Cuando los investigadores examinaron cómo cambiaban los genes en las células de soporte a lo largo del hipocampo, el estriado y la médula espinal, observaron respuestas tanto compartidas como específicas de cada región ante la patología tau. Astrocitos, microglía y oligodendrocitos mostraron actividad alterada, pero los conjuntos exactos de genes variaron según la localización. Esto sugiere que cada parte del sistema nervioso monta su propia versión de una respuesta al estrés, lo que podría ayudar a explicar por qué algunos síntomas, como las dificultades para caminar, pueden aparecer antes que la pérdida de memoria evidente. De forma importante, la médula espinal mostró una implicación notable, reforzando la idea de que el Alzheimer no es solo una enfermedad del cerebro, sino del sistema nervioso central en sentido más amplio.
Datos de mono que se parecen notablemente a los humanos
Para evaluar cuánto refleja el modelo de mono la enfermedad humana, el equipo comparó sus datos hipocampales con conjuntos de datos existentes de personas con Alzheimer de inicio temprano y con otro modelo de ratón con mutación tau. Se centraron en la microglía y en un estado especial «asociado a la enfermedad» de estas células descrito en pacientes humanos. Los patrones de actividad génica en la microglía del mono se superpusieron mucho más con los observados en cerebros humanos que los patrones de ratón, incluyendo muchos genes clave relacionados con la inmunidad y el estrés que cambiaban apenas en los ratones. Esto indica que el mono Tau-P301L captura firmas de enfermedad similares a las humanas a nivel unicelular mejor que los modelos roedores actuales.
Qué significa esto para la investigación futura del Alzheimer
Para el público general, el mensaje principal es que este estudio ofrece un mapa detallado, accesible públicamente y célula por célula de cómo una proteína tau humanizada perturba las células del cerebro y la médula espinal en una especie mucho más cercana a nosotros que los ratones. El atlas destaca qué tipos celulares y regiones están más afectados y muestra que el modelo de mono reproduce los cambios en las células inmunitarias humanas con mayor fidelidad que los modelos murinos estándar. En consecuencia, estos datos ofrecen un valioso campo de pruebas para ideas sobre cómo comienza y se propaga el Alzheimer, y pueden ayudar a los investigadores a diseñar terapias con mayores probabilidades de funcionar cuando finalmente lleguen a pacientes humanos.
Cita: Han, B., Chen, Y., Ouyang, W. et al. Single-nucleus RNA sequencing dataset of diverse tissues from wild-type monkey and Tau-P301L transgenic monkey. Sci Data 13, 497 (2026). https://doi.org/10.1038/s41597-026-06882-4
Palabras clave: Enfermedad de Alzheimer, proteína tau, modelo de primate no humano, secuenciación de ARN unicelular, microglía