Clear Sky Science · de
Ein Single‑Nucleus‑RNA‑Sequenzierungs‑Datensatz vielfältiger Gewebe von Wildtyp‑Affe und Tau‑P301L‑transgenen Affen
Warum diese Affenstudie wichtig ist
Alzheimer‑Krankheit ist vor allem dafür bekannt, Menschen das Gedächtnis zu rauben, sie verändert aber auch Bewegung, Gleichgewicht und die Gesundheit vieler Arten von Gehirnzellen. Um bessere Therapien zu entwickeln, brauchen Wissenschaftler Tiermodelle, die den Menschen so genau wie möglich nachbilden. Diese Studie stellt eine detaillierte zelluläre Karte eines speziell konstruierten Affen vor, der Alzheimer‑ähnliche Veränderungen entwickelt, und bietet damit ein kraftvolles neues Fenster darauf, wie verschiedene Gehirn‑ und Rückenmarkszellen reagieren, während die Krankheit fortschreitet.
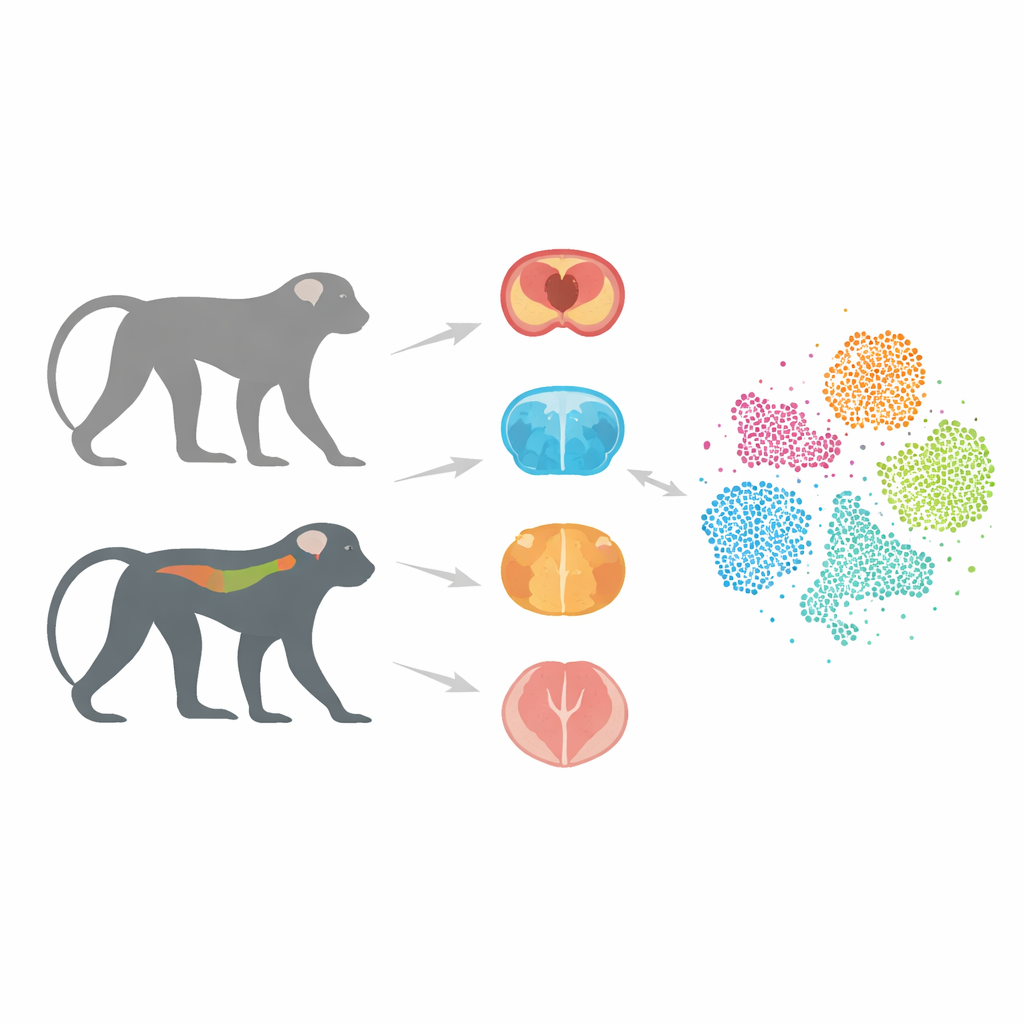
Ein näherer tierischer Ersatz für den Menschen
Die meiste Alzheimer‑Forschung beruhte auf Mäusen, die menschliche Gene tragen, die mit der Krankheit verknüpft sind. Diese Modelle haben den Forschern vieles beigebracht, sagen aber oft nicht zuverlässig voraus, ob ein potenzielles Medikament beim Menschen wirkt. Ein wesentlicher Grund ist, dass Mausgehirne und Immunsysteme deutlich anders sind als unsere. Affen dagegen teilen eine wesentlich ähnliche Gehirnstruktur und Genlage mit Menschen. In früheren Arbeiten erzeugten die Autoren Kynomolgusaffen, die eine menschliche Version des Tau‑Proteins tragen, genannt Tau‑P301L, das sich bei mehreren Demenzen abnorm verklumpt. Diese Affen entwickeln allmählich Nervenzellschäden und Bewegungsprobleme und ähneln damit zentralen Merkmalen der beim Menschen tau‑getriebenen Erkrankung.
Die Botschaften Tausender Zellen lesen
In diesem Projekt konzentrierte sich das Team auf drei Schlüsselregionen: den Hippocampus, der für das Gedächtnis wichtig ist; das Striatum, das an Bewegung und Motivation beteiligt ist; und das Rückenmark, das Haltung und Gang steuert und zunehmend als Teil des Alzheimer‑Bildes anerkannt wird. Aus transgenen und gesunden Affen isolierten die Forschenden einzelne Zellkerne aus diesen Geweben und nutzten Single‑Nucleus‑RNA‑Sequenzierung. Diese Technik erfasst, welche Gene in jeder Zelle aktiv sind, sodass Wissenschaftler Zelltypen und -zustände mit hoher Präzision unterscheiden können. Nach sorgfältigen Qualitätskontrollen zur Entfernung beschädigter Zellen und technischer Fehler stellten sie ein Atlas von 36.623 hochqualitativen Zellen zusammen.
Eine zelluläre Karte des Affennervensystems
Durch das Gruppieren von Zellen mit ähnlichen Genaktivitätsmustern identifizierte das Team 13 große Zelltypen, darunter Neuronen, mehrere Arten von Stützzellen wie Astrozyten und Oligodendrozyten, immunähnliche Mikroglia und seltene Populationen wie T‑Zellen und Ventrikelzonen‑Zellen. Sie verifizierten jede Gruppe mit bekannten Markergenen und zeigten, dass die Cluster klar und konsistent waren. Im Vergleich zwischen erkrankten und gesunden Affen fanden sie, dass bestimmte Mikroglia—eine Art Gehirn‑Immunzelle—bei den Tau‑P301L‑Tieren vermehrt auftraten. Diese Mikroglia exprimierten Gene, die zuvor mit Schadenswahrnehmung und entzündlichen Reaktionen in Verbindung gebracht wurden, wie sie um Proteinablagerungen in menschlichen Alzheimer‑Gehirnen beobachtet werden, was darauf hindeutet, dass das Affenmodell eine wichtige Immunantwort abbildet, die in vielen Mausstudien fehlt oder abgeschwächt ist.
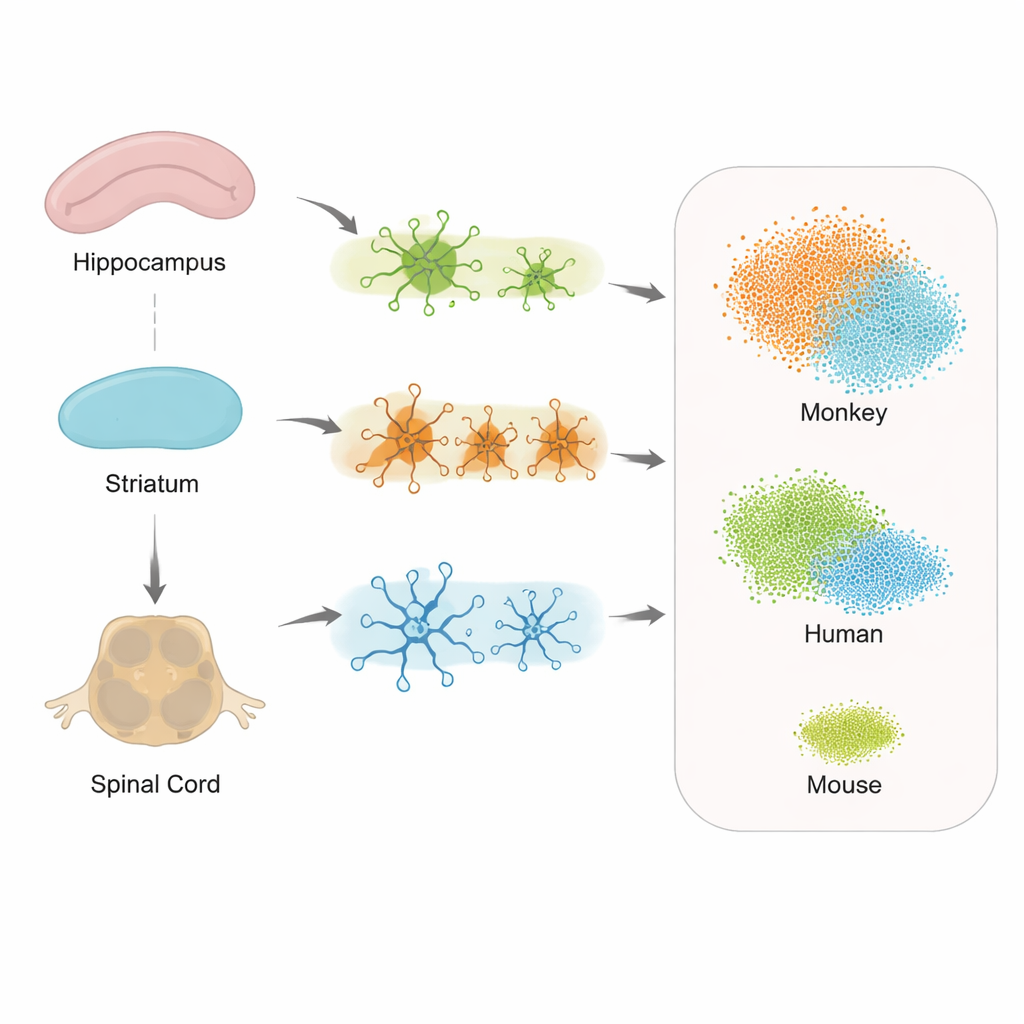
Unterschiedliche Regionen, unterschiedliche Zellreaktionen
Als die Forschenden untersuchten, wie Gene in Stützzellen im Hippocampus, Striatum und Rückenmark verändert wurden, zeigten sich sowohl gemeinsame als auch regionsspezifische Reaktionen auf Tau‑Pathologie. Astrozyten, Mikroglia und Oligodendrozyten wiesen alle veränderte Aktivität auf, doch die genauen Gen‑Sätze variierten je nach Standort. Das deutet darauf hin, dass jeder Teil des Nervensystems seine eigene Version einer Stressantwort mobilisiert, was helfen könnte zu erklären, warum manche Symptome, etwa Probleme beim Gehen, vor offensichtlichem Gedächtnisverlust auftreten. Wichtig ist, dass das Rückenmark stark beteiligt war, was die Idee stützt, dass Alzheimer nicht nur eine Erkrankung des Gehirns, sondern des gesamten zentralen Nervensystems ist.
Affen‑Daten, die verblüffend menschlich wirken
Um zu prüfen, wie gut das Affenmodell die menschliche Erkrankung spiegelt, verglich das Team seine Hippocampus‑Daten mit bestehenden Datensätzen von Menschen mit früh beginnender Alzheimer‑Krankheit und mit einem anderen tau‑mutanten Mausmodell. Sie konzentrierten sich auf Mikroglia und auf einen speziellen "krankheitsassoziierten" Zustand dieser Zellen, der bei Patienten beschrieben wurde. Die Genaktivitätsmuster in Affen‑Mikroglia überlappten weit stärker mit denen in menschlichen Gehirnen als die Muster aus Mäusen, einschließlich vieler wichtiger Immun‑ und Stress‑bezogener Gene, die sich bei Mäusen kaum veränderten. Das zeigt, dass der Tau‑P301L‑Affe krankheitsähnliche Signaturen auf Einzelzellebene besser erfasst als derzeitige Nagetiermodelle.
Was das für die zukünftige Alzheimer‑Forschung bedeutet
Für Nicht‑Spezialisten lautet die Hauptaussage, dass diese Studie eine reichhaltige, öffentlich verfügbare Zell‑für‑Zell‑Karte liefert, wie ein humanisiertes Tau‑Protein Gehirn‑ und Rückenmarkszellen in einer dem Menschen deutlich näheren Spezies stört als Mäuse. Der Atlas hebt hervor, welche Zelltypen und Regionen am stärksten betroffen sind, und zeigt, dass das Affenmodell menschliche Immunzellveränderungen treuer reproduziert als Standard‑Mausmodelle. Dadurch bieten diese Daten ein wertvolles Testfeld für Hypothesen darüber, wie Alzheimer beginnt und sich ausbreitet, und sie könnten Forschern helfen, Therapien zu entwerfen, die eine höhere Wahrscheinlichkeit haben, beim Menschen erfolgreich zu sein.
Zitation: Han, B., Chen, Y., Ouyang, W. et al. Single-nucleus RNA sequencing dataset of diverse tissues from wild-type monkey and Tau-P301L transgenic monkey. Sci Data 13, 497 (2026). https://doi.org/10.1038/s41597-026-06882-4
Schlüsselwörter: Alzheimer‑Krankheit, Tau‑Protein, Modell nicht‑menschlicher Primaten, Einzelzellen‑RNA‑Sequenzierung, Mikroglia