Clear Sky Science · ja
ワイルドタイプのサルとTau-P301L遺伝子導入サルから得られた多様な組織の単一核RNAシーケンスデータセット
このサル研究が重要な理由
アルツハイマー病は記憶喪失で知られていますが、運動やバランス、そしてさまざまな種類の脳細胞の健康にも影響を与えます。より良い治療を設計するには、人間の病態をできるだけ忠実に再現する動物モデルが必要です。本研究は、アルツハイマー様の変化を示すように特別に改変されたサルから得られた詳細な細胞地図を提示しており、病気の進行に伴ってさまざまな脳や脊髄の細胞がどのように反応するかを探る強力な新たな窓を提供します。
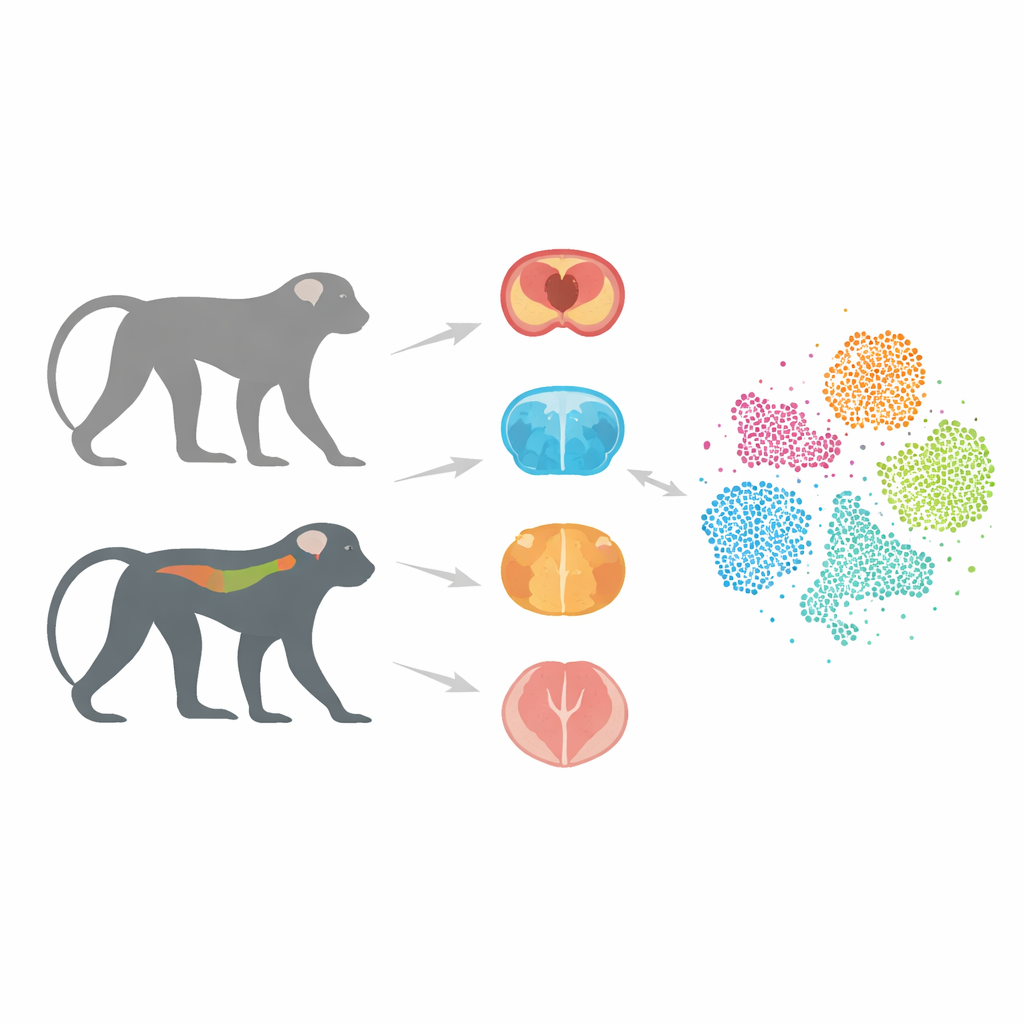
ヒトに近い動物代替モデル
これまでの多くのアルツハイマー研究は、疾患に関連するヒト遺伝子を導入したマウスに依拠してきました。これらのモデルは多くを教えてくれましたが、候補薬がヒトで有効かどうかを予測できないことがしばしばあります。その大きな理由の一つは、マウスの脳や免疫系がヒトと大きく異なることです。これに対してサルは、脳構造や遺伝的背景がヒトとはるかに類似しています。以前の研究で著者らは、タウタンパク質のヒト型変異であるTau-P301Lを持つカニクイザルを作成しました。このタンパク質はいくつかの認知症で異常に凝集します。これらのサルは徐々にニューロンの障害や運動障害を示し、タウが駆動するヒトの病態の重要な特徴を模倣します。
何千もの細胞内部のメッセージを読む
本研究では、チームは海馬(記憶に重要)、線条体(運動と動機づけに関与)、および姿勢や歩行の制御に関与し、アルツハイマーの全体像の一部としてますます注目されている脊髄の3つの主要領域に焦点を当てました。遺伝子改変サルと健常サルの両方から、これらの組織の細胞から個々の核を分離し、単一核RNAシーケンスを用いました。この手法は各細胞でどの遺伝子が活性化されているかを読み取り、細胞型や状態を高い精度で識別可能にします。損傷細胞や技術的誤差を除去する慎重な品質管理ののち、36,623個の高品質な細胞からなるアトラスを作成しました。
サル神経系の細胞地図
遺伝子発現パターンが類似した細胞をグループ化することで、研究チームはニューロン、アストロサイトやオリゴデンドロサイトなどの複数の支持細胞、免疫様のミクログリア、T細胞や脳室帯細胞のような稀な集団を含む13の主要な細胞型を同定しました。各グループは既知のマーカー遺伝子で検証され、クラスタが明瞭で一貫していることが示されました。病変サルと健常サルを比較すると、Tau-P301Lサルで特定のミクログリア集団が増加していることが分かりました。これらのミクログリアは、ヒトのアルツハイマー脳でタンパク質沈着の周囲に見られる損傷検知や炎症応答に関連した遺伝子を発現しており、サルモデルが多くのマウス研究で欠けている、あるいは弱まっている重要な免疫反応をとらえていることを示唆しています。
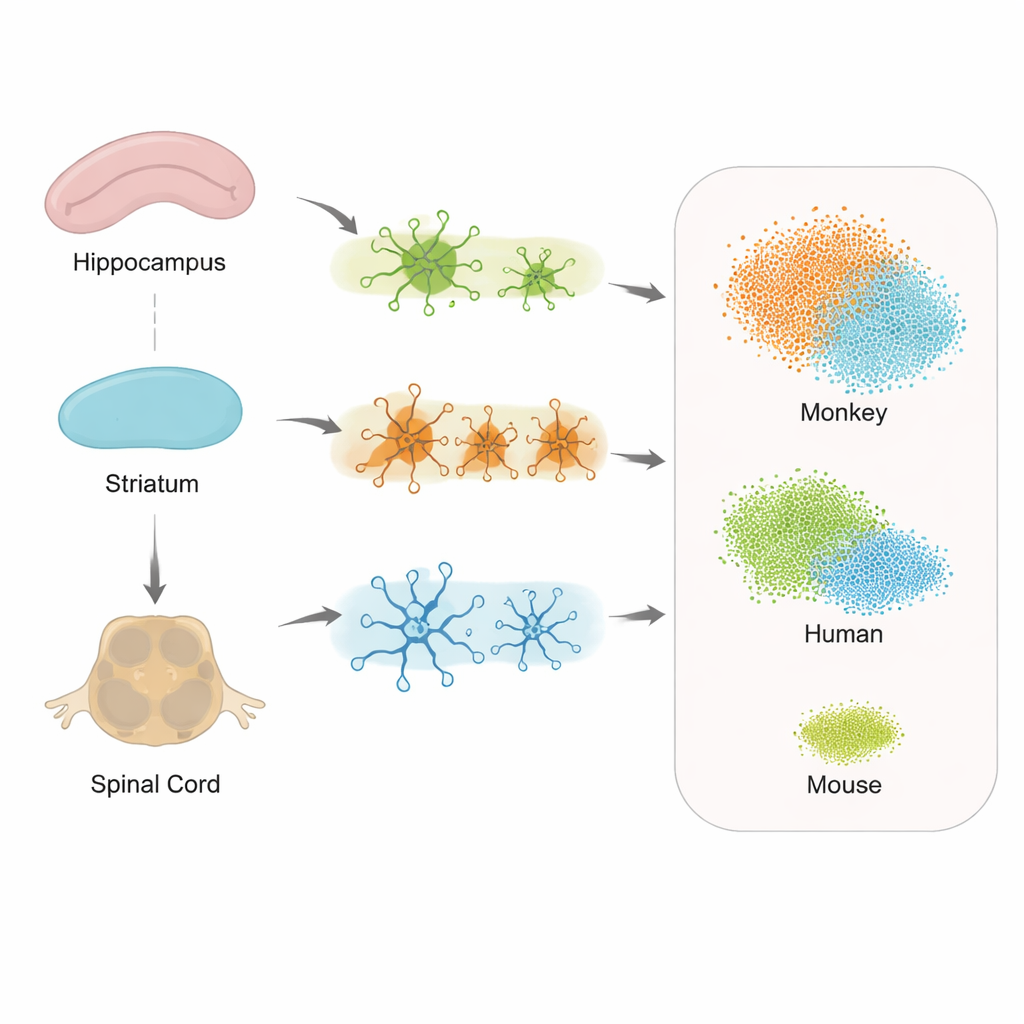
領域ごとに異なる細胞の応答
研究者たちが海馬、線条体、脊髄の支持細胞における遺伝子変化を調べたところ、タウ病理に対して共通の応答と領域特異的な応答の両方が見られました。アストロサイト、ミクログリア、オリゴデンドロサイトはいずれも活性の変化を示しましたが、具体的な遺伝子群は部位によって異なっていました。これは、神経系の各部位がそれぞれ独自のストレス応答を立ち上げることを示唆しており、歩行障害のような症状が明白な記憶障害の前に現れる理由を説明する手助けになるかもしれません。重要な点として、脊髄も強く関与しており、アルツハイマー病が脳だけの疾患ではなく中枢神経系全体の疾患であるという考えを支持します。
ヒトに非常に似たサルのデータ
サルモデルがどれほどヒトの病態を反映しているかを検証するために、チームは海馬データを早発性アルツハイマー病患者の既存データセットや別のタウ変異マウスモデルと比較しました。彼らは特にミクログリアと、ヒト患者で記述されている特別な「疾患関連」状態に焦点を当てました。サルのミクログリアにおける遺伝子発現パターンは、マウスのパターンよりもヒト脳のそれとはるかに重なりが大きく、マウスではほとんど変化しなかった多くの重要な免疫関連やストレス関連遺伝子が含まれていました。これは、Tau-P301Lサルが現行の齧歯類モデルよりも単一細胞レベルでヒトに似た病態シグネチャをとらえていることを示しています。
今後のアルツハイマー研究にとっての意義
専門外の読者に向けた主なメッセージは、この研究がヒト化されたタウタンパク質が我々に近い種の脳と脊髄の細胞にどのように影響するかを細胞ごとに示した、豊富で公開可能なアトラスを提供するという点です。このアトラスは、どの細胞型や領域が最も影響を受けるかを浮き彫りにし、サルモデルが標準的なマウスモデルよりもヒトの免疫細胞変化を忠実に再現することを示しています。その結果、これらのデータはアルツハイマー病の始まりと広がりの仮説を検証するための貴重な試験場を提供し、最終的にヒト患者に到達したときに効果を示す可能性が高い治療法の設計に役立つ可能性があります。
引用: Han, B., Chen, Y., Ouyang, W. et al. Single-nucleus RNA sequencing dataset of diverse tissues from wild-type monkey and Tau-P301L transgenic monkey. Sci Data 13, 497 (2026). https://doi.org/10.1038/s41597-026-06882-4
キーワード: アルツハイマー病, タウタンパク質, ヒト以外霊長類モデル, 単一細胞(単一核)RNAシーケンス, ミクログリア