Clear Sky Science · it
Dataset di sequenziamento RNA di singoli nuclei di tessuti diversi da scimmia selvaggia e scimmia transgenica Tau-P301L
Perché questo studio sulle scimmie è importante
La malattia di Alzheimer è più nota per privare le persone della memoria, ma altera anche il movimento, l’equilibrio e la salute di molti tipi di cellule cerebrali. Per progettare trattamenti migliori, gli scienziati hanno bisogno di modelli animali che riproducano la condizione umana nel modo più fedele possibile. Questo studio presenta una mappa cellulare dettagliata di una scimmia appositamente ingegnerizzata che sviluppa cambiamenti simili all’Alzheimer, offrendo una nuova e potente finestra su come diverse cellule del cervello e del midollo spinale rispondono man mano che la malattia si sviluppa.
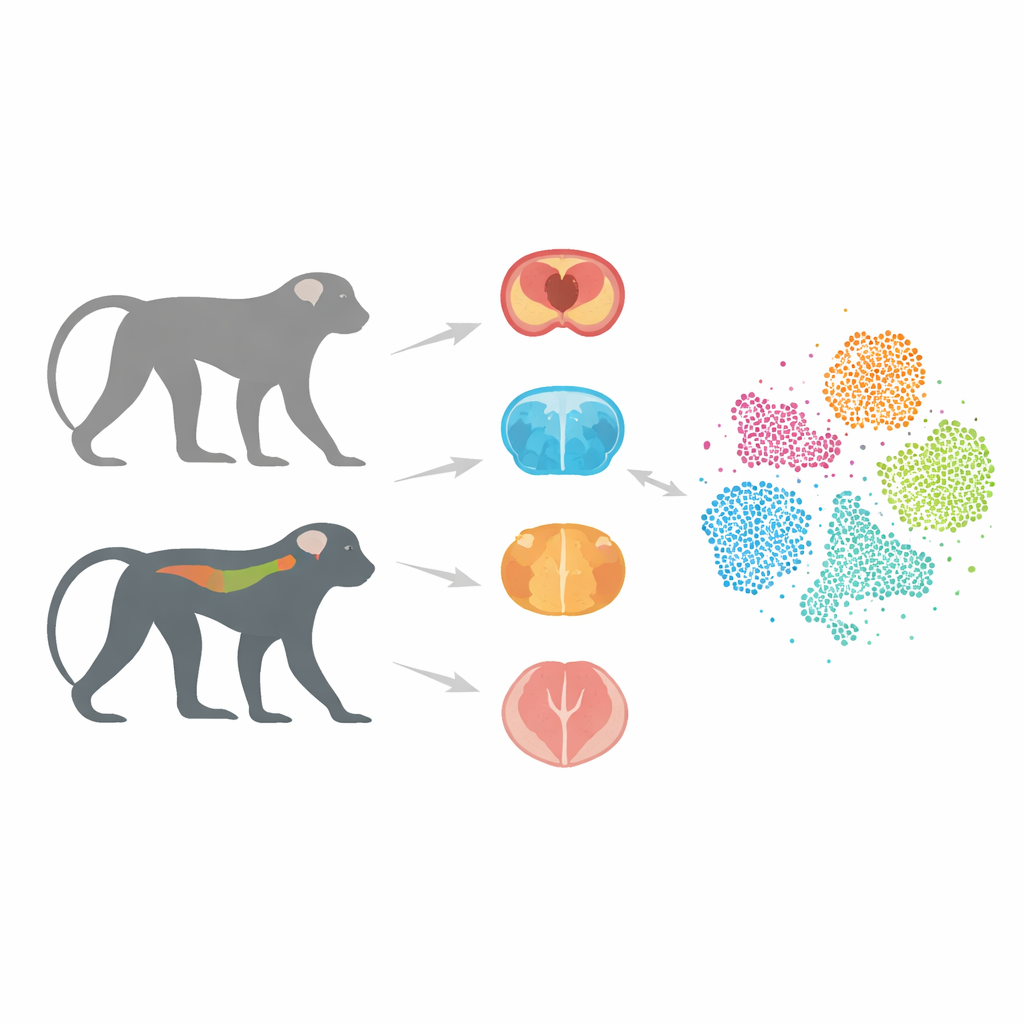
Un sostituto animale più vicino all’uomo
La maggior parte della ricerca sull’Alzheimer si è basata su topi che portano geni umani associati alla malattia. Questi modelli hanno insegnato molto ai ricercatori, ma spesso non riescono a prevedere se un potenziale farmaco funzionerà negli esseri umani. Un motivo principale è che cervelli e sistemi immunitari dei topi differiscono notevolmente dai nostri. Le scimmie, al contrario, condividono una struttura cerebrale e un corredo genico molto più simili a quelli umani. In lavori precedenti, gli autori hanno creato scimmie macaco cynamolgus che portano una versione umana della proteina tau, chiamata Tau-P301L, che si aggrega in modo anomalo in diverse forme di demenza. Queste scimmie sviluppano gradualmente danni ai neuroni e problemi di movimento, assomigliando a caratteristiche chiave delle malattie guidate dalla tau nell’uomo.
Leggere i messaggi all’interno di migliaia di cellule
In questo progetto, il team si è concentrato su tre regioni chiave: l’ippocampo, importante per la memoria; il corpo striato, coinvolto nel movimento e nella motivazione; e il midollo spinale, che aiuta a controllare la postura e la deambulazione ed è sempre più riconosciuto come parte del quadro dell’Alzheimer. Da scimmie transgeniche e sane, i ricercatori hanno isolato nuclei individuali da cellule di questi tessuti e hanno utilizzato il sequenziamento dell’RNA di singoli nuclei. Questa tecnica legge quali geni sono attivi in ciascuna cellula, permettendo di distinguere tipi e stati cellulari con grande precisione. Dopo attenti controlli di qualità per rimuovere cellule danneggiate ed errori tecnici, hanno compilato un atlante di 36.623 cellule ad alta qualità.
Una mappa cellulare del sistema nervoso della scimmia
Raggruppando cellule con schemi di attività genica simili, il team ha identificato 13 tipi cellulari principali, inclusi neuroni, diversi tipi di cellule di supporto come astrociti e oligodendrociti, microglia simili a cellule immunitarie e popolazioni rare come cellule T e cellule della zona ventricolare. Hanno verificato ciascun gruppo usando geni marker noti e hanno mostrato che i cluster erano chiari e coerenti. Confrontando scimmie malate e sane, hanno rilevato che alcune microglia—un tipo di cellula immunitaria cerebrale—erano aumentate negli animali Tau-P301L. Queste microglia esprimevano geni precedentemente collegati al riconoscimento del danno e a risposte infiammatorie osservate attorno ai depositi proteici nei cervelli umani con Alzheimer, suggerendo che il modello di scimmia cattura una reazione immunitaria importante assente o attenuata in molti studi su topo.
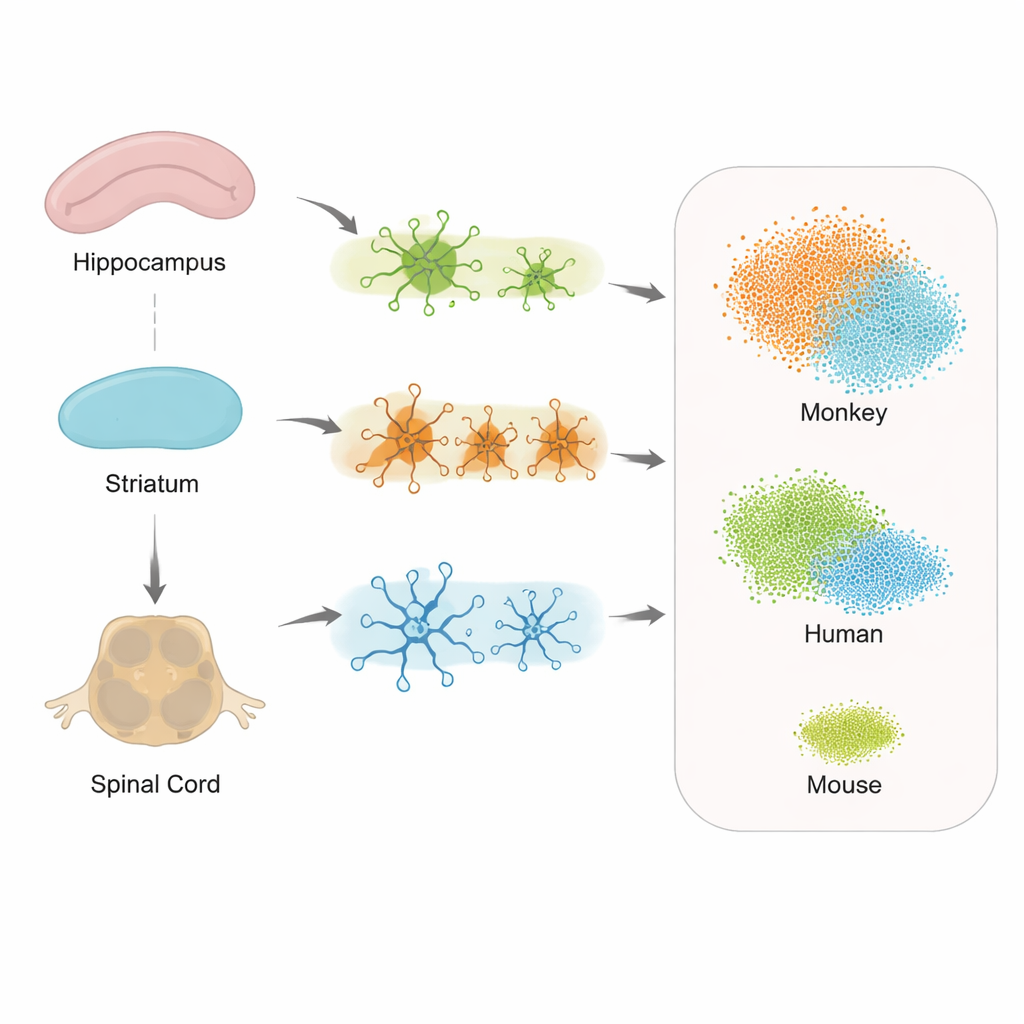
Regioni diverse, risposte cellulari diverse
Quando i ricercatori hanno esaminato come i geni cambiassero nelle cellule di supporto nell’ippocampo, nel corpo striato e nel midollo spinale, hanno osservato risposte sia condivise sia specifiche per regione alla patologia da tau. Astrociti, microglia e oligodendrociti mostravano tutti attività alterata, ma gli insiemi precisi di geni variavano in base alla localizzazione. Questo suggerisce che ogni parte del sistema nervoso monta la propria versione di una risposta allo stress, il che potrebbe aiutare a spiegare perché alcuni sintomi, come le difficoltà nel camminare, possono comparire prima della perdita di memoria evidente. È importante sottolineare che il midollo spinale mostrava un coinvolgimento significativo, sostenendo l’idea che l’Alzheimer non sia solo una malattia del cervello, ma del più ampio sistema nervoso centrale.
Dati delle scimmie che assomigliano notevolmente all’umano
Per verificare quanto bene il modello di scimmia rispecchiasse la malattia umana, il team ha confrontato i propri dati ippocampali con dataset esistenti di persone con Alzheimer a insorgenza precoce e con un altro modello murino con mutazione tau. Hanno focalizzato l’attenzione sulle microglia e su uno speciale stato «associato alla malattia» di queste cellule descritto nei pazienti umani. I modelli di attività genica nelle microglia della scimmia si sovrapponevano molto più a quelli dei cervelli umani rispetto ai modelli murini, includendo molti geni chiave legati all’immunità e allo stress che cambiavano poco nei topi. Ciò indica che la scimmia Tau-P301L cattura firme della malattia simili a quelle umane a livello di singola cellula meglio degli attuali modelli roditori.
Cosa significa questo per la ricerca futura sull’Alzheimer
Per i non specialisti, il messaggio principale è che questo studio fornisce una ricca mappa cellula-per-cellula, pubblicamente disponibile, di come una proteina tau umanizzata interrompe le cellule del cervello e del midollo spinale in una specie molto più vicina a noi rispetto ai topi. L’atlante mette in evidenza quali tipi cellulari e regioni sono più colpiti e mostra che il modello di scimmia riproduce i cambiamenti delle cellule immunitarie umane in modo più fedele rispetto ai modelli murini standard. Di conseguenza, questi dati offrono un campo di prova prezioso per idee su come l’Alzheimer inizia e si diffonde, e potrebbero aiutare i ricercatori a progettare terapie che abbiano maggiori probabilità di funzionare quando arriveranno finalmente ai pazienti umani.
Citazione: Han, B., Chen, Y., Ouyang, W. et al. Single-nucleus RNA sequencing dataset of diverse tissues from wild-type monkey and Tau-P301L transgenic monkey. Sci Data 13, 497 (2026). https://doi.org/10.1038/s41597-026-06882-4
Parole chiave: Malattia di Alzheimer, proteina tau, modello di primate non umano, sequenziamento RNA a singola cellula, microglia