Clear Sky Science · pl
Zbiór danych pojedynczego jądrowego sekwencjonowania RNA z różnych tkanek małpy typu dzikiego i transgenicznej małpy Tau-P301L
Dlaczego to badanie na małpach ma znaczenie
Choroba Alzheimera jest powszechnie kojarzona z utratą pamięci, ale wpływa też na ruch, równowagę i stan wielu typów komórek mózgu. Aby opracować lepsze terapie, naukowcy potrzebują modeli zwierzęcych jak najbardziej odzwierciedlających warunki u ludzi. To badanie przedstawia szczegółową mapę komórkową specjalnie zmodyfikowanej małpy, która rozwija zmiany podobne do tych występujących w chorobie Alzheimera, oferując nową, potężną perspektywę na to, jak różne komórki mózgu i rdzenia reagują w miarę postępu choroby.
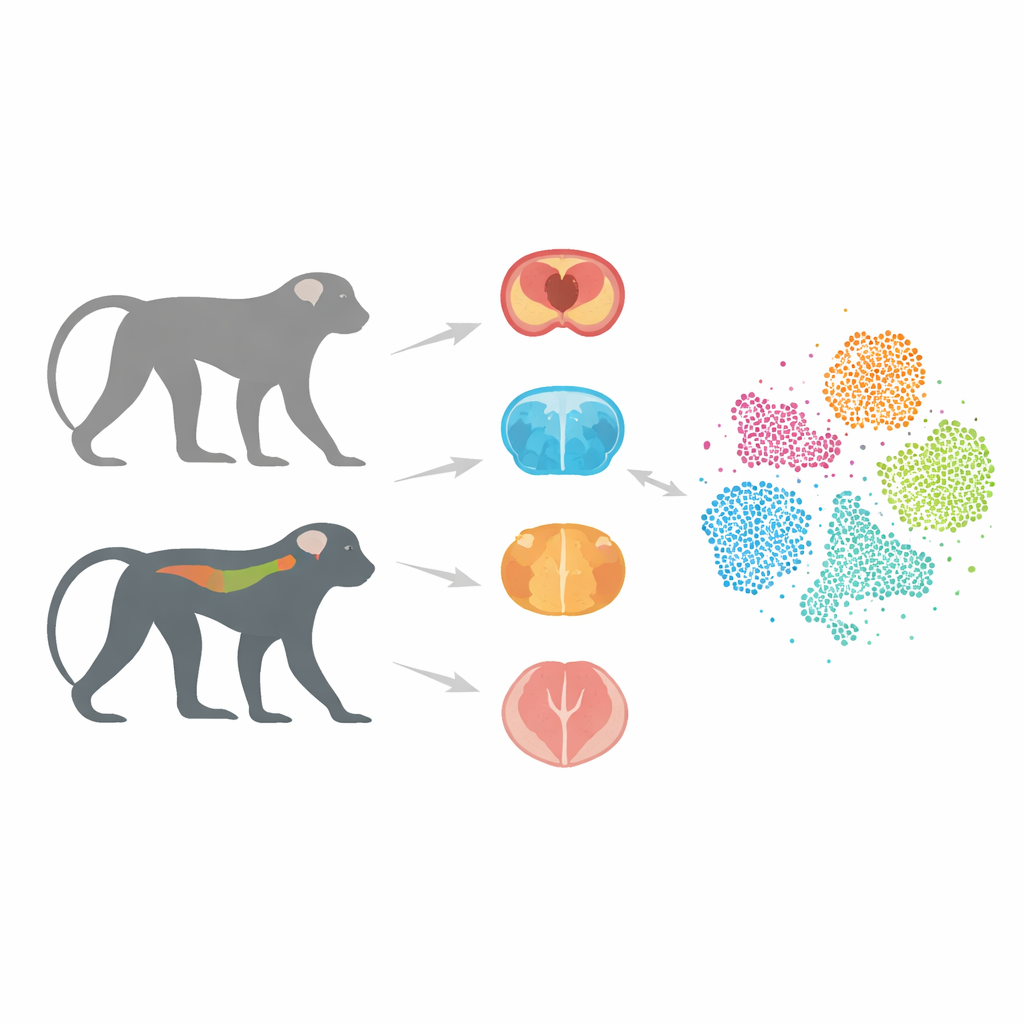
Bliższy zwierzęcy odpowiednik człowieka
Większość badań nad Alzheimerem opiera się na myszach niosących ludzkie geny związane z chorobą. Modele te wiele nas nauczyły, ale często zawodzą przy przewidywaniu, czy dany lek zadziała u ludzi. Jednym z powodów są zasadnicze różnice między mózgami i układami odpornościowymi myszy i ludzi. Małpy natomiast mają znacznie podobniejszą budowę mózgu i zestaw genów. W wcześniejszych pracach autorzy stworzyli makaki krótkogoniaste (cynomolgus) przenoszące ludzką wersję białka tau, zwaną Tau-P301L, która wykazuje nieprawidłowe agregowanie w kilku otępieniach. Te małpy stopniowo rozwijają uszkodzenia neuronów i problemy z ruchem, przypominając kluczowe cechy chorób napędzanych patologią tau u ludzi.
Odczytywanie informacji w tysiącach komórek
W tym projekcie zespół skoncentrował się na trzech kluczowych obszarach: hipokampie, istotnym dla pamięci; prążkowiu, zaangażowanym w ruch i motywację; oraz rdzeniu kręgowym, który kontroluje postawę i chód i coraz częściej uznawany jest za część obrazu choroby Alzheimera. Zarówno z małp transgenicznych, jak i zdrowych, badacze izolowali pojedyncze jądra z komórek tych tkanek i zastosowali pojedyncze jądrowe sekwencjonowanie RNA. Ta technika odczytuje, które geny są aktywne w każdej komórce, pozwalając rozróżnić typy i stany komórkowe z dużą precyzją. Po starannych kontrolach jakości w celu usunięcia uszkodzonych komórek i błędów technicznych skompilowali atlasy obejmujące 36 623 wysokiej jakości komórek.
Mapa komórkowa układu nerwowego małpy
Grupując komórki o podobnych wzorcach aktywności genów, zespół zidentyfikował 13 głównych typów komórek, w tym neurony, kilka rodzajów komórek wspierających, takich jak astrocyty i oligodendrocyty, komórko-podobne mikrogleju, oraz rzadkie populacje, jak komórki T i komórki strefy komorowej. Każdą grupę zweryfikowano za pomocą znanych genów markerowych i wykazano, że klastry były czyste i spójne. Porównując małpy chore i zdrowe, stwierdzono, że określone populacje mikrogleju — rodzaju komórek odpornościowych mózgu — zwiększyły się u zwierząt Tau-P301L. Te mikrogleje eksprymowały geny wcześniej powiązane z wykrywaniem uszkodzeń i odpowiedziami zapalnymi obserwowanymi wokół złogów białkowych w ludzkich mózgach chorych na Alzheimera, co sugeruje, że model małpi odzwierciedla ważną reakcję immunologiczną, która bywa nieobecna lub stłumiona w wielu badaniach na myszach.
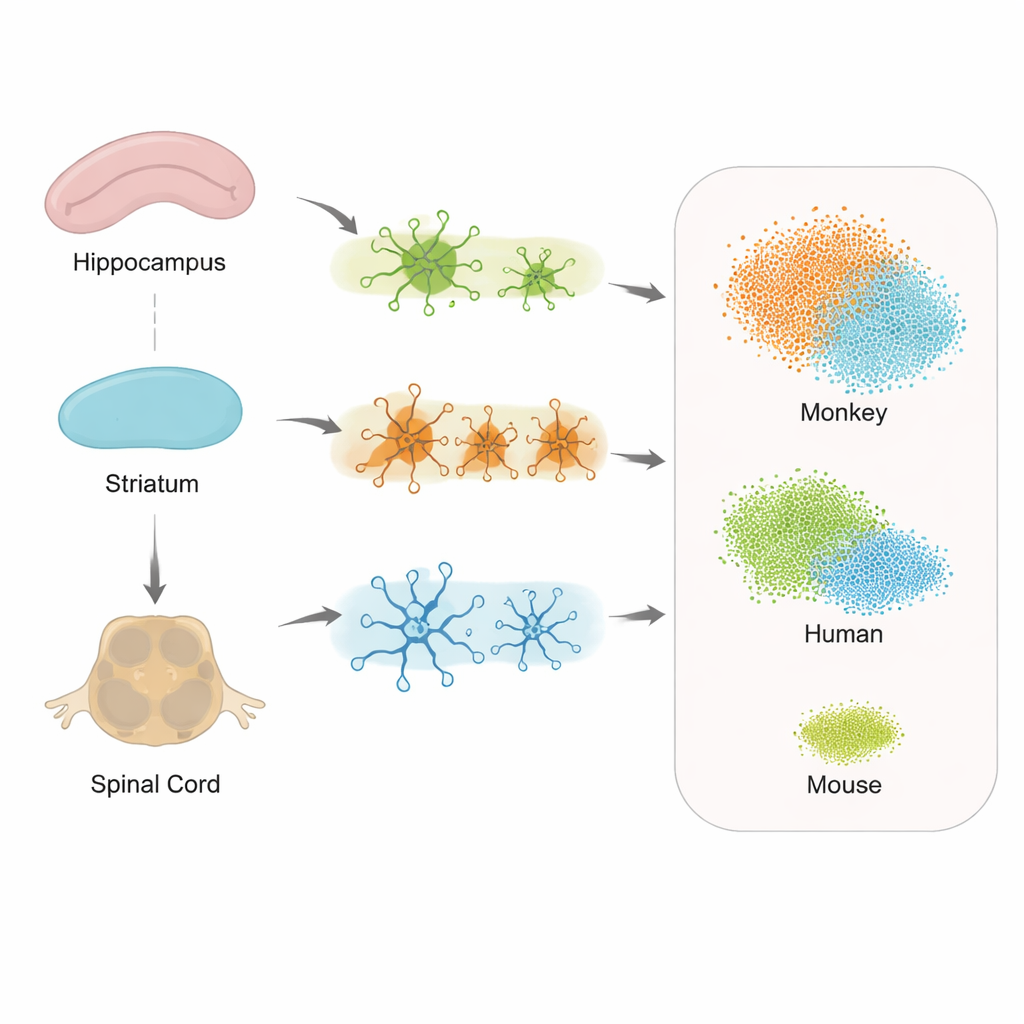
Różne regiony, różne reakcje komórek
Gdy badacze analizowali zmiany ekspresji genów w komórkach wspierających w hipokampie, prążkowiu i rdzeniu kręgowym, zaobserwowali zarówno wspólne, jak i specyficzne dla regionu reakcje na patologię tau. Astrocyty, mikroglej i oligodendrocyty wykazywały zmienioną aktywność, lecz dokładne zbiory genów różniły się w zależności od lokalizacji. Sugeruje to, że każda część układu nerwowego uruchamia własną wersję odpowiedzi na stres, co może pomagać tłumaczyć, dlaczego niektóre objawy, jak trudności w chodzeniu, mogą pojawiać się wcześniej niż wyraźna utrata pamięci. Co istotne, rdzeń kręgowy wykazał silne zaangażowanie, co wspiera pogląd, że Alzheimer nie jest chorobą jedynie mózgu, lecz szerszego układu nerwowego.
Dane z małp wyglądające uderzająco ludzko
Aby sprawdzić, jak dobrze model małpi odzwierciedla chorobę u ludzi, zespół porównał swoje dane z hipokampa z istniejącymi zestawami danych od osób z wczesnym początkiem choroby Alzheimera oraz z innym mysim modelem z mutacją tau. Skoncentrowali się na mikrogleju i na specjalnym «stanie związanym z chorobą» tych komórek opisywanym u pacjentów ludzkich. Wzorce aktywności genów w mikrogleju małp pokrywały się znacznie bardziej z tymi w ludzkich mózgach niż wzorce mysie, obejmując wiele kluczowych genów związanych z odpornością i stresem, które u myszy niemal się nie zmieniały. Wskazuje to, że małpa Tau-P301L najlepiej odwzorowuje sygnatury choroby podobne do ludzkich na poziomie pojedynczych komórek, lepiej niż obecne modele gryzoniowe.
Co to znaczy dla przyszłych badań nad Alzheimerem
Dla osób niebędących specjalistami główne przesłanie jest takie: to badanie udostępnia bogatą, publicznie dostępną mapę komórka po komórce pokazującą, jak udomowiona wersja białka tau zakłóca funkcjonowanie komórek mózgu i rdzenia w gatunku znacznie bliższym nam niż myszy. Atlas wskazuje, które typy komórek i regiony są najbardziej dotknięte oraz pokazuje, że model małpi wierniej odwzorowuje zmiany w komórkach odpornościowych ludzi niż standardowe modele mysie. W rezultacie dane te stanowią cenne pole do testowania hipotez o tym, jak zaczyna się i rozprzestrzenia Alzheimer, i mogą pomóc naukowcom w projektowaniu terapii mających większe szanse powodzenia u pacjentów.
Cytowanie: Han, B., Chen, Y., Ouyang, W. et al. Single-nucleus RNA sequencing dataset of diverse tissues from wild-type monkey and Tau-P301L transgenic monkey. Sci Data 13, 497 (2026). https://doi.org/10.1038/s41597-026-06882-4
Słowa kluczowe: choroba Alzheimera, białko tau, model naczelnych niebędący człowiekiem, sekwencjonowanie RNA pojedynczych komórek, mikroglej