Clear Sky Science · fr
Jeu de données de séquençage ARN unicellulaire des noyaux de tissus divers chez le singe sauvage-type et le singe transgénique Tau-P301L
Pourquoi cette étude sur le singe est importante
La maladie d’Alzheimer est surtout connue pour voler la mémoire des personnes, mais elle altère aussi le mouvement, l’équilibre et la santé de nombreux types de cellules cérébrales. Pour concevoir de meilleurs traitements, les chercheurs ont besoin de modèles animaux qui reproduisent la maladie humaine aussi fidèlement que possible. Cette étude présente une carte cellulaire détaillée d’un singe spécialement modifié qui développe des changements proches de l’Alzheimer, offrant une nouvelle fenêtre puissante sur la manière dont différentes cellules du cerveau et de la moelle épinière réagissent à l’apparition de la maladie.
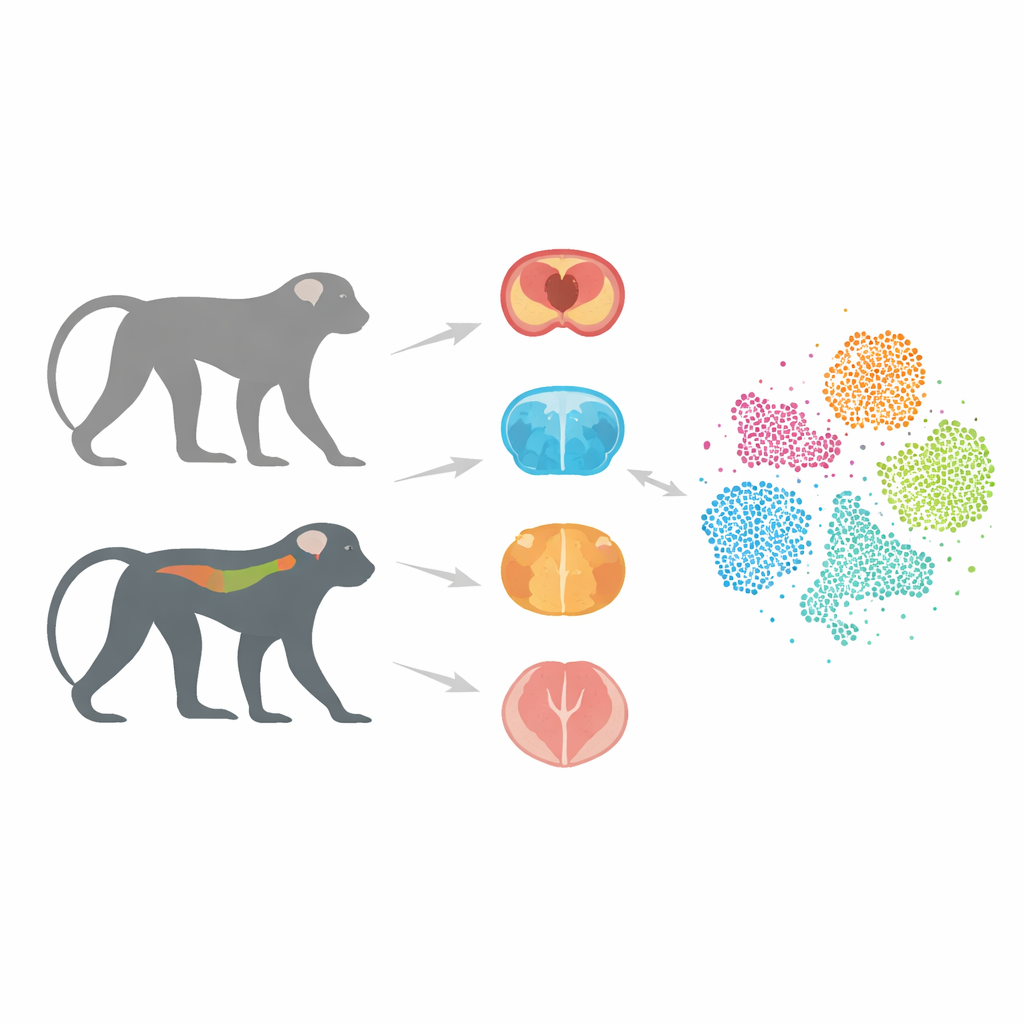
Un substitut animal plus proche de l’humain
La plupart des recherches sur Alzheimer ont reposé sur des souris porteuses de gènes humains liés à la maladie. Ces modèles ont beaucoup appris aux chercheurs, mais ils échouent souvent à prédire si un médicament potentiel fonctionnera chez l’homme. Une raison majeure est que les cerveaux et les systèmes immunitaires des souris diffèrent fortement des nôtres. Les singes, en revanche, partagent une structure cérébrale et un patrimoine génétique bien plus proches de ceux des humains. Dans des travaux antérieurs, les auteurs ont créé des macaques cynomolgus portant une version humaine de la protéine tau, appelée Tau-P301L, qui s’agrège anormalement dans plusieurs démences. Ces singes développent progressivement des lésions neuronales et des troubles moteurs, ressemblant à des caractéristiques clés de la maladie tau humaine.
Lire les messages à l’intérieur de milliers de cellules
Dans ce projet, l’équipe s’est concentrée sur trois régions clés : l’hippocampe, important pour la mémoire ; le striatum, impliqué dans le mouvement et la motivation ; et la moelle épinière, qui aide à contrôler la posture et la marche et est de plus en plus reconnue comme faisant partie du tableau de l’Alzheimer. À partir de singes transgéniques et sains, les chercheurs ont isolé des noyaux individuels de cellules de ces tissus et utilisé le séquençage ARN des noyaux uniques. Cette technique lit les gènes actifs dans chaque cellule, permettant de distinguer les types et états cellulaires avec une grande précision. Après des contrôles de qualité rigoureux pour éliminer les cellules endommagées et les artefacts techniques, ils ont compilé un atlas de 36 623 cellules de haute qualité.
Une carte cellulaire du système nerveux du singe
En groupant les cellules selon des motifs d’activité génique similaires, l’équipe a identifié 13 types cellulaires majeurs, incluant des neurones, plusieurs types de cellules de soutien telles que les astrocytes et les oligodendrocytes, des microglies de type immunitaire, et des populations rares comme les lymphocytes T et les cellules de la zone ventriculaire. Ils ont vérifié chaque groupe à l’aide de gènes marqueurs connus et montré que les clusters étaient nets et cohérents. En comparant singes malades et sains, ils ont constaté que certaines microglies — un type de cellule immunitaire cérébrale — s’étaient multipliées chez les animaux Tau-P301L. Ces microglies exprimaient des gènes déjà associés à la détection de dommages et à des réponses inflammatoires observées autour des dépôts protéiques dans les cerveaux d’Alzheimer humains, suggérant que le modèle de singe capture une réaction immunitaire importante absente ou atténuée dans de nombreuses études sur la souris.
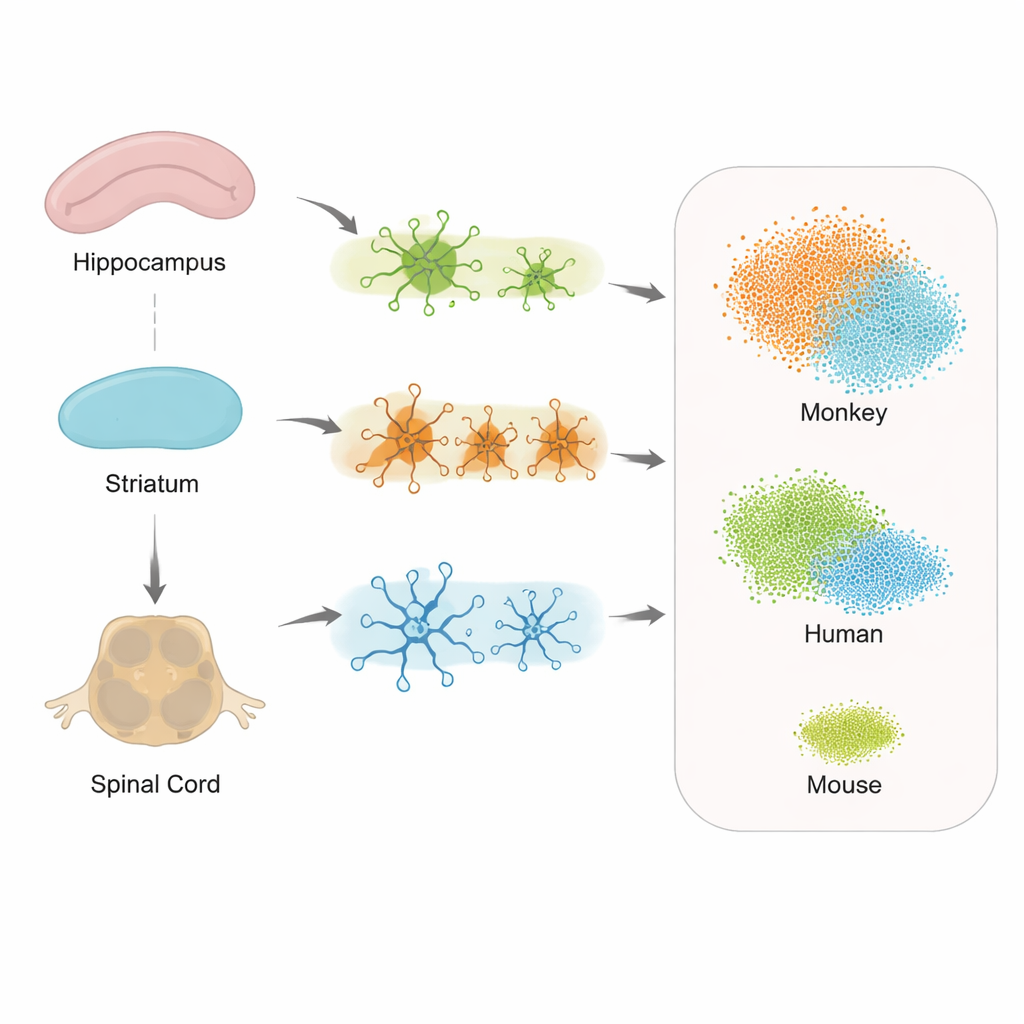
Régions différentes, réponses cellulaires différentes
Lorsque les chercheurs ont examiné les modifications d’expression génique dans les cellules de soutien à travers l’hippocampe, le striatum et la moelle épinière, ils ont observé des réponses à la pathologie tau à la fois partagées et spécifiques à chaque région. Astrocytes, microglies et oligodendrocytes ont tous montré une activité modifiée, mais les jeux de gènes exacts variaient selon l’emplacement. Cela suggère que chaque partie du système nerveux déclenche sa propre version d’une réponse au stress, ce qui pourrait aider à expliquer pourquoi certains symptômes, comme des difficultés à marcher, peuvent apparaître avant une perte de mémoire évidente. Fait important, la moelle épinière montrait une forte implication, soutenant l’idée que l’Alzheimer n’est pas uniquement une maladie du cerveau, mais du système nerveux central dans son ensemble.
Des données de singe étonnamment proches de l’humain
Pour tester dans quelle mesure le modèle de singe reflète la maladie humaine, l’équipe a comparé ses données hippocampiques à des ensembles de données existants de patients atteints d’Alzheimer à début précoce et à un autre modèle murin mutant pour la tau. Ils se sont concentrés sur les microglies et sur un état particulier « associé à la maladie » de ces cellules qui a été décrit chez les patients humains. Les motifs d’expression génique des microglies du singe se recoupaient beaucoup plus avec ceux des cerveaux humains que ne le faisaient les motifs murins, incluant de nombreux gènes clés liés à l’immunité et au stress qui changeaient à peine chez la souris. Cela indique que le singe Tau-P301L capture des signatures de la maladie ressemblant à celles de l’humain au niveau unicellulaire mieux que les modèles rongeurs actuels.
Ce que cela signifie pour la recherche future sur l’Alzheimer
Pour les non-spécialistes, le message principal est que cette étude fournit une riche carte cellule par cellule, accessible publiquement, montrant comment une protéine tau humanisée perturbe les cellules du cerveau et de la moelle épinière dans une espèce bien plus proche de nous que la souris. L’atlas met en évidence les types cellulaires et les régions les plus touchés et montre que le modèle de singe reproduit plus fidèlement les changements des cellules immunitaires observés chez l’homme que les modèles murins standard. En conséquence, ces données offrent un terrain d’essai précieux pour des hypothèses sur le démarrage et la propagation de l’Alzheimer, et elles pourraient aider les chercheurs à concevoir des thérapies ayant de meilleures chances de fonctionner lorsqu’elles seront enfin testées chez l’homme.
Citation: Han, B., Chen, Y., Ouyang, W. et al. Single-nucleus RNA sequencing dataset of diverse tissues from wild-type monkey and Tau-P301L transgenic monkey. Sci Data 13, 497 (2026). https://doi.org/10.1038/s41597-026-06882-4
Mots-clés: Maladie d’Alzheimer, protéine tau, modèle de primate non humain, séquençage ARN unicellulaire, microglie