Clear Sky Science · sv
Single-nucleus RNA-sekvenseringsdataset från olika vävnader hos vildtyp-apa och Tau-P301L transgen apa
Varför denna studie på apor är viktig
Alzheimers sjukdom är mest känd för att beröva människor minnet, men den påverkar också rörelse, balans och hälsan hos många typer av hjärnceller. För att utveckla bättre behandlingar behöver forskare djurmodeller som efterliknar det mänskliga tillståndet så nära som möjligt. Denna studie presenterar en detaljerad cellkarta från en särskilt konstruerad apa som utvecklar Alzheimer-liknande förändringar, och erbjuder ett kraftfullt nytt fönster in i hur olika hjärn- och ryggmärgsceller reagerar när sjukdomen tar fart.
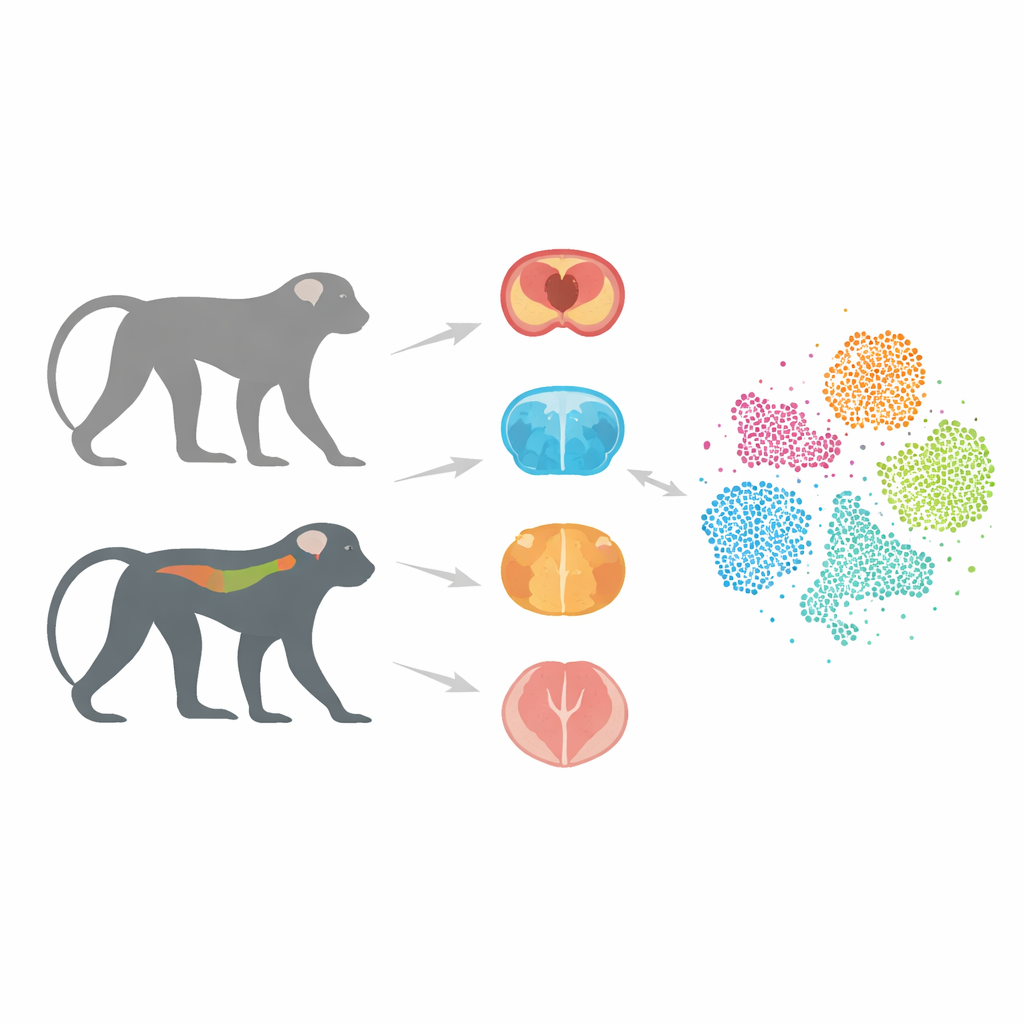
En närmare djurmässig ersättning för människor
Större delen av Alzheimerforskningen har förlitat sig på möss som bär mänskliga gener kopplade till sjukdomen. Dessa modeller har lärt forskare mycket, men de förutser ofta inte om ett potentiellt läkemedel kommer att fungera hos människor. En stor anledning är att mushjärnor och immunsystem skiljer sig markant från våra. Apor, däremot, delar en mycket mer lik hjärnstruktur och genuppsättning med människor. I tidigare arbete skapade författarna cynomolgusapor som bär en mänsklig variant av tauproteinet, kallad Tau-P301L, som klumpar ihop sig abnormt i flera demenssjukdomar. Dessa apor utvecklar gradvis nervcellsskador och rörelseproblem som liknar viktiga drag hos människans tau-drivna sjukdom.
Att läsa budskapen inuti tusentals celler
I detta projekt fokuserade teamet på tre nyckelregioner: hippocampus, viktig för minne; striatum, involverad i rörelse och motivation; och ryggmärgen, som hjälper till att kontrollera hållning och gång och som i allt högre grad erkänns som en del av Alzheimers bild. Från både transgena och friska apor isolerade forskarna individuella kärnor från celler i dessa vävnader och använde single-nucleus RNA-sekvensering. Denna teknik läser vilka gener som är aktiva i varje cell och gör det möjligt för forskare att särskilja celltyper och celltillstånd med stor precision. Efter noggranna kvalitetskontroller för att avlägsna skadade celler och tekniska fel sammanställde de en atlas med 36 623 högkvalitativa celler.
En cellulär karta över apans nervsystem
Genom att gruppera celler med liknande genaktivitetsmönster identifierade teamet 13 huvudsakliga celltyper, inklusive neuroner, flera typer stödjeceller såsom astrocyter och oligodendrocyter, immunsystemsliknande mikroglia och sällsynta populationer som T‑celler och ventrikulära zonceller. De verifierade varje grupp med hjälp av kända markörgener och visade att klusterna var rena och konsekventa. Genom att jämföra sjuka och friska apor fann de att vissa mikroglia — en typ av hjärnans immunceller — expanderade hos Tau-P301L-djuren. Dessa mikroglia uttryckte gener som tidigare kopplats till skadegörande- och inflammatoriska svar som ses runt proteinavlagringar i mänskliga Alzheimers-hjärnor, vilket antyder att apmodellen fångar en viktig immunreaktion som saknas eller dämpas i många studier på möss.
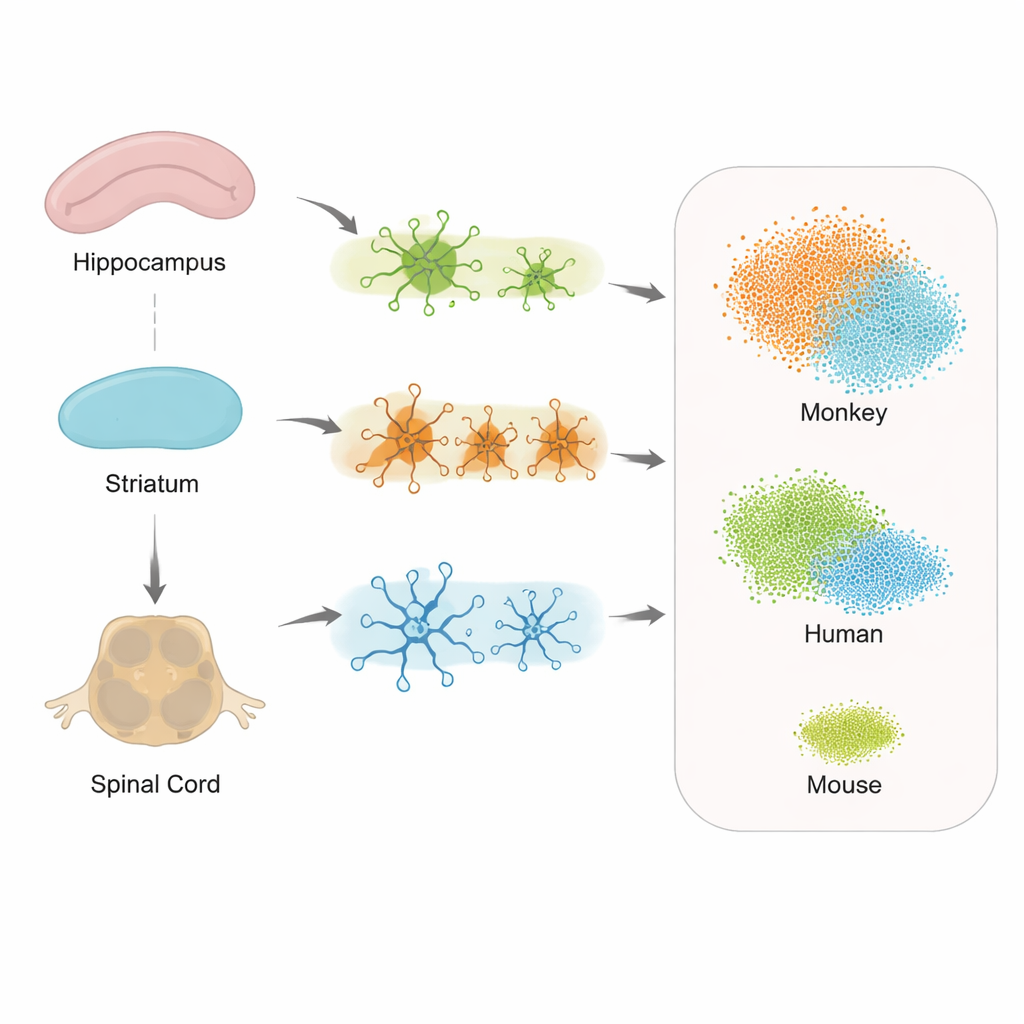
Olika regioner, olika cellulära svar
När forskarna undersökte hur gener ändrades i stödjeceller över hippocampus, striatum och ryggmärg såg de både gemensamma och regionsspecifika svar på taupatologi. Astrocyter, mikroglia och oligodendrocyter visade alla förändrad aktivitet, men de exakta genuppsättningarna varierade efter plats. Detta tyder på att varje del av nervsystemet monterar upp sin egen version av ett stressvar, vilket kan bidra till att förklara varför vissa symptom, som gångsvårigheter, kan uppträda före tydliga minnesproblem. Viktigt är att ryggmärgen visade starkt engagemang, vilket stödjer idén att Alzheimer inte bara är en hjärnsjukdom utan en sjukdom i det bredare centrala nervsystemet.
Apodata som ser slående mänskliga ut
För att testa hur väl apmodellen speglar mänsklig sjukdom jämförde teamet sina hippocampusdata med befintliga dataset från personer med tidigt debuterande Alzheimer och från en annan tau-mutant musmodell. De fokuserade på mikroglia och på ett särskilt ”disease-associated” tillstånd hos dessa celler som beskrivits hos mänskliga patienter. Genaktivitetsmönstren i apa-mikroglia överlappade i mycket större utsträckning med dem i mänskliga hjärnor än musmönstren gjorde, inklusive många centrala immunsvars- och stressrelaterade gener som knappt ändrades hos möss. Detta indikerar att Tau-P301L-apan fångar mänskliga sjukdomssignaturer på single-cell-nivå bättre än nuvarande gnagarmodeller.
Vad detta betyder för framtida Alzheimerforskning
För icke-specialister är huvudbudskapet att denna studie levererar en rik, publikt tillgänglig cell-för-cell-karta över hur ett humaniserat tauprotein stör hjärn- och ryggmärgsceller i en art mycket närmare oss än möss. Atlassen belyser vilka celltyper och regioner som påverkas mest och visar att apmodellen reproducerar mänskliga immuncellsförändringar mer troget än standardmusmodeller. Som en följd erbjuder dessa data en värdefull testbädd för idéer om hur Alzheimers börjar och sprider sig, och de kan hjälpa forskare att utforma terapier som har större chans att fungera när de slutligen når mänskliga patienter.
Citering: Han, B., Chen, Y., Ouyang, W. et al. Single-nucleus RNA sequencing dataset of diverse tissues from wild-type monkey and Tau-P301L transgenic monkey. Sci Data 13, 497 (2026). https://doi.org/10.1038/s41597-026-06882-4
Nyckelord: Alzheimers sjukdom, tauprotein, modell med icke-mänsklig primat, single-cell RNA-sekvensering, mikroglia