Clear Sky Science · nl
Single-nucleus RNA-sequencing dataset van diverse weefsels van wildtype-aap en Tau-P301L transgene aap
Waarom deze aapstudie van belang is
De ziekte van Alzheimer staat vooral bekend om het ontnemen van geheugen, maar verandert ook beweging, evenwicht en de gezondheid van veel typen hersencellen. Om betere behandelingen te ontwikkelen hebben wetenschappers diermodellen nodig die de menselijke aandoening zo nauwkeurig mogelijk nabootsen. Deze studie introduceert een gedetailleerde cellulaire kaart van een speciaal geconstrueerde aap die Alzheimer-achtige veranderingen ontwikkelt, en biedt daarmee een krachtig nieuw venster op hoe verschillende cellen van hersenen en ruggenmerg reageren naarmate de ziekte vordert.
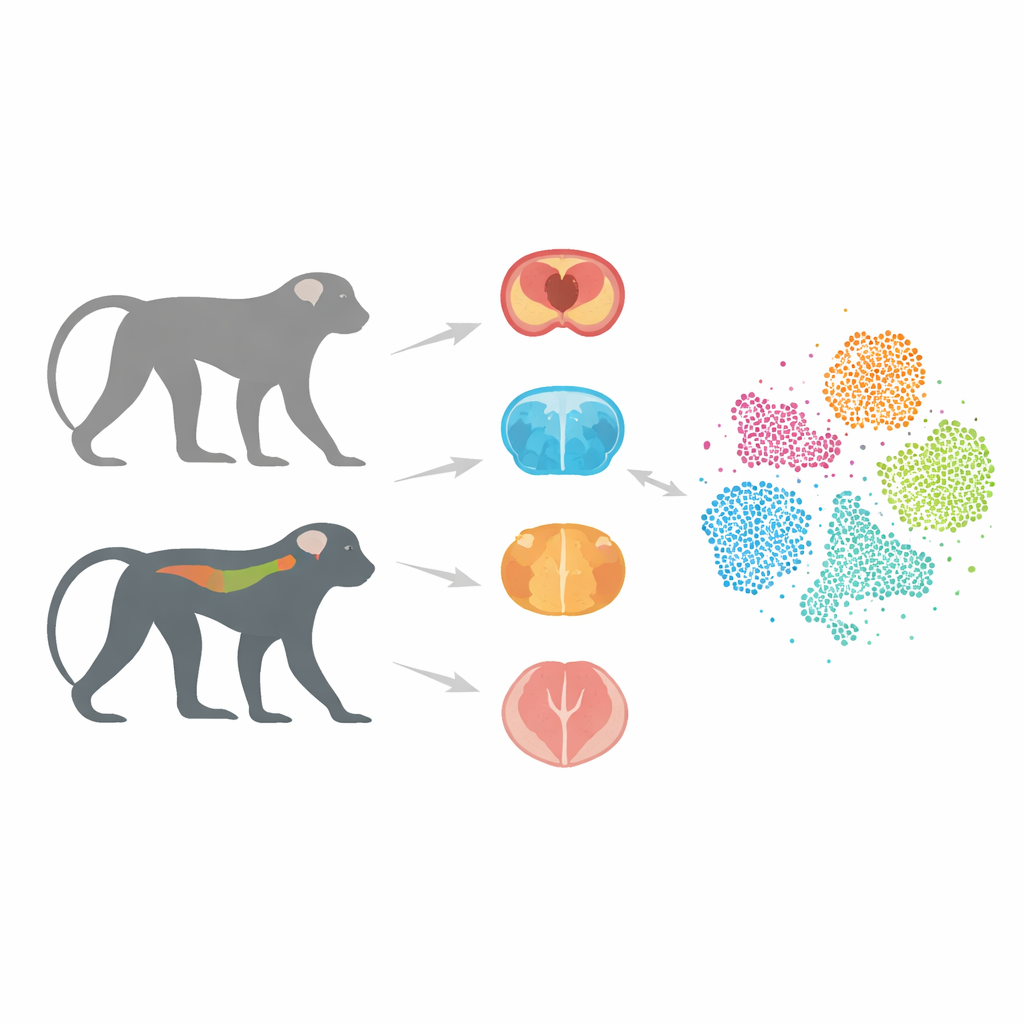
Een dichterbij staande diervervanger voor mensen
Het merendeel van Alzheimer-onderzoek heeft gebruikgemaakt van muizen die menselijke genen dragen die met de ziekte in verband worden gebracht. Deze modellen hebben onderzoekers veel geleerd, maar voorspellen vaak niet betrouwbaar of een mogelijk geneesmiddel bij mensen zal werken. Een belangrijke reden is dat muizenhersenen en immuunsystemen sterk verschillen van die van ons. Apen daarentegen delen een veel vergelijkbaardere hersenstructuur en genetische samenstelling met mensen. In eerder werk creëerden de auteurs cynomolgusapen die een menselijke variant van het tau-eiwit dragen, Tau-P301L, dat bij meerdere vormen van dementie abnormaal samenklontert. Deze apen ontwikkelen geleidelijk zenuwcelbeschadiging en bewegingsproblemen, die belangrijke kenmerken van bij mensen door tau aangedreven ziekte nabootsen.
De boodschappen lezen binnen duizenden cellen
In dit project richtte het team zich op drie belangrijke gebieden: de hippocampus, belangrijk voor geheugen; het striatum, betrokken bij beweging en motivatie; en het ruggenmerg, dat houding en lopen helpt te regelen en dat steeds meer wordt erkend als deel van het Alzheimer‑beeld. Van zowel transgene als gezonde apen isoleerden de onderzoekers individuele kernen uit cellen in deze weefsels en gebruikten single-nucleus RNA-sequencing. Deze techniek leest af welke genen in elke cel actief zijn, waardoor wetenschappers celtypes en -toestanden met hoge precisie kunnen onderscheiden. Na zorgvuldige kwaliteitscontroles om beschadigde cellen en technische fouten te verwijderen, stelden ze een atlas samen van 36.623 hoogwaardige cellen.
Een cellulaire kaart van het aapzenuwstelsel
Door cellen met vergelijkbare genactiviteitspatronen te groeperen identificeerde het team 13 hoofdceltypes, waaronder neuronen, verschillende soorten ondersteunende cellen zoals astrocyten en oligodendrocyten, immuunachtige microglia, en zeldzame populaties zoals T‑cellen en cellen uit de ventrikelzone. Ze verifieerden elke groep met bekende markergenen en toonden aan dat de clusters schoon en consistent waren. In vergelijking tussen zieke en gezonde apen vonden ze dat bepaalde microglia—een type hersenimmuuncel—uitgebreid waren in de Tau-P301L‑dieren. Deze microglia drukten genen uit die eerder in verband zijn gebracht met schade‑detectie en ontstekingsreacties rond eiwitafzettingen in menselijke Alzheimerhersenen, wat suggereert dat het apenmodel een belangrijke immuunreactie vastlegt die in veel muizenstudies ontbreekt of verzacht is.
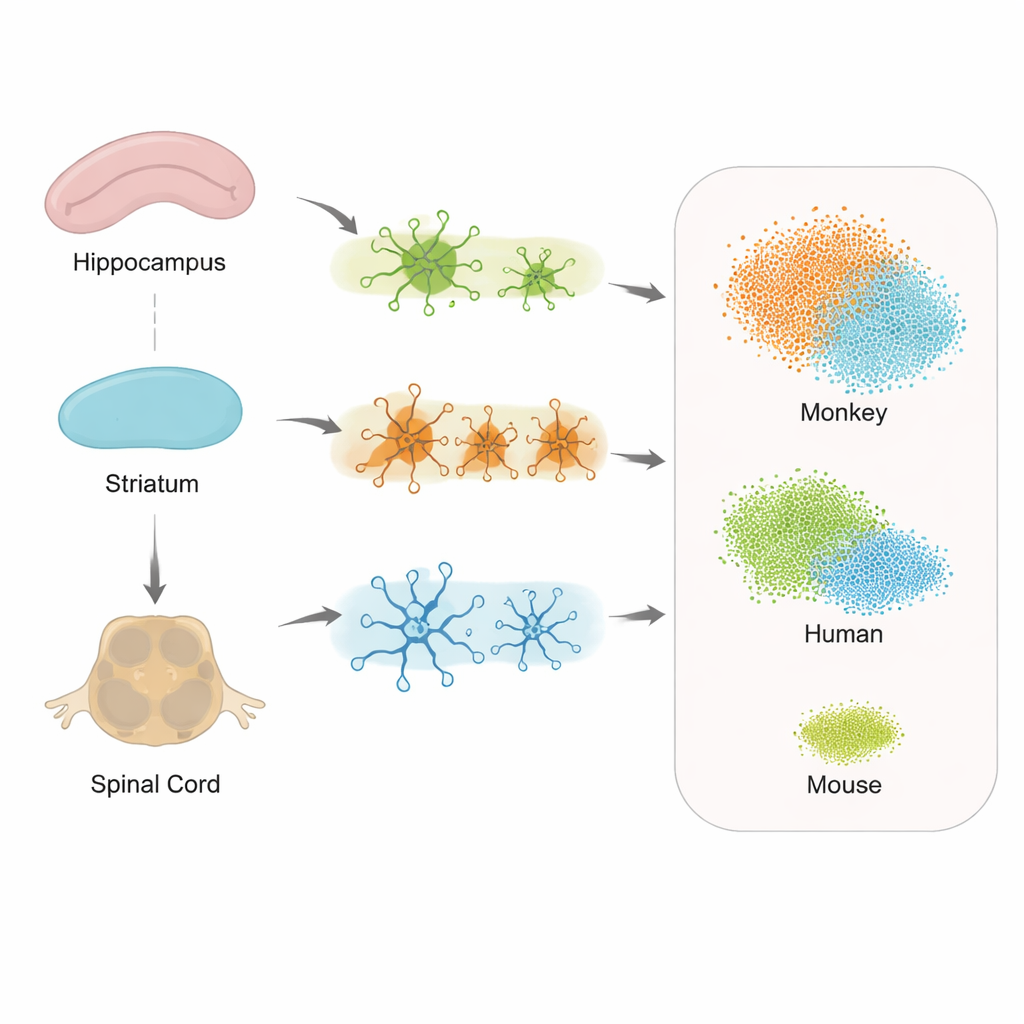
Verschillende regio’s, verschillende cellulaire reacties
Toen de onderzoekers onderzochten hoe genexpressie veranderde in ondersteunende cellen in de hippocampus, het striatum en het ruggenmerg, zagen ze zowel gedeelde als regiogebonden reacties op tau‑pathologie. Astrocyten, microglia en oligodendrocyten toonden allemaal gewijzigde activiteit, maar de precieze sets genen verschilden per locatie. Dit suggereert dat elk deel van het zenuwstelsel zijn eigen variant van een stressrespons optuigt, wat kan helpen verklaren waarom sommige symptomen, zoals looppatronen, eerder optreden dan duidelijke geheugenproblemen. Belangrijk is dat het ruggenmerg sterke betrokkenheid liet zien, wat de gedachte ondersteunt dat Alzheimer niet alleen een ziekte van de hersenen is, maar van het bredere centrale zenuwstelsel.
Aapgegevens die opvallend menselijk lijken
Om te testen hoe goed het apenmodel de menselijke ziekte weerspiegelt, vergeleek het team hun hippocampale gegevens met bestaande datasets van mensen met vroeg‑beginende Alzheimer en met een ander tau‑mutant muismodel. Ze concentreerden zich op microglia en op een speciale “disease-associated” toestand van deze cellen die bij menselijke patiënten is beschreven. De genactiviteitspatronen in apenmicroglia overlapten veel meer met die in menselijke hersenen dan met de muizenpatronen, inclusief veel belangrijke immuun‑ en stressgerelateerde genen die in muizen nauwelijks veranderden. Dit geeft aan dat de Tau‑P301L‑aap human‑achtige ziektesignaturen op single-cell niveau beter vastlegt dan huidige knaagdiermodellen.
Wat dit betekent voor toekomstig Alzheimer‑onderzoek
Voor niet‑specialisten is de belangrijkste boodschap dat deze studie een rijke, openbaar beschikbare cel‑voor‑cel kaart levert van hoe een gehumaniseerd tau‑eiwit hersen‑ en ruggenmergcellen verstoort in een soort die veel dichter bij ons staat dan muizen. De atlas benadrukt welke celtypes en regio’s het meest worden getroffen en laat zien dat het apenmodel immuuncelveranderingen meer getrouw reproduceert dan standaard muismodellen. Daardoor bieden deze gegevens een waardevol testveld voor ideeën over hoe Alzheimer begint en zich verspreidt, en kunnen ze onderzoekers helpen therapieën te ontwerpen die een betere kans hebben te werken wanneer ze uiteindelijk mensen bereiken.
Bronvermelding: Han, B., Chen, Y., Ouyang, W. et al. Single-nucleus RNA sequencing dataset of diverse tissues from wild-type monkey and Tau-P301L transgenic monkey. Sci Data 13, 497 (2026). https://doi.org/10.1038/s41597-026-06882-4
Trefwoorden: Ziekte van Alzheimer, tau-eiwit, niet-menselijk primatenmodel, single-cell RNA-sequencing, microglia