Clear Sky Science · pt
Conjunto de dados de RNA-seq de núcleo único de tecidos diversos de macaco selvagem e macaco transgênico Tau-P301L
Por que Este Estudo em Macacos Importa
A doença de Alzheimer é mais conhecida por roubar a memória das pessoas, mas também altera o movimento, o equilíbrio e a saúde de muitos tipos de células cerebrais. Para projetar tratamentos melhores, os cientistas precisam de modelos animais que imitem a condição humana o mais fielmente possível. Este estudo introduz um mapa celular detalhado de um macaco especialmente modificado que desenvolve mudanças semelhantes às da Alzheimer, oferecendo uma nova janela poderosa sobre como diferentes células do cérebro e da medula espinhal respondem à medida que a doença surge.
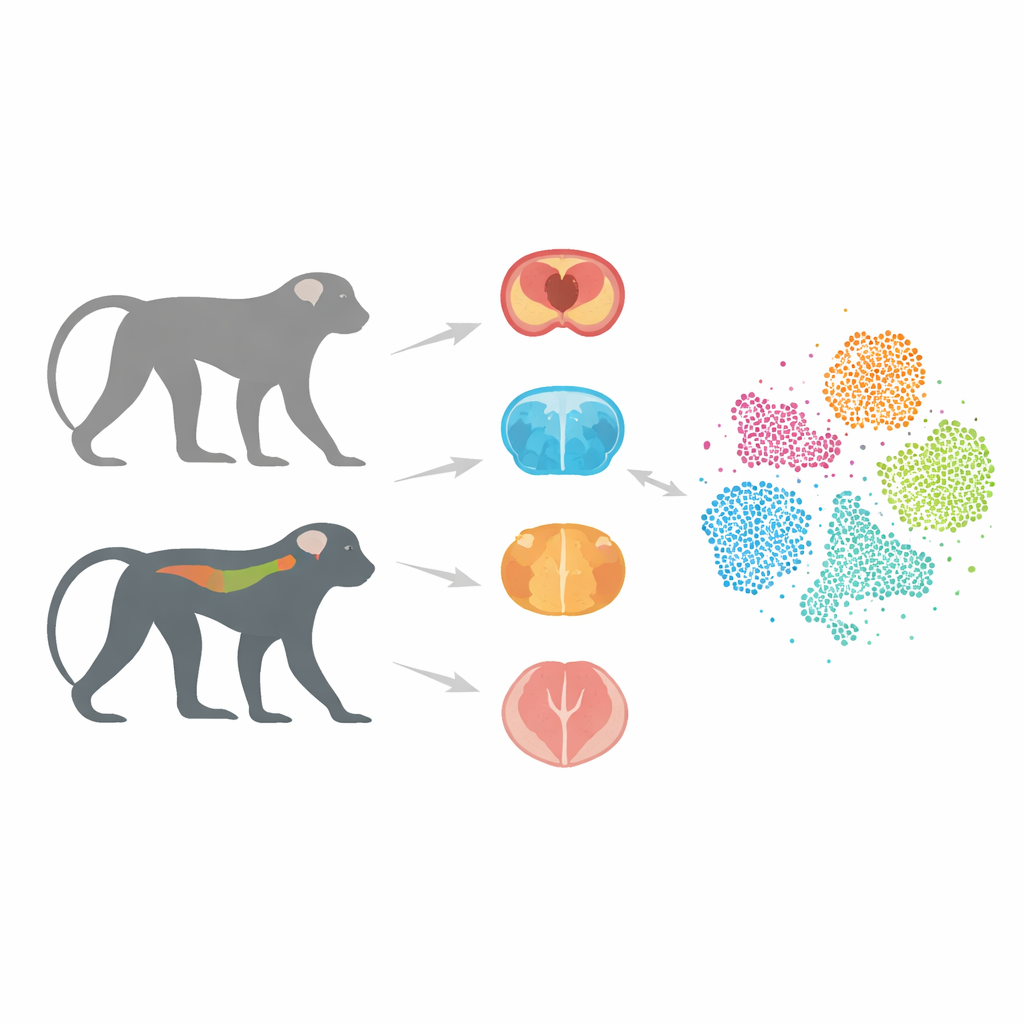
Um Substituto Animal Mais Próximo dos Humanos
A maior parte da pesquisa sobre Alzheimer tem se apoiado em camundongos que carregam genes humanos associados à doença. Esses modelos ensinaram muito aos pesquisadores, mas muitas vezes falham em prever se um possível medicamento funcionará em pessoas. Uma grande razão é que o cérebro e o sistema imunológico dos camundongos diferem consideravelmente dos nossos. Os macacos, por contraste, compartilham uma estrutura cerebral e um conjunto genético muito mais semelhantes aos humanos. Em trabalhos anteriores, os autores criaram macacos cynomolgus que carregam uma versão humana da proteína tau, chamada Tau-P301L, que se agrega anormalmente em várias demências. Esses macacos desenvolvem gradualmente danos aos neurônios e problemas de movimento, assemelhando-se a características centrais das doenças humanas impulsionadas pela tau.
Lendo as Mensagens Dentro de Milhares de Células
Neste projeto, a equipe concentrou-se em três regiões-chave: o hipocampo, importante para a memória; o estriado, envolvido em movimento e motivação; e a medula espinhal, que ajuda a controlar a postura e a marcha e é cada vez mais reconhecida como parte do quadro da Alzheimer. De macacos transgênicos e saudáveis, os pesquisadores isolaram núcleos individuais de células desses tecidos e usaram sequenciamento de RNA de núcleo único. Essa técnica lê quais genes estão ativos em cada célula, permitindo que os cientistas distingam tipos e estados celulares com grande precisão. Após rigorosas verificações de qualidade para remover células danificadas e erros técnicos, eles compilaram um atlas de 36.623 células de alta qualidade.
Um Mapa Celular do Sistema Nervoso do Macaco
Agrupando células com padrões semelhantes de atividade gênica, a equipe identificou 13 tipos celulares principais, incluindo neurônios, vários tipos de células de suporte como astrócitos e oligodendrócitos, microglia com função imunológica e populações raras como células T e células da zona ventricular. Eles verificaram cada grupo usando genes marcadores conhecidos e mostraram que os aglomerados eram limpos e consistentes. Comparando macacos doentes e saudáveis, encontraram que certas microglias — um tipo de célula imunológica do cérebro — se expandiram nos animais Tau-P301L. Essas microglias expressavam genes previamente ligados à detecção de danos e respostas inflamatórias observadas ao redor de depósitos de proteína em cérebros humanos com Alzheimer, sugerindo que o modelo de macaco captura uma reação imune importante ausente ou atenuada em muitos estudos com camundongos.
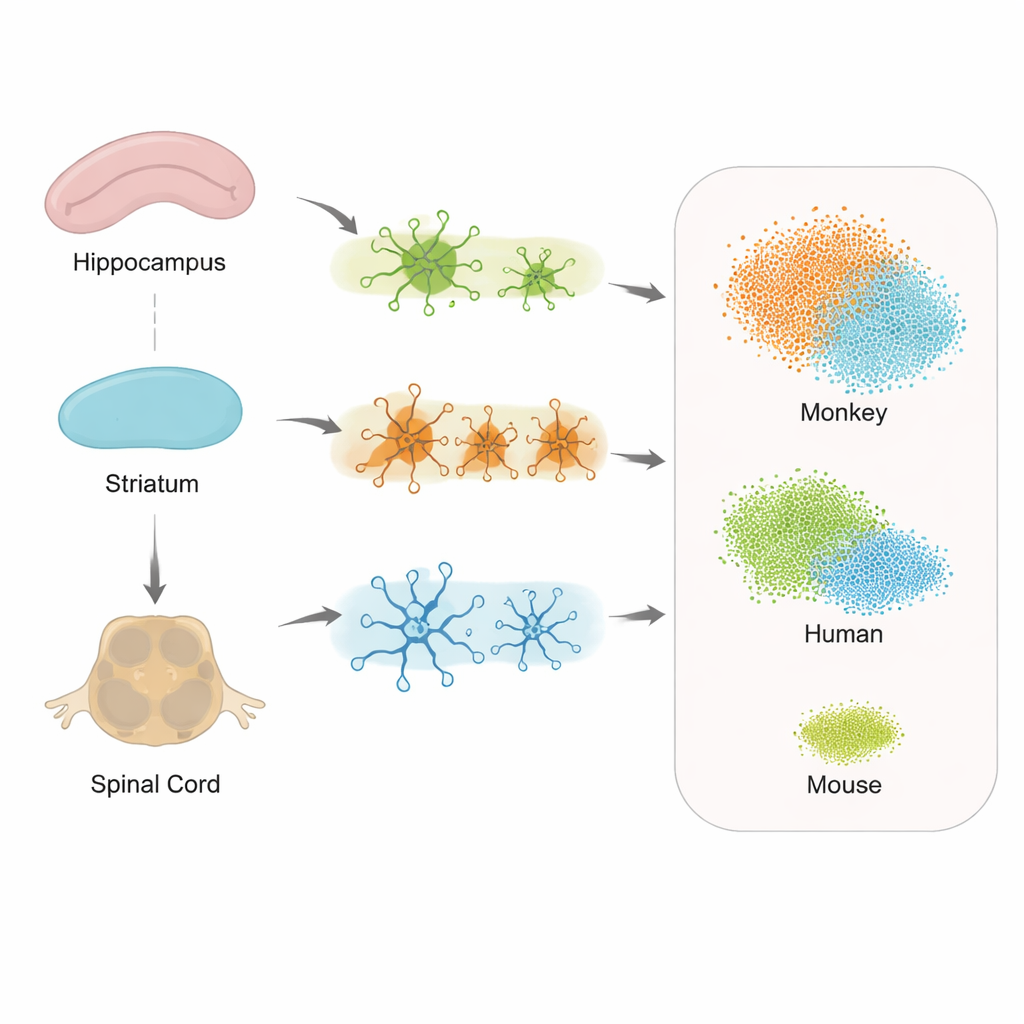
Regiões Diferentes, Respostas Celulares Diferentes
Quando os pesquisadores examinaram como os genes mudavam nas células de suporte do hipocampo, estriado e medula espinhal, observaram respostas tanto compartilhadas quanto específicas por região à patologia tau. Astrócitos, microglia e oligodendrócitos mostraram atividade alterada, mas os conjuntos exatos de genes variaram conforme a localização. Isso sugere que cada parte do sistema nervoso monta sua própria versão de uma resposta ao estresse, o que pode ajudar a explicar por que alguns sintomas, como dificuldades para caminhar, podem aparecer antes da perda óbvia de memória. Importante, a medula espinhal mostrou forte envolvimento, apoiando a ideia de que a Alzheimer não é apenas uma doença do cérebro, mas do sistema nervoso central mais amplo.
Dados de Macaco que Parecem Notavelmente Humanos
Para testar o quanto o modelo de macaco reflete a doença humana, a equipe comparou seus dados do hipocampo com conjuntos de dados existentes de pessoas com Alzheimer de início precoce e com outro modelo murino com mutação na tau. Eles se concentraram nas microglias e em um estado especial "associado à doença" dessas células que foi descrito em pacientes humanos. Os padrões de atividade gênica nas microglias de macaco se sobrepuseram muito mais com os dos cérebros humanos do que os padrões murinos, incluindo muitos genes-chave relacionados à imunidade e ao estresse que mal mudaram em camundongos. Isso indica que o macaco Tau-P301L captura assinaturas de doença mais semelhantes às humanas no nível de célula única do que os modelos roedores atuais.
O Que Isso Significa para Pesquisas Futuras sobre Alzheimer
Para não especialistas, a principal mensagem é que este estudo fornece um mapa rico, publicamente disponível, célula a célula, de como uma proteína tau humanizada perturba células do cérebro e da medula espinhal em uma espécie muito mais próxima de nós do que os camundongos. O atlas destaca quais tipos celulares e regiões são mais afetados e mostra que o modelo de macaco reproduz mudanças em células imunes humanas com mais fidelidade do que modelos murinos padrão. Como resultado, esses dados oferecem um campo valioso para testar ideias sobre como a Alzheimer começa e se espalha, e podem ajudar pesquisadores a projetar terapias com maior chance de funcionar quando chegarem finalmente aos pacientes humanos.
Citação: Han, B., Chen, Y., Ouyang, W. et al. Single-nucleus RNA sequencing dataset of diverse tissues from wild-type monkey and Tau-P301L transgenic monkey. Sci Data 13, 497 (2026). https://doi.org/10.1038/s41597-026-06882-4
Palavras-chave: Doença de Alzheimer, proteína tau, modelo de primata não humano, sequenciamento de RNA de célula única, microglia