Clear Sky Science · zh
自身免疫性神经炎通过MIF核酸酶介导的parthanatos导致神经元死亡
为何大脑中的炎症很重要
多发性硬化及相关疾病不仅攻击神经纤维周围的髓鞘——它们也会逐步杀死神经细胞本身。这种隐匿的神经元损失会推动行走、视力和认知方面的问题,即便复发得到控制后仍可持续存在。这里总结的研究提出了一个基本但至关重要的问题:在大脑和脊髓的自身免疫性炎症中,神经元究竟如何死亡?是否可以在不完全抑制免疫系统的情况下阻断这一过程?
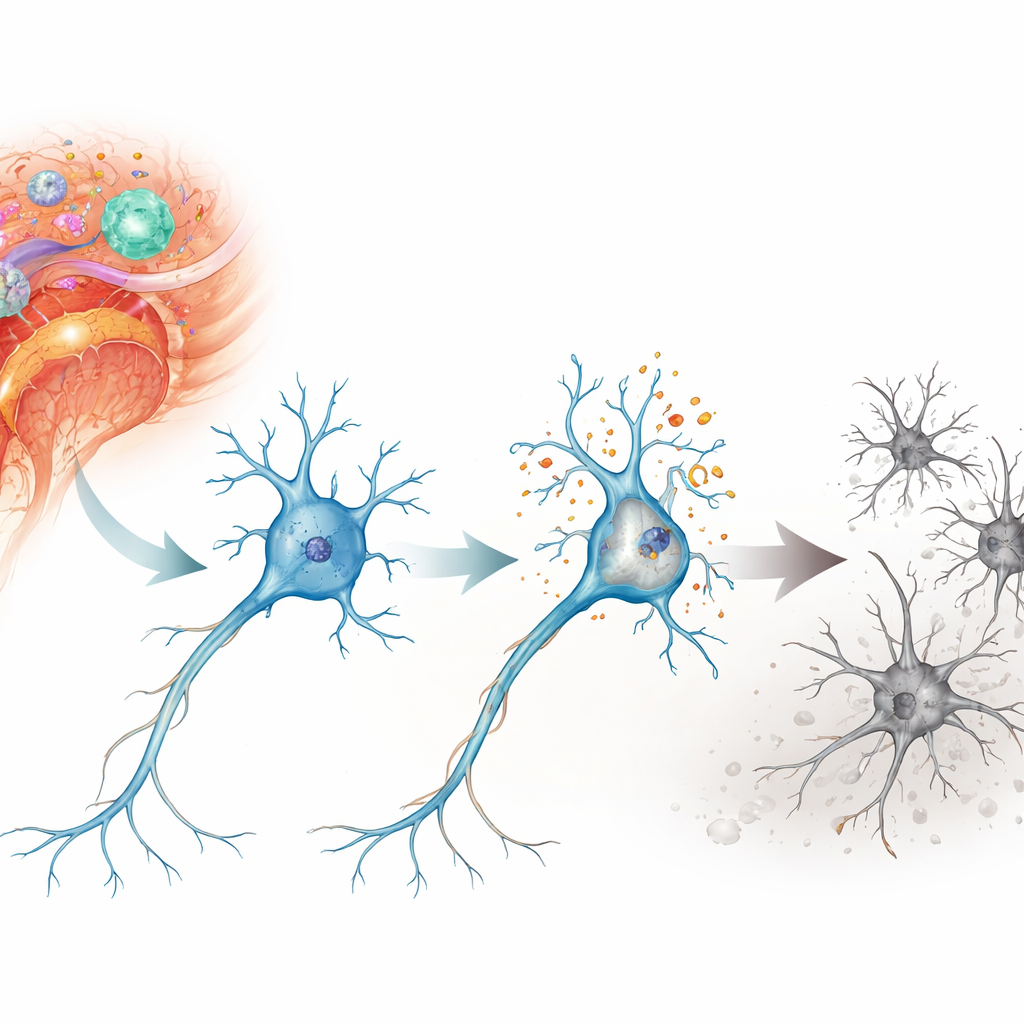
神经元内的一连串破坏反应
研究者关注一种称为parthanatos的细胞死亡形式,这是一种由严重DNA损伤触发的程序性死亡,而不是更常见的细胞自杀路径——凋亡。在一种称为实验性自身免疫性脑脊髓炎的小鼠模型中,他们检查了脊髓和视网膜中的神经元——这些区域在多发性硬化中受损明显。他们在这些神经元中发现了明显的DNA断裂和氧化应激信号,尤其是在脊髓的运动神经元和将眼睛与大脑连接的视网膜神经节细胞中。数日到数周内,这些细胞逐步丧失,其时间进程与动物中神经功能障碍的恶化相吻合。
遵循一种名为parthanatos的死亡脚本
深入观察时,团队追踪了受影响神经元内parthanatos的分子步骤。当DNA受损时,细胞核内的一种酶PARP1变得过度活跃并产生长链的分子PAR。这些PAR链溢出到细胞体内,帮助触发线粒体蛋白AIF的释放,AIF与另一种蛋白巨噬细胞迁移抑制因子(MIF)结合。AIF–MIF复合体随后回到细胞核。在那里,MIF充当核酸酶——一种切割DNA的酶——导致基因组的大规模断裂并决定了神经元的命运。作者在小鼠疾病高峰期检测到这些标志性变化,包括过量的PAR、AIF–MIF结合以及MIF在神经元细胞核中的积累,在一例多发性硬化患者的人脑组织中也观察到程度较轻的类似现象。
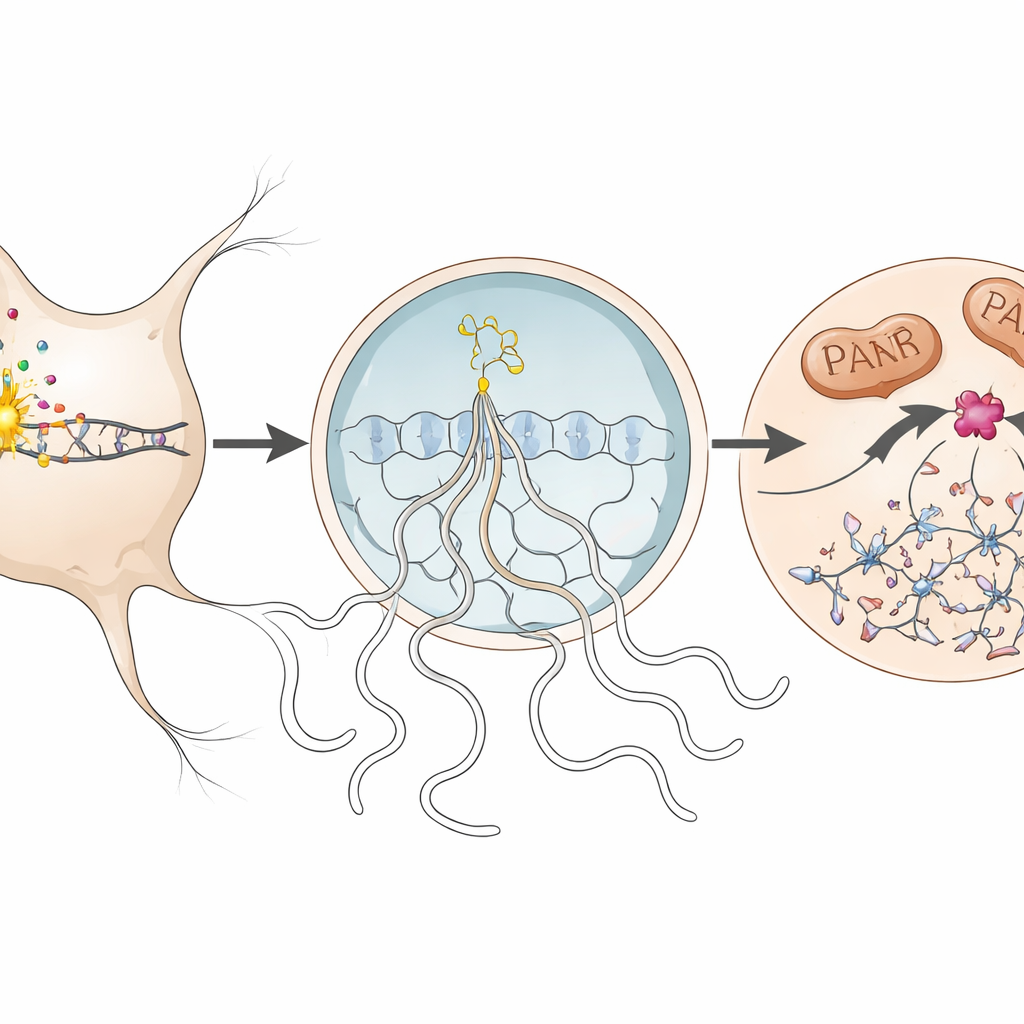
通过解除单一酶的武装来保护神经元
为检验这一通路是否真正驱动神经元丧失,研究者用两种互补的方法破坏了MIF的核酸酶活性。首先,他们使用了一种敲入小鼠,携带MIF的一处微小突变(E22Q),该突变保留了MIF的其它功能但使其不能切割DNA。在这些动物中,针对髓鞘的自身免疫攻击和免疫细胞进入脊髓的情况未见改变,但脊髓和视网膜中的神经元明显得到更好保存,长期残疾评分也低于正常小鼠。其次,他们使用PAANIB-1这种小分子选择性阻断MIF的核酸酶活性。无论是预先给药还是在症状出现后给药,该药在疾病慢性期均减少了神经元丧失,而不改变免疫细胞浸润、胶质细胞活化或脱髓鞘的程度。
当parthanatos被阻断时神经元的不同反应
团队接着探究幸存神经元在基因表达层面上有哪些不同。通过对脊髓组织进行单细胞核RNA测序,他们对数万例来自有病或无病的正常小鼠与MIF突变小鼠的神经元进行了表达谱分析。在伴有自身免疫炎症的标准小鼠中,神经元启动了许多与免疫相关的基因,包括响应干扰素信号和参与抗原呈递的通路,同时下调了对正常电信号传导、神经递质通讯和保护性生长因子产生重要的基因。相比之下,MIF突变小鼠的神经元在很大程度上保持了这些核心功能性基因的表达,尽管某些炎症程序甚至更强烈地被激活。对人类多发性硬化脑组织数据的再分析显示了类似的长期基础神经功能基因抑制,提示小鼠的发现反映了人体中的变化。
这对未来治疗意味着什么
综合来看,结果指向parthanatos——特别是由MIF执行的最终DNA切割步骤——作为炎症在自身免疫疾病中杀死神经元的关键途径。重要的是,阻断MIF的核酸酶活性保护了神经元而不抑制更广泛的免疫反应或改变髓鞘丧失,且被保护的神经元似乎保留了更健康的基因表达模式。对大众读者而言,结论是这项工作识别出一个明确的分子“关闭开关”,用于切断神经元内的破坏性死亡程序。针对性药物如果能翻转这一开关,理论上可在现有以免疫为主的多发性硬化及其他脑脊髓炎症性疾病治疗中,增添真正的神经保护作用。
引用: Mace, J.W., Gadani, S.P., Smith, M.D. et al. Autoimmune neuroinflammation leads to neuronal death via MIF nuclease-mediated parthanatos. Nat Neurosci 29, 796–809 (2026). https://doi.org/10.1038/s41593-026-02201-7
关键词: 多发性硬化, 神经炎症, 神经元细胞死亡, parthanatos, MIF核酸酶