Clear Sky Science · sv
Autoimmun neuroinflammation leder till neurons död via MIF-nukleasmedierad parthanatos
Varför inflammation i hjärnan är viktig
Multipel skleros och närliggande sjukdomar angriper inte bara isoleringen runt nervtrådarna — de dödar också nervcellerna själva, om än långsamt. Denna dolda förlust av neuroner driver gång-, syn- och kognitiva problem som kan fortsätta även när skov är under kontroll. Studien som sammanfattas här ställer en grundläggande men avgörande fråga: under autoimmun inflammation i hjärnan och ryggmärgen, hur dör neuronerna exakt, och kan den processen blockeras utan att helt slå ut immunsystemet?
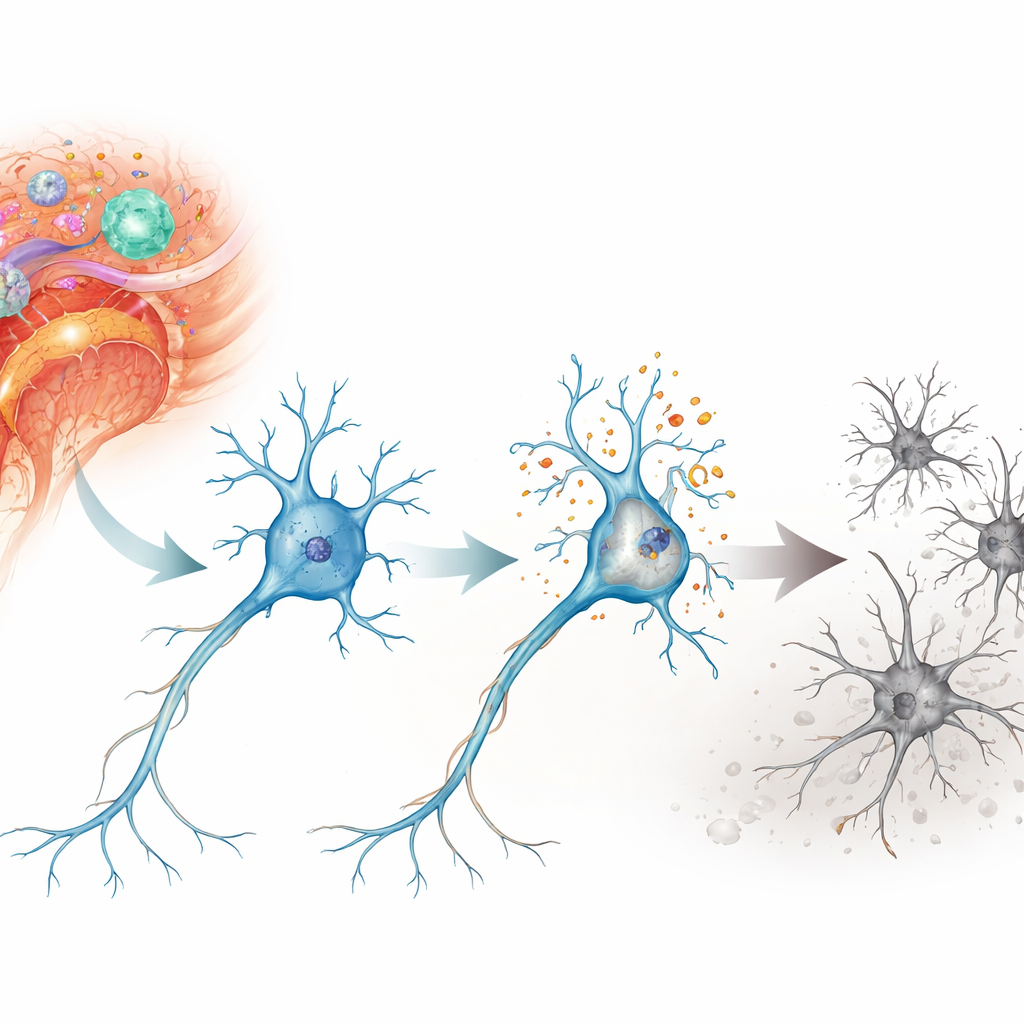
En skadlig kedjereaktion inne i neuronerna
Forskarna fokuserade på en form av celldöd kallad parthanatos, ett program som utlöses av omfattande DNA-skador snarare än genom den mer bekanta självmordsvägen apoptos. I en musmodell för autoimmun neuroinflammation, känd som experimentell autoimmun encefalomyelit, undersökte de neuroner i ryggmärgen och näthinnan — regioner som skadas vid multipel skleros. De fann tydliga tecken på DNA-brott och oxidativ stress i dessa neuroner, särskilt i motorneuroner i ryggmärgen och i ganglieceller i näthinnan som förbinder ögat med hjärnan. Över dagar till veckor förlorades dessa celler gradvis, i takt med djurets försämrade neurologiska funktion.
Följer ett dödsskript kallat parthanatos
Närmare granskning visade att teamet spårade parthanatos molekylära steg inne i de drabbade neuronerna. När DNA skadades blev ett enzym i cellkärnan, PARP1, överaktivt och producerade långa kedjor av en molekyl kallad PAR. Dessa kedjor läckte ut i cellkroppen, där de medverkade till frisättning av ett mitokondriellt protein (AIF) som samarbetar med ett annat protein, macrophage migration inhibitory factor (MIF). AIF–MIF-komplexet rörde sig sedan tillbaka in i kärnan. Där agerade MIF som ett nukleas — ett enzym som klipper DNA — vilket orsakade storskalig fragmentering av genomet och avgjorde neuronens öde. Författarna detekterade var och en av dessa kännetecken, inklusive överskott av PAR, AIF–MIF-bindning och ackumulering av MIF i neuronernas kärnor, under sjukdomstoppen hos mössen och, i begränsad omfattning, i mänsklig hjärnvävnad från en person med multipel skleros.
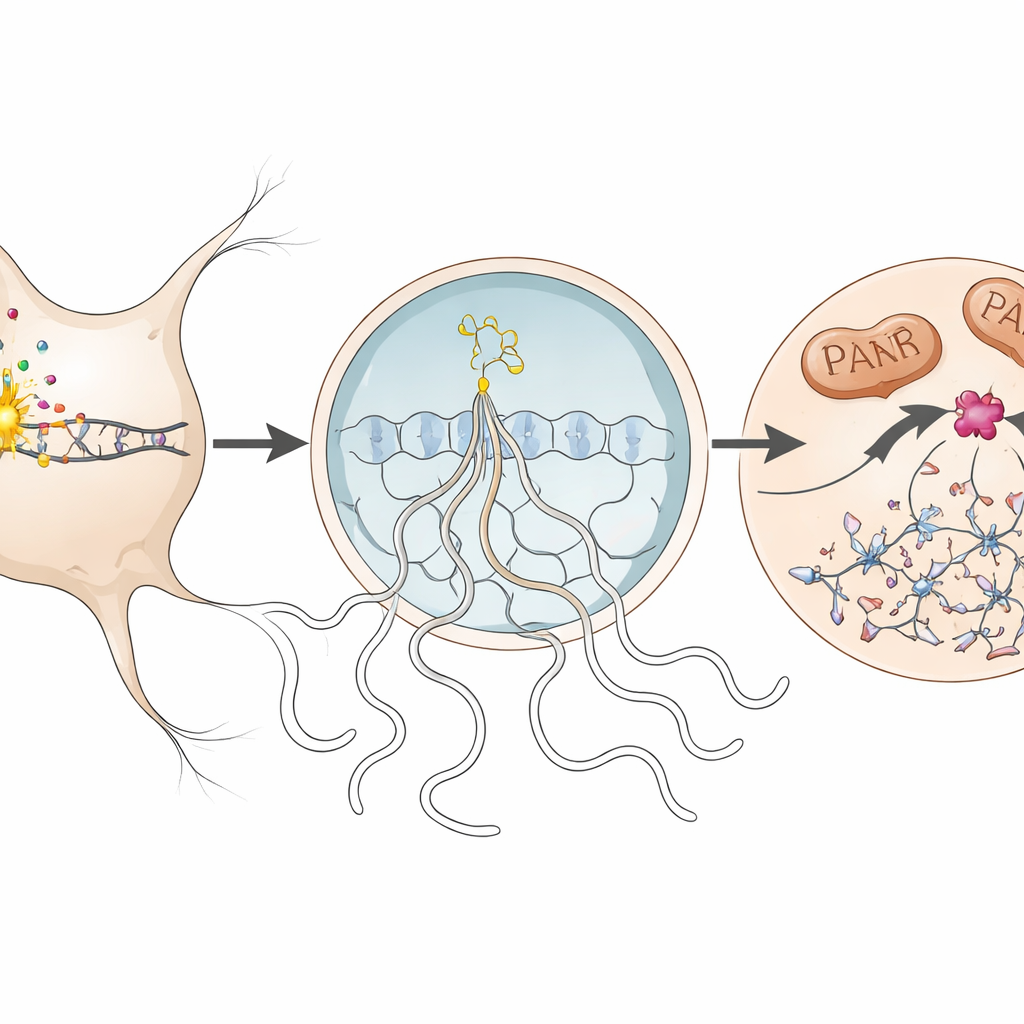
Skydda neuroner genom att oskadliggöra ett enskilt enzym
För att testa om denna väg faktiskt driver neuronförlust inaktiverade forskarna MIF:s nukleasaktivitet på två kompletterande sätt. Först använde de en knock-in-mus som bär en subtil mutation i MIF (E22Q) som lämnar dess andra funktioner intakta men förhindrar att det klipper DNA. Hos dessa djur var det autoimmuna angreppet på myelinet och inflödet av immunceller till ryggmärgen oförändrat, men neuroner i ryggmärgen och näthinnan bevarades signifikant bättre och långtidsfunktionsmått var lägre än hos normala möss. För det andra behandlade de mössen med PAANIB-1, ett småmolekylärt ämne som selektivt blockerar MIF:s nukleasaktivitet. Oavsett om det gavs profylaktiskt eller efter att symtomen börjat, minskade läkemedlet neuronförlust i den kroniska sjukdomsfasen utan att påverka immuncellsinfiltration, gliacellaktivering eller graden av demyelinisering.
Neuroner svarar annorlunda när parthanatos blockeras
Teamet undersökte därefter hur överlevande neuroner skiljde sig på genaktivitetsnivå. Med singelnukleär RNA-sekvensering av ryggmärgsvävnad profiltade de tiotusentals neuroner från normala och MIF-mutanta möss med och utan sjukdom. Hos standardmössen med autoimmun inflammation aktiverade neuroner många immunrelaterade gener, inklusive vägar som svarar på interferonsignaler och hjälper till att presentera antigener, samtidigt som gener viktiga för normal elektrisk signalering, neurotransmittorkommunikation och produktion av skyddande tillväxtfaktorer nedreglerades. I kontrast behöll neuroner i MIF-mutanta möss mycket av denna grundfunktionella genuttryck, även om vissa inflammatoriska program var ännu mer aktiverade. En omanalys av mänskliga multipel skleros-data visade en liknande långvarig undertryckning av grundläggande neuronala funktionsgener, vilket tyder på att fynden hos möss återspeglar förändringar hos människor.
Vad detta betyder för framtida behandlingar
Sammantaget pekar resultaten på parthanatos — specifikt det slutliga DNA-klippsteget utfört av MIF — som en nyckelväg genom vilken inflammation dödar neuroner vid autoimmun sjukdom. Viktigt är att blockering av MIF:s nukleasaktivitet räddade neuroner utan att dämpa den bredare immunresponsen eller ändra myelinförlusten, och de skyddade neuronerna verkade behålla hälsosammare genuttrycksmönster. För en allmän läsare innebär slutsatsen att detta arbete identifierar en konkret molekylär ”avstängningsknapp” för ett destruktivt dödsprogram inne i neuronerna. Målinriktade läkemedel som slår om den här knappen skulle i princip kunna ge verkligt neuroprotektionstillägg till befintliga immunfokuserade behandlingar för multipel skleros och andra inflammatoriska tillstånd i hjärnan och ryggmärgen.
Citering: Mace, J.W., Gadani, S.P., Smith, M.D. et al. Autoimmune neuroinflammation leads to neuronal death via MIF nuclease-mediated parthanatos. Nat Neurosci 29, 796–809 (2026). https://doi.org/10.1038/s41593-026-02201-7
Nyckelord: multipel skleros, neuroinflammation, neuronal celldöd, parthanatos, MIF-nukleas