Clear Sky Science · tr
Otoimmün nöroenflamasyon, MIF nükleaz aracılı parthanatos yoluyla nöron ölümüne yol açar
Beyindeki iltihap neden önemli?
Multipl skleroz ve ilişkili hastalıklar yalnızca sinir liflerinin etrafındaki yalıtımı (miyelin) hedef almaz—aynı zamanda sinir hücrelerini (nöronları) da yavaş yavaş öldürür. Bu gizli nöron kaybı, ataklar kontrol altına alınsa bile yürüyüş, görme ve düşünme ile ilgili bozuklukların sürmesine neden olabilir. Burada özetlenen çalışma temel ama kritik bir soruyu ele alıyor: Beyin ve omuriliğin otoimmün inflamasyonu sırasında nöronlar tam olarak nasıl ölüyor ve bu sürecin tamamında bağışıklık sistemini bütünüyle kapatmadan engellenmesi mümkün mü?
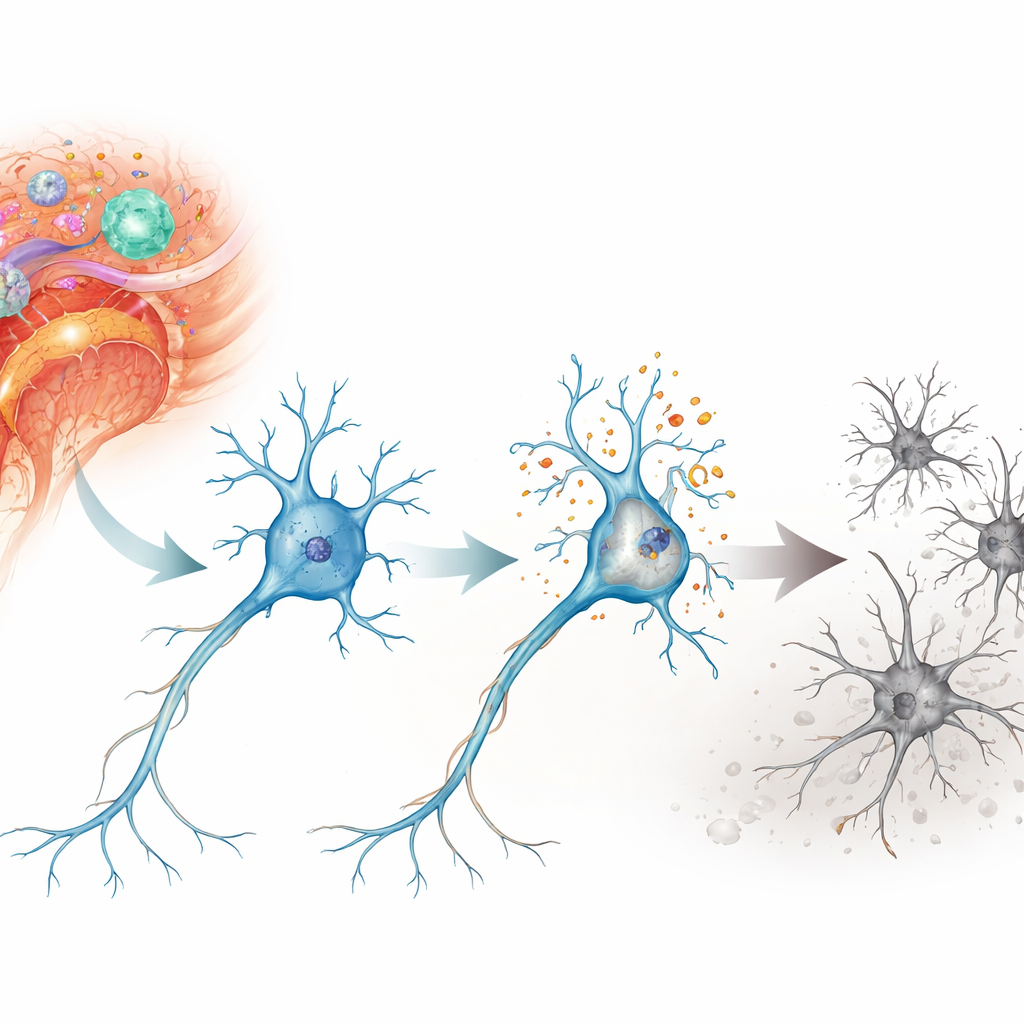
Nöronların içinde hasar verici bir zincirleme reaksiyon
Araştırmacılar, parthanatos adı verilen bir hücre ölümü biçimine odaklandı; bu program, daha yaygın bilinen intihar yolu olan apoptozdan ziyade şiddetli DNA hasarıyla tetiklenir. Deneysel otoimmün ensefalomiyelit olarak bilinen otoimmün nöroenflamasyonun fare modelinde, multipl sklerozda zarar gören omurilik ve retina nöronlarını incelediler. Özellikle omuriliğin motor nöronları ve gözü beyne bağlayan retinal ganglion hücrelerinde güçlü DNA kırıkları ve oksidatif stres belirtileri buldular. Günlerden haftalara kadar süren bir zaman diliminde bu hücreler kademeli olarak kayboldu; bu kayıp hayvanlardaki kötüleşen nörolojik yetmezlik zaman çizelgesiyle örtüştü.
Parthanatos adlı ölüm senaryosunu izlemek
Daha yakından bakıldığında ekip, etkilenen nöronlardaki parthanatosun moleküler adımlarını izledi. DNA hasarlandığında, çekirdekteki PARP1 adlı bir enzim aşırı aktif hale geldi ve PAR adı verilen uzun molekül zincirleri üretti. Bu zincirler hücre gövdesine sızdı ve mitokondriden bir protein (AIF) salınımını tetiklemeye yardımcı oldu; AIF, makrofaj göçünü engelleme faktörü (MIF) adlı başka bir proteinle eşlik etti. AIF–MIF kompleksi sonra çekirdeğe geri girdi. Orada MIF, DNA’yı kesen bir nükleaz olarak davrandı ve genomun büyük ölçekli parçalanmasına neden olarak nöronun kaderini belirledi. Yazarlar, aşırı PAR birikimi, AIF–MIF bağlanması ve MIF’in nöronal çekirdekte birikmesi de dahil olmak üzere bu belirteçlerin her birini farelerde hastalık zirvesi sırasında ve sınırlı ölçüde bir multipl sklerozlu insan beyin dokusunda tespit ettiler.
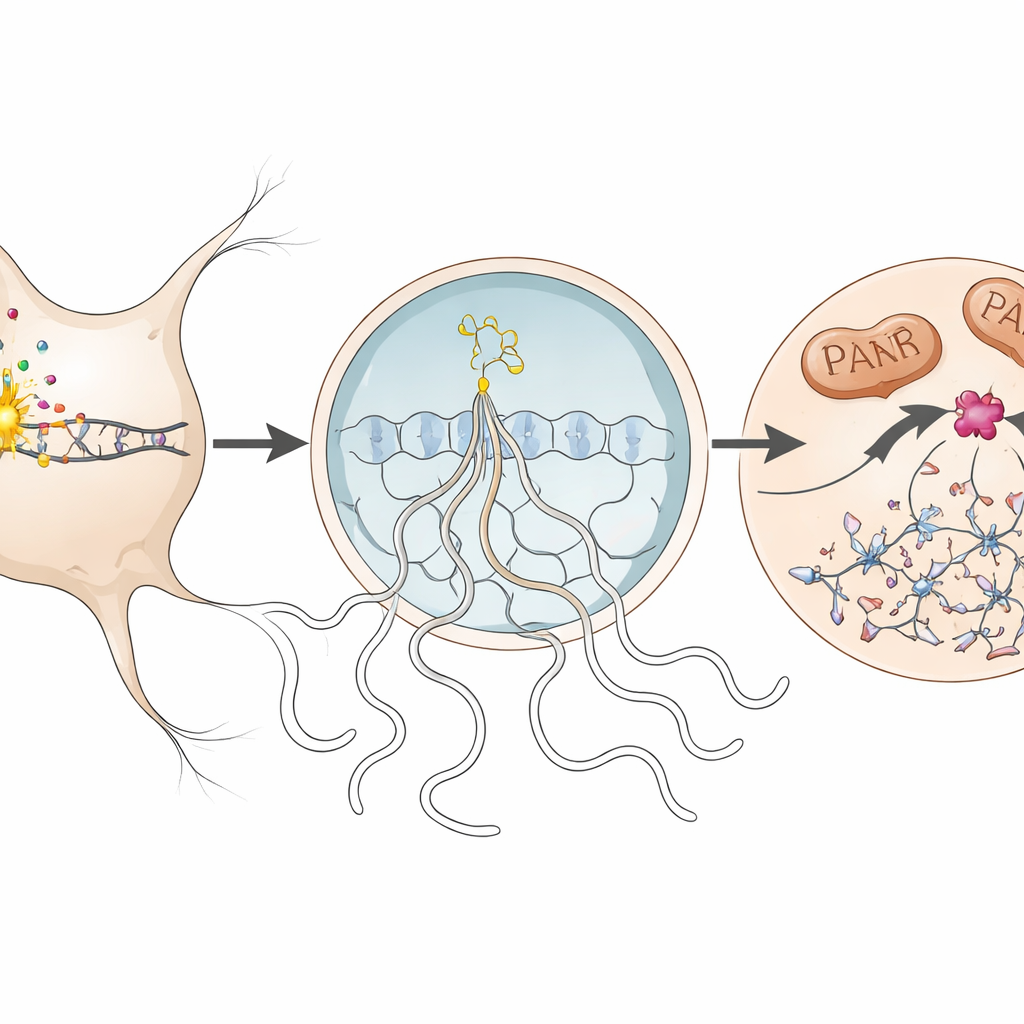
Tek bir enzimi etkisiz hale getirerek nöronları korumak
Bu yol gerçekten nöron kaybını mı yönlendiriyor test etmek için araştırmacılar MIF’in nükleaz aktivitesini iki tamamlayıcı yolla devre dışı bıraktı. Önce, MIF’te diğer işlevlerini koruyan ancak DNA’yı kesmesini engelleyen ince bir mutasyon (E22Q) taşıyan bir knock-in fare kullandılar. Bu hayvanlarda miyeline yönelik otoimmün saldırı ve omuriliğe immün hücre akını değişmedi; buna karşın omurilik ve retinadaki nöronlar anlamlı şekilde daha iyi korunmuştu ve uzun dönem engel skorları normal farelere göre daha düşüktü. İkinci olarak, MIF’in nükleaz aktivitesini seçici olarak engelleyen küçük bir molekül olan PAANIB-1 ile fareleri tedavi ettiler. Hem önleyici olarak hem de semptomlar başladıktan sonra verildiğinde, bu ilaç kronik hastalık fazında nöron kaybını azalttı; immün hücre infiltrasyonu, glial aktivasyon veya demiyelinizasyon derecesini değiştirmedi.
Parthanatos engellendiğinde nöronlar farklı tepki veriyor
Ekip daha sonra hayatta kalan nöronların gen etkinliği düzeyinde nasıl farklılaştığını sordu. Tek-nükleus RNA dizileme kullanarak omurilik dokusundan on binlerce nöronu, hem hastalıklı hem de sağlıklı MIF-mutant ve normal farelerden profillendiler. Otoimmün inflamasyonlu standart farelerde nöronlar, interferon sinyallerine yanıt veren ve antijen sunumuna yardımcı olan yollar dahil birçok bağışıklık ilişkili geni açarken, normal elektriksel sinyal iletimi, nörotransmitter iletişimi ve koruyucu büyüme faktörlerinin üretimi için önemli genleri kapattılar. Buna karşılık, MIF-mutant farelerdeki nöronlar bu temel fonksiyonel gen ifadesinin büyük bir kısmını korudu; bazı inflamatuar programlar ise daha güçlü biçimde aktive olmuştu. İnsan multipl skleroz beyin verilerinin yeniden analizi, temel nöronal fonksiyon genlerinin uzun vadeli baskılanmasını gösterdi; bu da fare bulgularının insanlardaki değişiklikleri yansıttığını düşündürüyor.
Gelecekteki tedaviler açısından ne anlama geliyor?
Toparlarsak, bulgular parthanatosu—özellikle MIF tarafından gerçekleştirilen son DNA kesme adımını—otoimmün hastalıkta inflamasyonun nöronları öldürmesinin ana yollarından biri olarak işaretliyor. Önemli olan, MIF’in nükleaz aktivitesinin engellenmesinin daha geniş bağışıklık yanıtını zayıflatmadan veya miyelin kaybını değiştirmeden nöronları koruması ve korunan nöronların daha sağlıklı gen ifade desenlerini sürdürmesi oldu. Bilgi düzeyi genel okuyucu için özetle bu çalışma, nöronlar içindeki yıkıcı bir ölümü başlatan moleküler bir “kapatma düğmesi”ni somutlaştırıyor. Bu düğmeyi hedef alan ilaçlar, teoride, multipl skleroz ve beyin ile omuriliğin diğer inflamatuvar durumları için bağışıklık odaklı mevcut tedavilere gerçek bir nörokoruma ekleyebilir.
Atıf: Mace, J.W., Gadani, S.P., Smith, M.D. et al. Autoimmune neuroinflammation leads to neuronal death via MIF nuclease-mediated parthanatos. Nat Neurosci 29, 796–809 (2026). https://doi.org/10.1038/s41593-026-02201-7
Anahtar kelimeler: multipl skleroz, nöroenflamasyon, nöronal hücre ölümü, parthanatos, MIF nükleaz